29. 甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。
Ⅰ.利用甲醇(CH
3HO)制备甲醛
脱氢法:CH
3OH(g)
⇌ HCHO(g)+H
2 (g) ΔH
1=+92.09kJ·mol
-1氧化法:CH
3OH(g)+1/2O
2(g)
⇌HCHO(g)+H
2O(g) ΔH
2(1)脱氢法制甲醛,有利于提高平衡产率的条件有
________ (写出一条)。
(2)已知:2 H
2(g) + O
2(g)= 2H
2O(g) ΔH
3=-483.64kJ·mol
-1,则ΔH
2=
________________。
(3)750K 下,在恒容密闭容器中,充入一定量的甲醇,发生脱氢法反应,若起始压强为P
0,达到平衡时转化率为40.0% ,则反应的平衡常数K
p=
________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,忽略其它反应)。
(4)Na
2CO
3是脱氢法反应的催化剂,有研究指出,催化反应的部分机理如下:
历程i :CH
3OH→·H+ ·CH
2OH 历程ii :·CH
2OH→·H+ HCHO
历程iii:.·CH
2OH→3·H +CO 历程iv:·H+·H→H
2如图所示为在体积为1L的恒容容器中,投入1mol CH
3OH,在碳酸钠催化剂作用下,经过10min反应,测得甲醇的转化率(X)与甲醇的选择性(S)与温度的关系(甲醛的选择性:转化的CH
3OH中生成HCHO的百分比)。回答下列问题:
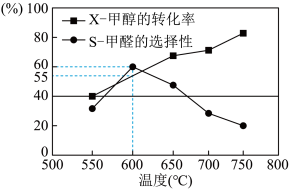
①600℃时,前10min内甲醛的平均速率为
v(HCHO)=
______②从平衡角度分析550℃- 650℃甲醇生成甲醛的转化率随温度升高的原因为
______;
③反应历程i的活化能
______(填“>”“<” 或“=”)CH
3OH(g)
⇌HCHO(g)+H
2(g)活化能。
④650℃- 750℃反应历程ii的速率
_______(填“>”“<” 或“=”)反应历程iii的速率。
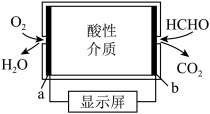
Ⅱ.甲醛超标会危害人体健康,需对甲醛含量检测及处理。
某甲醛气体探测仪利用燃料电池工作原理,b电极反应方程式为
________。