23. 乙酸制氢过程有如下反应:
反应Ⅰ:CH
3COOH(g)

2CO(g)+2H
2(g)
△H
1反应Ⅱ:CH
3COOH(g)

CH
4(g)+CO
2(g)
△H
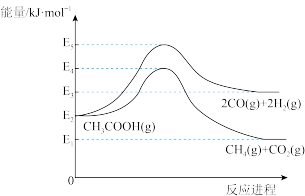
2(1)由如图可知,
△H
1=
_______kJ/mol(用有关E的代数式表示)。
(2)在容积相同的密闭容器中,加入等量乙酸蒸气制氢,在相何时间测得温度与气体产率的关系如图。
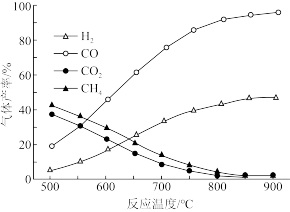
①650℃之前,氢气产率低于甲烷的原因是
_______。
②分析图象发现,该容器内还发生了其他的副反应,分析理由是
_______。
③若保持其他条件不变,在乙酸蒸气中掺杂一定量水,氢气的产率显著提高而CO的产率下降,请用化学方程式表示可能发生的反应
_______。
(3)按照符合“绿色化学”要求(原子利用率100%),可采用光催化反应技术直接合成乙酸,下列原料组合符合要求的是_______(填标号)
| A.CO2+H2 | B.CO+H2 | C.H2O+CH4 | D.CO2+CH4 |
(4)用甲醇与CO反应来制备乙酸。反应如下:CH
3OH(g)+CO(g) =CH
3COOH(1) 。在恒压密闭容器中通入0.20 mol的CH
3OH和0.22mol的CO气体,回答如下问题:
①恒温恒压下,不能说明上述反应达到平衡状态的是
_______(填编号)。
A.容器内混合气体的密度保持不变
B.容器内压强保持不变
C.CH
3OH的浓度保持不变
D.CO的体积分数保持不变
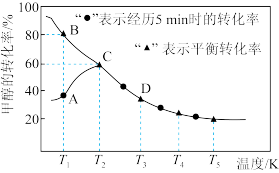
②测得甲醇的转化率随温度变化如图所示。温度为T
1时,该反应的正反应速率:v(B)
正_______v(A)
正(填“>”,“=”或“<”)。温度为T
1时,在恒压容器中,上述反应已达到平衡,再通入0.10molCH
3OH和0.11molCO的混合气体,再次达到平衡,甲醇的转化率
_______80%(“>”,“=”或“<”)。