26. Ⅰ.测定化学反应速率
某同学利用如图装置测定化学反应速率。

(已知:S
2O
32-+2H
+=H
2O+S↓+SO
2↑)
(1)为保证实验准确性、可靠性,利用该装置进行实验前应先进行的步骤是
__;除如图所示的实验用品、仪器外,还需要的一件实验仪器是
__。
(2)若在2min时收集到224mL(已折算成标准状况)气体,可计算出该2min内H
+的反应速率,而该测定值比实际值偏小,其原因是
___。
Ⅱ.为探讨化学反应速率的影响因素
某小组利用H
2C
2O
4溶液和酸性KMnO
4溶液反应来探究“外界条件对化学反应速率的影响”。已知:5H
2C
2O
4+2KMnO
4+3H
2SO
4=K
2SO
4+2MnSO
4+10CO
2↑+8H
2O
实验时,通过测定褪色所需时间来判断反应的快慢。限选试剂与仪器:0.20mol/LH
2C
2O
4溶液,0.010mol/L酸性KMnO
4溶液,蒸馏水,锥形瓶,恒温水浴槽,量筒,秒表。该小组设计了如下的方案。
| 物理量 | 水 | H2C2O4溶液 | 酸性KMnO4溶液 | 温度/℃ |
| 体积/mL | 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | |
| ① | 0 | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
| ② | 0 | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | | | 1.0 | 0.010 | 4.0 | 25 |
(1)已知反应后H
2C
2O
4转化为CO
2逸出,KMnO
4转化为MnSO
4。为了观察到紫色褪去,H
2C
2O
4与KMnO
4初始的物质的量需要满足的关系为:n(H
2C
2O
4):n(KMnO
4)≥
__。
(2)实验③测得KMnO
4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO
4)=
__mol·L
-1·min
-1。
(3)请完成表格内二处空白
__、
__。
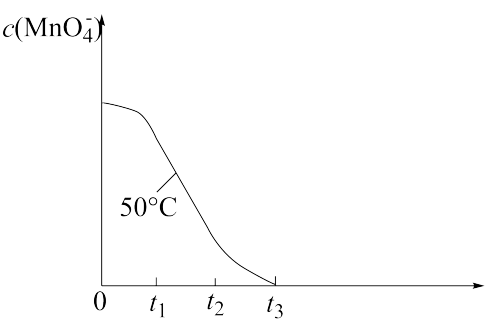
(4)已知50℃时c(MnO
4-)~反应时间t的变化曲线如图。其中反应速率最快的阶段是
__,原因是
___。