四川省泸县第一中学2019-2020学年高二下学期期中考试化学试题
四川
高二
期中
2020-05-27
235次
整体难度:
适中
考查范围:
有机化学基础、物质结构与性质、化学反应原理、化学实验基础
四川省泸县第一中学2019-2020学年高二下学期期中考试化学试题
四川
高二
期中
2020-05-27
235次
整体难度:
适中
考查范围:
有机化学基础、物质结构与性质、化学反应原理、化学实验基础
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
1. 下列说法正确的是
| A.聚乙烯、蛋白质、淀粉和油脂都是有机高分子化合物 |
| B.能与NaHCO3溶液反应的有机物C5H10O2有4种 |
| C.利用乙醇的可燃性可检查司机是否酒后驾车 |
| D.石蜡油分解的产物均能使溴的四氯化碳溶液褪色 |
您最近一年使用:0次
2018-03-06更新
|
410次组卷
|
2卷引用:山东省菏泽市2018届高三上学期期末考试化学试题
单选题
|
较易(0.85)
名校
2. 下列说法不正确的是
| A.乙醇的酯化反应和酯的水解反应均属于取代反应 |
| B.乙烯能使酸性高锰酸钾溶液褪色,是因为乙烯分子中含有碳碳双键 |
| C.乙醛分子式为C2H4O2它可以还原生成乙醇 |
| D.苯与溴水混合,反复振荡后溴水层颜色变浅是因为苯与溴水发生了加成反应 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
3. W、X、Y、Z均为短周期主族元素,原子序数依次增大,W是周期表中原子半径最小的原子,X与Y形成的某种化合物能与水发生氧化还原反应,且生成酸,W、X、Y三种元素的核电荷数之和等于Z的原子序数,则下列说法正确的是
| A.原子半径:X>Y>Z>W |
| B.W和X形成的某种化合物中,可能既有离子键,又有共价键 |
| C.单质的氧化性:Y<Z |
| D.简单氢化物的稳定性:X<Y<Z |
您最近一年使用:0次
2020-01-09更新
|
102次组卷
|
2卷引用:河北省张家口市2020届高三10月阶段检测化学试题
单选题
|
适中(0.65)
名校
4. 已知:H2(g)+Cl2(g) =2HCl(g)反应的能量变化示意图如下:
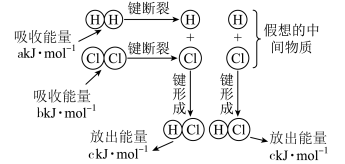
下列说法正确的是

下列说法正确的是
| A.点燃条件和光照条件下,反应的ΔH不同 |
| B.反应的ΔH约为[2c- (a+b)]kJ·mol-1 |
| C.“假想的中间物质”的总能量低于起始态H2和Cl2的总能量 |
| D.反应涉及的物质中,既有含极性键的物质,也有含非极性键的物质 |
您最近一年使用:0次
2018-01-20更新
|
617次组卷
|
6卷引用:北京市海淀区2018届高三上学期期末考试化学试题
单选题
|
适中(0.65)
名校
5. 已知:原子序数小于18的同一主族的两种元素X和Y,其原子半径:X<Y。下列说法正确的是
| A.若X和Y均位于VIIA,则键能大小为HX<HY |
| B.若X和Y均位于VIA,则H2X分子间易形成氢键 |
| C.若X和Y均位于IVA,则半径Y<X |
| D.若X和Y均位于IIA,则第一电离能大小为X<Y |
您最近一年使用:0次
2019-05-06更新
|
91次组卷
|
2卷引用:吉林省辽源市田家炳高级中学2018-2019学年高二下学期期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
6. 如图是某空间站能量转化系统的局部示意图,其中燃料电池采用KOH溶液为电解液,下列有关说法中不正确的是
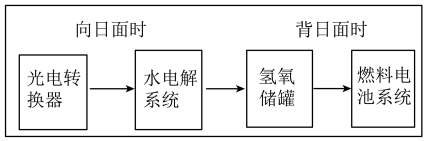

| A.该能量转化系统中的水也是可能循环的 |
| B.燃料电池系统产生的能量实际上来自于水 |
C.水电解系统中的阳极有 放出 放出 |
D.燃料电池放电时的负极反应: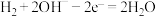 |
【知识点】 燃料电池 新型电池解读 原电池、电解池综合考查解读
您最近一年使用:0次
2020-02-14更新
|
95次组卷
|
2卷引用:2020届高三化学选修4二轮专题练——原电池电极方程式书写及相关计算【夯实基础】【精编25题】
单选题
|
适中(0.65)
名校
解题方法
7. 用NaOH溶液吸收烟气中的SO2,将所得的吸收液用三室膜电解技术处理,原理如图所示.下列说法错误的是


| A.电极a为电解池阴极 |
B.阳极上有反应HSO -2e—+H2O=SO -2e—+H2O=SO +3H+发生 +3H+发生 |
| C.当电路中通过1mol电子的电量时,理论上将产生0.5mol H2 |
| D.处理后可得到较浓的H2SO4和NaHSO3产品 |
您最近一年使用:0次
2020-01-29更新
|
459次组卷
|
4卷引用:福建省泉州市2020届普通高中毕业班单科质量检查化学试题
二、解答题 添加题型下试题
8. 雾霾天气肆虐给人类健康带来了严重影响.燃煤和汽车尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO 2CO2(g)+N2(g)△H<0
2CO2(g)+N2(g)△H<0
①反应的速率-时间图像如图甲所示.若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图像如图乙所示。以下说法正确的是___________ (填对应字母)。

A.a1>a2B.b1<b2C.t1>t2D.图乙中阴影部分面积更大E.图甲中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是_________ (填代号)

(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
已知:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
2NO2(g) N2O4(g)△H=﹣56.9kJ/mol
N2O4(g)△H=﹣56.9kJ/mol
H2O(g)=H2O(l)△H=﹣44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:______________ 。
(3)CH4和H2O(g)在催化剂表面发生反应CH4+H2O⇌CO+3H2,该反应在不同温度下的化学平衡常数如表:
①该反应是_________ 反应(填“吸热”或“放热”)。
②T℃时,向1L密闭容器中投入lmolCH4和lmolH2O(g),平衡时c(CH4)=0.5mol/L,该温度下反应CH4+H2O CO+3H2的平衡常数K=
CO+3H2的平衡常数K=______________ 。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO
 2CO2(g)+N2(g)△H<0
2CO2(g)+N2(g)△H<0①反应的速率-时间图像如图甲所示.若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图像如图乙所示。以下说法正确的是

A.a1>a2B.b1<b2C.t1>t2D.图乙中阴影部分面积更大E.图甲中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是

(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
已知:CH4(g)+2NO2(g)
 N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol
N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ/mol2NO2(g)
 N2O4(g)△H=﹣56.9kJ/mol
N2O4(g)△H=﹣56.9kJ/molH2O(g)=H2O(l)△H=﹣44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:
(3)CH4和H2O(g)在催化剂表面发生反应CH4+H2O⇌CO+3H2,该反应在不同温度下的化学平衡常数如表:
| 温度/℃ | 800 | 1000 | 1200 | 1400 |
| 平衡常数 | 0.45 | 1.92 | 276.5 | 1771.5 |
①该反应是
②T℃时,向1L密闭容器中投入lmolCH4和lmolH2O(g),平衡时c(CH4)=0.5mol/L,该温度下反应CH4+H2O
 CO+3H2的平衡常数K=
CO+3H2的平衡常数K=
您最近一年使用:0次
三、填空题 添加题型下试题
9. 恒温时,将2molA和2molB气体投入固定容积为2L密闭容器中发生反应:2A(g)+B(g) xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
(1)x=____________
(2)从反应开始到10s,B的平均反应速率为____________
(3)从反应开始到40s达平衡状态,A的平均反应速率为____________
(4)平衡时容器中B的体积分数为____________
(5)下列各项能表示该反应达到平衡状态是____________
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量n(A)∶n(B)=2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体密度不再变化
 xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:
xC(g)+D(s),10s时,测得A的物质的量为1.7mol,C的反应速率为0.0225mol·L—1·s—1;40s时反应恰好处于平衡状态,此时B的转化率为20%。请填写下列空白:(1)x=
(2)从反应开始到10s,B的平均反应速率为
(3)从反应开始到40s达平衡状态,A的平均反应速率为
(4)平衡时容器中B的体积分数为
(5)下列各项能表示该反应达到平衡状态是
A.消耗A的物质的量与生成D的物质的量之比为2∶1
B.容器中A、B的物质的量n(A)∶n(B)=2∶1
C.气体的平均相对分子质量不再变化
D.压强不再变化
E.气体密度不再变化
【知识点】 化学反应速率计算解读 化学平衡的有关计算 化学平衡状态的判断方法解读
您最近一年使用:0次
四、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
名校
10. CoCl2·6H2O是一种饲料营养强化剂。以含钴废料(含少量Fe、Al等杂质)制取CoCl2·6H2O的一种新工艺流程如下图:

已知:①CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,易失去结晶水变成有毒的无水氯化钴。(乙醚:无色液体,沸点34.5℃,在水中的溶解度小)
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)钴的性质与铁相似,能与盐酸和硝酸反应,写出钴与盐酸反应的化学方程式:________________________________ 。
(2)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点:
①为__________________________ ,防止大气污染;
②防止产品中混有硝酸盐。
(3) 加入碳酸钠调节pH至a,a的范围应是5.2~_________ 。
(4) 操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和_________ 。
(5)根据表中数据,判断Ksp[Fe(OH)3]________ Ksp[Co(OH)2] (填“<”、“=”或“>”) 。在实验室中,为了从上述产品中获得纯净的CoCl2·6H2O,采用的方法是:将产品溶于乙醚过滤后,再蒸馏。

已知:①CoCl2·6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,易失去结晶水变成有毒的无水氯化钴。(乙醚:无色液体,沸点34.5℃,在水中的溶解度小)
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
请回答下列问题:
(1)钴的性质与铁相似,能与盐酸和硝酸反应,写出钴与盐酸反应的化学方程式:
(2)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点:
①为
②防止产品中混有硝酸盐。
(3) 加入碳酸钠调节pH至a,a的范围应是5.2~
(4) 操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和
(5)根据表中数据,判断Ksp[Fe(OH)3]
您最近一年使用:0次
2018-03-10更新
|
214次组卷
|
2卷引用:福建省莆田第一中学2017-2018学年高二上学期期末考试化学试题
五、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
11. 请回答下列问题:
(1)(NH4)2SO4中含有化学键的类型为_________________________ 。
(2)KNO3中NO3-的立体构型为____________________ ,其中N原子的杂化方式为________ ,写出与NO 互为等电子体的另一种阴离子的化学式:
互为等电子体的另一种阴离子的化学式:_______________ 。
(3)已知配合物CrCl3·6H2O中心原子Cr3+的配位数为6,向含0.1 mol CrCl3·6H2O的溶液中滴加2 mol·L-1 AgNO3溶液,反应完全后共消耗AgNO3溶液50 mL,则该配合物的化学式为________________ ,Cr在基态时,价电子排布式为_____________________ 。
(4)LiBH4由Li+和BH4-构成,BH4-的立体构型是____________ ,根据化合物LiBH4判断,Li、B、H的电负性由大到小的顺序为____________ 。
(5)丙酮( )分子中C原子轨道杂化类型为
)分子中C原子轨道杂化类型为_____________ ;含有的π键与σ键数目之比为___________ 。
(6)第一电离能I 1(Zn)______ I 1(Cu)(填“大于”或“小于”),原因是_______________ 。
(1)(NH4)2SO4中含有化学键的类型为
(2)KNO3中NO3-的立体构型为
 互为等电子体的另一种阴离子的化学式:
互为等电子体的另一种阴离子的化学式:(3)已知配合物CrCl3·6H2O中心原子Cr3+的配位数为6,向含0.1 mol CrCl3·6H2O的溶液中滴加2 mol·L-1 AgNO3溶液,反应完全后共消耗AgNO3溶液50 mL,则该配合物的化学式为
(4)LiBH4由Li+和BH4-构成,BH4-的立体构型是
(5)丙酮(
 )分子中C原子轨道杂化类型为
)分子中C原子轨道杂化类型为(6)第一电离能I 1(Zn)
您最近一年使用:0次
2019-05-27更新
|
624次组卷
|
2卷引用:福建省永春县第一中学2018-2019学年高二下学期期中考试化学试题
六、解答题 添加题型下试题
解答题-有机推断题
|
适中(0.65)
名校
解题方法
12. 可由N物质通过以下路线合成天然橡胶和香料柑青酸甲酯衍生物F。

已知:①RCHO+R′CH2CH CH2
CH2

② +
+


(1)用系统命名法对N命名________ 。
(2)①试剂a的名称是________ 。②C→D中反应i的反应类型是________ 。
(3)E的结构简式是________ 。
(4)关于试剂b的下列说法不正确的是________ (填字母序号)。
a.存在顺反异构体 b.难溶于水 c.能发生取代、加成和氧化反应 d.不能与NaOH溶液发生反应
(5)写出A生成B的反应方程式_______________ 。
(6)分子中含有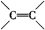 和
和 结构的D的所有同分异构共有
结构的D的所有同分异构共有______ 种(含顺反异构体),写出其中任意一种含反式结构的结构简式________ 。

已知:①RCHO+R′CH2CH
 CH2
CH2

②
 +
+


(1)用系统命名法对N命名
(2)①试剂a的名称是
(3)E的结构简式是
(4)关于试剂b的下列说法不正确的是
a.存在顺反异构体 b.难溶于水 c.能发生取代、加成和氧化反应 d.不能与NaOH溶液发生反应
(5)写出A生成B的反应方程式
(6)分子中含有
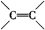 和
和 结构的D的所有同分异构共有
结构的D的所有同分异构共有
您最近一年使用:0次
2016-12-09更新
|
220次组卷
|
5卷引用:2016届重庆市一中高三下学期模拟考试理综化学试卷
2016届重庆市一中高三下学期模拟考试理综化学试卷2016届重庆市一中高三5月模拟考试理综化学试卷(已下线)解密22 有机化学基础(教师版)——备战2018年高考化学之高频考点解密(已下线)2019年6月2日 《每日一题》选修5-每周一测四川省泸县第一中学2019-2020学年高二下学期期中考试化学试题
试卷分析
整体难度:适中
考查范围:有机化学基础、物质结构与性质、化学反应原理、化学实验基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
3
填空题
2
试卷难度
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 脂肪烃的来源 乙醇与强氧化剂的反应 醇与强氧化剂的氧化反应 高分子化合物的分类和表示方法 | |
| 2 | 0.85 | 乙烯的氧化反应 苯的取代反应 乙醛与强氧化剂的反应 酯的水解反应机理 | |
| 3 | 0.65 | 元素非金属性强弱的比较方法 微粒半径大小的比较方法 根据原子结构进行元素种类推断 共价键与离子键的比较 | |
| 4 | 0.65 | 化学反应热的计算 能量的相互转化 吸热反应和放热反应 焓变产生原因及表示 | |
| 5 | 0.65 | 同主族元素性质递变规律理解及应用 电离能变化规律 键能、键长、键角及应用 | |
| 6 | 0.65 | 燃料电池 新型电池 原电池、电解池综合考查 | |
| 7 | 0.65 | 电解原理的应用 电解原理的理解及判断 电解池电极反应式及化学方程式的书写与判断 | |
| 二、解答题 | |||
| 8 | 0.65 | 盖斯定律与热化学方程式 化学反应速率的图像 化学平衡的移动及其影响因素 化学平衡常数的有关计算 | 原理综合题 |
| 10 | 0.65 | 沉淀溶解平衡的应用 物质分离、提纯综合应用 中和滴定 物质制备的探究 | 工业流程题 |
| 12 | 0.65 | 烯烃系统命名法 有机物的推断 多官能团有机物的结构与性质 信息给予的有机合成 | 有机推断题 |
| 三、填空题 | |||
| 9 | 0.85 | 化学反应速率计算 化学平衡的有关计算 化学平衡状态的判断方法 | |
| 11 | 0.65 | 物质结构与性质综合考查 利用杂化轨道理论判断化学键杂化类型 配合物的结构与性质 简单配合物的成键 | |



