CO2的捕获和利用技术对减缓日益严重的环境问题有重要意义。利用CO2加氢制CH3OH的过程中,主要发生的化学反应如下:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  =+49.5kJ
=+49.5kJ
②CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)  =-40.9kJ
=-40.9kJ
完成下列填空:
(1)反应②达到平衡后,其他条件不变,升高温度,v正__ v逆(选填“>”或“<”)。
(2)在1L密闭容器中通入1molCO2和3molH2,发生上述反应,CO2的平衡转化率随温度和压强的变化如图所示。比较压强大小:p1_ p2(选填“>”或“<”)。
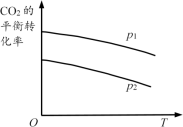
某温度下达到平衡时,容器中的n(CH3OH)=0.3mol、n(CO)=0.3mol。达到平衡所需时间tmin,则0~tmin内CH3OH平均反应速率v(CH3OH)=__ ;反应②的平衡常数K的数值为__ 。
工业废气中的CO2可用氨水捕获,生成NH4HCO3溶液。
(3)常温下,0.1mol·L-1的NH4HCO3溶液的pH≈8,请解释原因__ 。
(4)常温下,将等体积、等物质的量浓度的NH4HCO3溶液与NaCl溶液充分混合后静置,发现有沉淀析出,则沉淀的化学式为__ ;比较上层清液中的离子浓度关系:c(H+)+c(NH )
)___ c(OH-)+c(HCO )+2c(CO
)+2c(CO )(选填“>”“<”或“=”)。
)(选填“>”“<”或“=”)。
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  =+49.5kJ
=+49.5kJ②CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)  =-40.9kJ
=-40.9kJ完成下列填空:
(1)反应②达到平衡后,其他条件不变,升高温度,v正
(2)在1L密闭容器中通入1molCO2和3molH2,发生上述反应,CO2的平衡转化率随温度和压强的变化如图所示。比较压强大小:p1

某温度下达到平衡时,容器中的n(CH3OH)=0.3mol、n(CO)=0.3mol。达到平衡所需时间tmin,则0~tmin内CH3OH平均反应速率v(CH3OH)=
工业废气中的CO2可用氨水捕获,生成NH4HCO3溶液。
(3)常温下,0.1mol·L-1的NH4HCO3溶液的pH≈8,请解释原因
(4)常温下,将等体积、等物质的量浓度的NH4HCO3溶液与NaCl溶液充分混合后静置,发现有沉淀析出,则沉淀的化学式为
 )
) )+2c(CO
)+2c(CO )(选填“>”“<”或“=”)。
)(选填“>”“<”或“=”)。
2022·上海金山·一模 查看更多[1]
更新时间:2021-12-27 21:50:39
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】碳中和作为一种新型环保形式,目前已经被越来越多的大型活动和会议采用。回答下列有关问题:
(1)利用 合成二甲醚有两种工艺。
合成二甲醚有两种工艺。
工艺1:涉及以下主要反应:
Ⅰ.甲醇的合成:
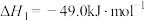
Ⅱ.逆水汽变换:
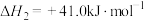
Ⅲ.甲醇脱水:

工艺2:利用 直接加氢合成
直接加氢合成 (反应Ⅳ)
(反应Ⅳ)
①据上述信息可知反应Ⅳ的热化学方程式为___________ ,反应Ⅰ低温___________ 自发进行(填“能”、“不能”)。
②恒温恒容情况下,下列说法能判断反应Ⅳ达到平衡的是___________ 。
A.气体物质中碳元素与氧元素的质量比不变
B.容器内 浓度保持不变
浓度保持不变
C.容器内气体密度不变
D.容器内气体的平均摩尔质量不变
(2)工艺1需先合成甲醇。在不同压强下,按照 投料合成甲醇,实验测定
投料合成甲醇,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图甲、乙所示。
的平衡产率随温度的变化关系如下图甲、乙所示。
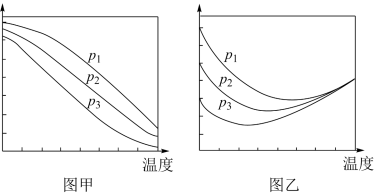
①下列说法正确的是___________ 。
A.图甲纵坐标表示 的平衡产率
的平衡产率
B.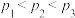
C.为了同时提高 的平衡转化率和
的平衡转化率和 的平衡产率,应选择低温、高压条件
的平衡产率,应选择低温、高压条件
D.一定温度压强下,提高 的平衡转化率的主要方向是寻找活性更高的催化剂
的平衡转化率的主要方向是寻找活性更高的催化剂
②图乙中,某温度时,三条曲线几乎交于一点的原因是___________ 。
(3)对于合成甲醇的反应:
 ,一定条件下,单位时间内不同温度下测定的
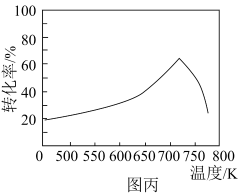
,一定条件下,单位时间内不同温度下测定的 转化率如图丙所示。温度高于
转化率如图丙所示。温度高于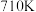 时,随温度的升高
时,随温度的升高 转化率降低的原因可能是
转化率降低的原因可能是___________ 。
(4) 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图丁所示,两电极均为惰性电极。
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图丁所示,两电极均为惰性电极。
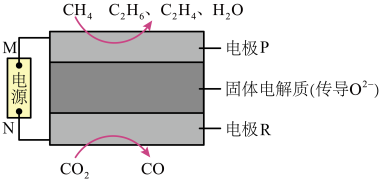
图丁
①电极M为电源的___________ 极;
②电极R上发生的电极反应为___________ 。
(1)利用
 合成二甲醚有两种工艺。
合成二甲醚有两种工艺。工艺1:涉及以下主要反应:
Ⅰ.甲醇的合成:

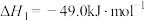
Ⅱ.逆水汽变换:

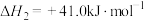
Ⅲ.甲醇脱水:


工艺2:利用
 直接加氢合成
直接加氢合成 (反应Ⅳ)
(反应Ⅳ)①据上述信息可知反应Ⅳ的热化学方程式为
②恒温恒容情况下,下列说法能判断反应Ⅳ达到平衡的是
A.气体物质中碳元素与氧元素的质量比不变
B.容器内
 浓度保持不变
浓度保持不变C.容器内气体密度不变
D.容器内气体的平均摩尔质量不变
(2)工艺1需先合成甲醇。在不同压强下,按照
 投料合成甲醇,实验测定
投料合成甲醇,实验测定 的平衡转化率和
的平衡转化率和 的平衡产率随温度的变化关系如下图甲、乙所示。
的平衡产率随温度的变化关系如下图甲、乙所示。
①下列说法正确的是
A.图甲纵坐标表示
 的平衡产率
的平衡产率B.
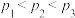
C.为了同时提高
 的平衡转化率和
的平衡转化率和 的平衡产率,应选择低温、高压条件
的平衡产率,应选择低温、高压条件D.一定温度压强下,提高
 的平衡转化率的主要方向是寻找活性更高的催化剂
的平衡转化率的主要方向是寻找活性更高的催化剂②图乙中,某温度时,三条曲线几乎交于一点的原因是
(3)对于合成甲醇的反应:

 ,一定条件下,单位时间内不同温度下测定的
,一定条件下,单位时间内不同温度下测定的 转化率如图丙所示。温度高于
转化率如图丙所示。温度高于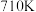 时,随温度的升高
时,随温度的升高 转化率降低的原因可能是
转化率降低的原因可能是
(4)
 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图丁所示,两电极均为惰性电极。
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图丁所示,两电极均为惰性电极。
图丁
①电极M为电源的
②电极R上发生的电极反应为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】CO2 的资源化利用是“减少碳排放”背景下的科学研究热点。
I.利用 CO2 甲烷化反应:CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g)进行热力学转化。
(1)已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-802kJ/mol
写出 CO2甲烷化反应的热化学方程式___________ 。
(2)CO2 甲烷化反应的平衡常数的表达式:K=___________ 。温度升高,K___________ (填“增大”或“减小”)。
II.CO2 催化加氢合成二甲醚。其过程中主要发生下列反应:
反应i:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41.2kJ·mol−1
反应ii:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ·mol−1
在恒压、CO2 和 H2 的起始量一定的条件下,CO2 平衡转化率和平衡时 CH3OCH3 的选择性随温度的变化如下图所示。

(3)①温度升高,平衡时CH3OCH3的选择性下降的原因是___________ 。
②温度高于300℃时,CO2平衡转化率随温度升高而上升的原因是___________ 。
III.电化学转化
多晶 Cu 可高效催化 CO2 甲烷化,电解 CO2 制备CH4 的原理示意图如下。电解过程中温度控制在 10℃左右,持续通入 CO2.阴、阳极室的 KHCO3 溶液的浓度基本保持不变。
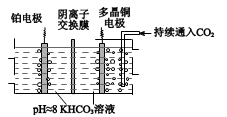
(4)多晶Cu作___________ (填“阴”或“阳”)极。
(5)阳极上发生的电极反应式是___________ 。
(6)阴离子交换膜中传导的离子是___________ ,移动方向是(填“从左向右”或者“从右向左”)___________ 。
I.利用 CO2 甲烷化反应:CO2(g)+4H2(g) ⇌CH4(g)+2H2O(g)进行热力学转化。
(1)已知:2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-802kJ/mol
写出 CO2甲烷化反应的热化学方程式
(2)CO2 甲烷化反应的平衡常数的表达式:K=
II.CO2 催化加氢合成二甲醚。其过程中主要发生下列反应:
反应i:CO2(g)+H2(g)=CO(g)+H2O(g) ΔH=+41.2kJ·mol−1
反应ii:2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(g) ΔH=-122.5kJ·mol−1
在恒压、CO2 和 H2 的起始量一定的条件下,CO2 平衡转化率和平衡时 CH3OCH3 的选择性随温度的变化如下图所示。

(3)①温度升高,平衡时CH3OCH3的选择性下降的原因是
②温度高于300℃时,CO2平衡转化率随温度升高而上升的原因是
III.电化学转化
多晶 Cu 可高效催化 CO2 甲烷化,电解 CO2 制备CH4 的原理示意图如下。电解过程中温度控制在 10℃左右,持续通入 CO2.阴、阳极室的 KHCO3 溶液的浓度基本保持不变。

(4)多晶Cu作
(5)阳极上发生的电极反应式是
(6)阴离子交换膜中传导的离子是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】已知化学反应①:Fe(s)+CO2(g)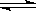 FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)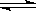 FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1173 K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1173 K情况下,K1、K2的值分别如下:
请填空:
(1)通过表格中的数值可以推断:反应①是________ (填“吸热”或“放热”)反应.
(2)现有反应③:CO2(g)+H2(g)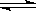 CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=_____________ .
(3)在相同温度下,根据反应①与②可推导出K1、K2与K3之间的关系式________ ,据此关系式及上表数据,也能推断出反应③是________ (填“吸热”或“放热”)反应.
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有________ (填写字母序号,下同).
A.增大压强 B.体积不变时充入稀有气体 C.升高温度
D.使用合适的催化剂 E.在体系中投入少量P2O5固体
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:①图甲中t2时刻发生改变的条件可能是________________ .
②图乙中t2时刻发生改变的条件可能是___________________ .
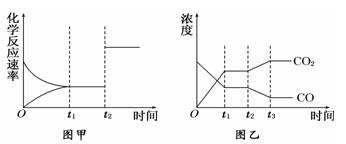
A.升高温度 B.降低温度 C.加入催化剂 D.增大压强
E.减小压强 F.充入CO2G.分离出部分CO
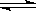 FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)
FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)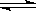 FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1173 K情况下,K1、K2的值分别如下:
FeO(s)+H2(g),其平衡常数为K2,在温度973 K和1173 K情况下,K1、K2的值分别如下:| 温度 | K1 | K2 |
| 973 K | 1.47 | 2.38 |
| 1173 K | 2.15 | 1.67 |
请填空:
(1)通过表格中的数值可以推断:反应①是
(2)现有反应③:CO2(g)+H2(g)
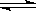 CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=
CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学表达式:K3=(3)在相同温度下,根据反应①与②可推导出K1、K2与K3之间的关系式
(4)要使反应③在一定条件下建立的平衡向正反应方向移动,可采取的措施有
A.增大压强 B.体积不变时充入稀有气体 C.升高温度
D.使用合适的催化剂 E.在体系中投入少量P2O5固体
(5)图甲、乙分别表示反应③在t1时刻达到平衡,在t2时刻因改变某个条件而发生变化的情况:①图甲中t2时刻发生改变的条件可能是
②图乙中t2时刻发生改变的条件可能是

A.升高温度 B.降低温度 C.加入催化剂 D.增大压强
E.减小压强 F.充入CO2G.分离出部分CO
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】甲醇是重要的化工原料,也可作燃料。工业上可用CO2和H2在一定条件下合成甲醇。回答下列问题。
(1)已知:CO 和 H2 的燃烧热分别为 283.0 kJ·mol-1、285.8kJ·mol-1 ,水的汽化热为 44.0kJ·mol-1, 反应① CO+H2O=CO2+H2 是生成合成甲醇的原料气(CO2、H2)的重要反应,其热化学方程式为: CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =_____ kJ·mol-1。
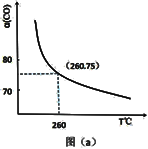
(2)某同学设计实验对反应①进行研究。将 1mol H2O(g)和 1mol CO 充入一个恒容密闭容器中,在催化剂和一定温度下达到化学平衡。如图是 CO 的平衡转化率(%)随温度变化的曲线,260℃时反应①的平衡常数 K=_______ 。
(3)CO2和 H2在催化剂、一定温度下合成甲醇。图为在容积为 1L 的恒容密闭容器中,加入 3 molH2和 1molCO2时经过相同时间甲醇产率与反应温度的关系曲线:
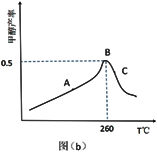
曲线上 A 点_____ (填“是”或“不是”)对应温度下的平衡产率,理由是_____ ,C 点甲醇的产率低于 B 点的原因可能是_____ (填标号)。
A.反应活化能增大 B.催化剂活性低 C.副反应多 D.平衡常数变大 E.平衡逆向移动
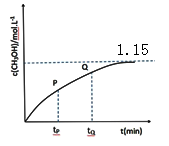
(4)CO和 H2在一定条件下也可以合成甲醇。在容积为1L的恒容密闭容器中,加入 a molH2和2.0molCO,在催化剂和 260℃温度条件下发生反应:CO+2H2=CH3OH。图为甲醇的浓度与反应时间的关系曲线,tP 时的 v 逆_____ tQ 时的 v 逆(填大于、小于或等于),判断的依据是_____ ,达平衡时氢气的浓度为 1.0mol/L,则起始时加入的氢气的物质的量为_____ mol。
(1)已知:CO 和 H2 的燃烧热分别为 283.0 kJ·mol-1、285.8kJ·mol-1 ,水的汽化热为 44.0kJ·mol-1, 反应① CO+H2O=CO2+H2 是生成合成甲醇的原料气(CO2、H2)的重要反应,其热化学方程式为: CO(g)+H2O(g)=CO2(g)+H2(g) ΔH =
(2)某同学设计实验对反应①进行研究。将 1mol H2O(g)和 1mol CO 充入一个恒容密闭容器中,在催化剂和一定温度下达到化学平衡。如图是 CO 的平衡转化率(%)随温度变化的曲线,260℃时反应①的平衡常数 K=

(3)CO2和 H2在催化剂、一定温度下合成甲醇。图为在容积为 1L 的恒容密闭容器中,加入 3 molH2和 1molCO2时经过相同时间甲醇产率与反应温度的关系曲线:

曲线上 A 点
A.反应活化能增大 B.催化剂活性低 C.副反应多 D.平衡常数变大 E.平衡逆向移动
(4)CO和 H2在一定条件下也可以合成甲醇。在容积为1L的恒容密闭容器中,加入 a molH2和2.0molCO,在催化剂和 260℃温度条件下发生反应:CO+2H2=CH3OH。图为甲醇的浓度与反应时间的关系曲线,tP 时的 v 逆

您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】锰酸锂( )是一种锂电池的正极材料。工业上以方锰矿(主要成分为MnO,还含有少量的
)是一种锂电池的正极材料。工业上以方锰矿(主要成分为MnO,还含有少量的 、
、 、CaO、
、CaO、 )为原料制备锰酸锂的流程如下:
)为原料制备锰酸锂的流程如下:
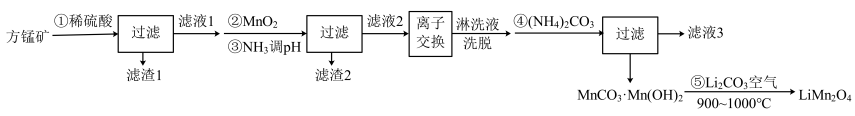
已知:I.25℃时,相关物质的Ksp如下表:
Ⅱ.25℃时, 电离常数
电离常数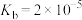
Ⅲ.离子浓度低于 时即为沉淀完全
时即为沉淀完全
(1)写出步骤①溶于稀硫酸时杂质 反应的离子方程式
反应的离子方程式___________ 。
(2)滤渣1的成分为 、
、___________ 。
(3)步骤②加入 的作用是
的作用是___________ 。
(4)步骤③加入 目的是除去杂质离子,若溶液中
目的是除去杂质离子,若溶液中 浓度为
浓度为 ,要确保杂质离子沉淀完全,同时不降低产品产率,步骤③调控pH的范围应该为
,要确保杂质离子沉淀完全,同时不降低产品产率,步骤③调控pH的范围应该为___________ 。反应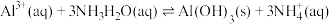 的平衡常数
的平衡常数
___________ 。
(5)已知步骤④中得到产物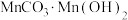 的产率与溶液pH的关系如图所示。若反应时溶液pH过大,所得产物
的产率与溶液pH的关系如图所示。若反应时溶液pH过大,所得产物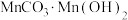 的产率偏低,但产品中Mn元素的质量分数偏大,原因是
的产率偏低,但产品中Mn元素的质量分数偏大,原因是___________ 。

(6)步骤⑤反应的化学方程式为___________ 。
 )是一种锂电池的正极材料。工业上以方锰矿(主要成分为MnO,还含有少量的
)是一种锂电池的正极材料。工业上以方锰矿(主要成分为MnO,还含有少量的 、
、 、CaO、
、CaO、 )为原料制备锰酸锂的流程如下:
)为原料制备锰酸锂的流程如下:
已知:I.25℃时,相关物质的Ksp如下表:
| 物质 |  |  |  |  |  |
| Ksp | 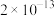 | 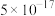 | 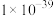 | 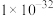 | 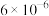 |
 电离常数
电离常数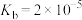
Ⅲ.离子浓度低于
 时即为沉淀完全
时即为沉淀完全(1)写出步骤①溶于稀硫酸时杂质
 反应的离子方程式
反应的离子方程式(2)滤渣1的成分为
 、
、(3)步骤②加入
 的作用是
的作用是(4)步骤③加入
 目的是除去杂质离子,若溶液中
目的是除去杂质离子,若溶液中 浓度为
浓度为 ,要确保杂质离子沉淀完全,同时不降低产品产率,步骤③调控pH的范围应该为
,要确保杂质离子沉淀完全,同时不降低产品产率,步骤③调控pH的范围应该为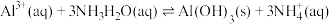 的平衡常数
的平衡常数
(5)已知步骤④中得到产物
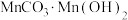 的产率与溶液pH的关系如图所示。若反应时溶液pH过大,所得产物
的产率与溶液pH的关系如图所示。若反应时溶液pH过大,所得产物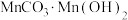 的产率偏低,但产品中Mn元素的质量分数偏大,原因是
的产率偏低,但产品中Mn元素的质量分数偏大,原因是
(6)步骤⑤反应的化学方程式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】如何降低大气中 的含量及有效地开发利用
的含量及有效地开发利用 引起了全世界的普遍重视.目前工业上有一种方法是用
引起了全世界的普遍重视.目前工业上有一种方法是用 来生产燃料甲醇.为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入
来生产燃料甲醇.为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入 和
和 .在500℃下发生发应,
.在500℃下发生发应, .实验测得
.实验测得 和
和 的物质的量(n)随时间变化如下图1所示:
的物质的量(n)随时间变化如下图1所示:
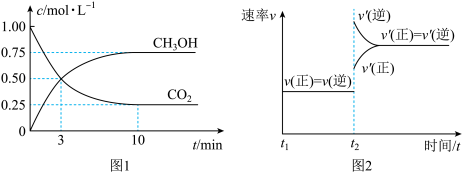
(1)从反应开始到平衡,氢气的平均反应速率
____________ .
(2)500℃该反应的平衡常数为________ (结果保留一位小数),图2是改变温度时化学反应速率随时间变化的示意图,平衡____ 移动(填“正向”或“逆向”或“不”).
(3)下列措施中不能使 的转化率增大的是
的转化率增大的是________ .
①在原容器中再充入 ②将水蒸气从体系中分离出
②将水蒸气从体系中分离出
③使用更有效的催化剂④缩小容器的容积⑤在原容器中再充入
(4)500℃条件下,测得某时刻, 、
、 、
、 和
和 的浓度均为0.4mol/L,则此时
的浓度均为0.4mol/L,则此时
_______  (填“>”“<”或“=”).
(填“>”“<”或“=”).
(5)若反应在500℃进行,在该1L的密闭容器中加入 、
、 和
和 ,达到平衡时
,达到平衡时 的转化率为
的转化率为______________ .
 的含量及有效地开发利用
的含量及有效地开发利用 引起了全世界的普遍重视.目前工业上有一种方法是用
引起了全世界的普遍重视.目前工业上有一种方法是用 来生产燃料甲醇.为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入
来生产燃料甲醇.为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入 和
和 .在500℃下发生发应,
.在500℃下发生发应, .实验测得
.实验测得 和
和 的物质的量(n)随时间变化如下图1所示:
的物质的量(n)随时间变化如下图1所示:
(1)从反应开始到平衡,氢气的平均反应速率

(2)500℃该反应的平衡常数为
(3)下列措施中不能使
 的转化率增大的是
的转化率增大的是①在原容器中再充入
 ②将水蒸气从体系中分离出
②将水蒸气从体系中分离出③使用更有效的催化剂④缩小容器的容积⑤在原容器中再充入

(4)500℃条件下,测得某时刻,
 、
、 、
、 和
和 的浓度均为0.4mol/L,则此时
的浓度均为0.4mol/L,则此时
 (填“>”“<”或“=”).
(填“>”“<”或“=”).(5)若反应在500℃进行,在该1L的密闭容器中加入
 、
、 和
和 ,达到平衡时
,达到平衡时 的转化率为
的转化率为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】CO2可用于制备CH4、合成气(CO、H2),是CO2资源化利用的重要途径。
(1)CO2甲烷化过程可能发生反应:
i.
ii.
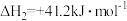
iii.
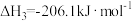
①
___________  。
。
②利用不同催化剂,在一定温度和反应时间条件下,测得产物的生成速率与催化剂的关系如图1.可知有利于制甲烷的催化剂是___________ 。
③压强一定时,按照 投料,发生上述反应,
投料,发生上述反应, 的平衡转化率与温度的关系如图2。
的平衡转化率与温度的关系如图2。
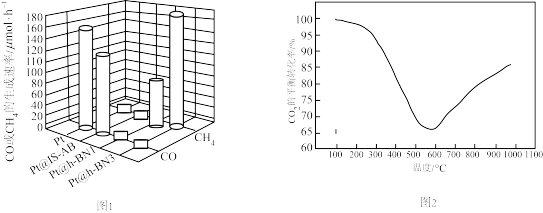
请解释温度高于600℃之后,随着温度升高 转化率增大的原因
转化率增大的原因___________ 。
(2)利用CO、 合成甲醇的反应为
合成甲醇的反应为
 ,向密闭容器中充入1molCO和
,向密闭容器中充入1molCO和 ,发生反应,测得CO的平衡转化率数据与温度、压强的对应关系如下表所示:
,发生反应,测得CO的平衡转化率数据与温度、压强的对应关系如下表所示:
①由此可知,P1_____ P2(填“大于”或“小于”)。有利于提高CO平衡转化率的措施是______ 。
②P2kPa、250℃条件下,反应5min达到平衡,此时H2的物质的量为_____ ,该反应的压强平衡常数Kp=_______ (kPa)2(用分压代替浓度,分压=总压×该组分物质的量分数,用P2的式子表示)。
(1)CO2甲烷化过程可能发生反应:
i.

ii.

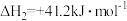
iii.

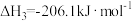
①

 。
。②利用不同催化剂,在一定温度和反应时间条件下,测得产物的生成速率与催化剂的关系如图1.可知有利于制甲烷的催化剂是
③压强一定时,按照
 投料,发生上述反应,
投料,发生上述反应, 的平衡转化率与温度的关系如图2。
的平衡转化率与温度的关系如图2。
请解释温度高于600℃之后,随着温度升高
 转化率增大的原因
转化率增大的原因(2)利用CO、
 合成甲醇的反应为
合成甲醇的反应为
 ,向密闭容器中充入1molCO和
,向密闭容器中充入1molCO和 ,发生反应,测得CO的平衡转化率数据与温度、压强的对应关系如下表所示:
,发生反应,测得CO的平衡转化率数据与温度、压强的对应关系如下表所示:| 温度/℃ 转化率 压强/kPa | 50 | 100 | 150 | 200 | 250 | 300 |
| P1 | 0.82 | 0.70 | 0.34 | 0.12 | 0.04 | 0.02 |
| P2 | 0.90 | 0.86 | 0.76 | 0.48 | 0.20 | 0.10 |
②P2kPa、250℃条件下,反应5min达到平衡,此时H2的物质的量为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】在密闭容器中投入一定量的A和B发生反应:mA(g)+nB(g) pC(g)+qD(g)。
pC(g)+qD(g)。
(1)若开始时加入A物质m mol,欲使A与B的转化率相等,则加入B物质________ mol。
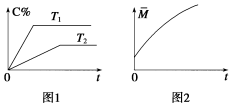
(2)相同的压强下,充入一定量的A、B后,在不同温度下C的百分含量与时间的关系如图1所示。则T1(填“>”、“<”或“=”)______ T2,该反应正反应方向的ΔH(填“>”、“<”或“=”)______ 0。
(3)一定条件下,从正反应开始至达到化学平衡的过程中,混合气体的平均相对分子质量随时间的变化如图2所示,测得达到平衡时A、B、C、D的物质的量均为1 mol。
①若在恒温恒容的条件下,向该平衡体系中再通入A、B、C、D各1 mol,则体系中气体的平均相对分子质量(填“增大”、“减小”、“不变”或“无法确定”)__________ 。
②若恒温恒压的条件下,向原平衡体系中再通入A、B、C、D各1 mol,则体系中气体的密度(填“增大”、“减小”、“不变”或“无法确定”)__________ 。
 pC(g)+qD(g)。
pC(g)+qD(g)。
(1)若开始时加入A物质m mol,欲使A与B的转化率相等,则加入B物质
(2)相同的压强下,充入一定量的A、B后,在不同温度下C的百分含量与时间的关系如图1所示。则T1(填“>”、“<”或“=”)
(3)一定条件下,从正反应开始至达到化学平衡的过程中,混合气体的平均相对分子质量随时间的变化如图2所示,测得达到平衡时A、B、C、D的物质的量均为1 mol。
①若在恒温恒容的条件下,向该平衡体系中再通入A、B、C、D各1 mol,则体系中气体的平均相对分子质量(填“增大”、“减小”、“不变”或“无法确定”)
②若恒温恒压的条件下,向原平衡体系中再通入A、B、C、D各1 mol,则体系中气体的密度(填“增大”、“减小”、“不变”或“无法确定”)
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氧气是一种常见的氧化剂,用途广泛。回答下列问题:
(1)用H2O2制取O2时,分解的热化学方程式为: 2H2O2(aq)=2H2O(l) +O2(g) ΔH= a kJ·mol-1
①相同条件下,H2O2分解时,无论是否使用催化剂,均不会改变的是_______ (填标号)。
A 反应速率 B 反应热 C 活化能 D 生成物
②以Fe3+作催化剂时,H2O2的分解反应分两步进行,第一步反应为: H2O2(aq) + 2Fe3+ (aq)=2Fe2+ (aq) +O2(g) +2H+ (aq)ΔH=b kJ·mol-1
第二步反应的热化学方程式为____________ 。
(2)工业上用Cl2生产某些含氯有机物时产生HCl副产物,可用O2将其转化为Cl2,实现循环利用[O2(g) + 4HCl(g) 2Cl2(g) + 2H2O(g)]。将1 molO2和4 molHCl充入某恒容密闭容器中,分别在T1和T2的温度下进行实验,测得容器内总压强(p)与反应时间(t)的变化关系如图所示。
2Cl2(g) + 2H2O(g)]。将1 molO2和4 molHCl充入某恒容密闭容器中,分别在T1和T2的温度下进行实验,测得容器内总压强(p)与反应时间(t)的变化关系如图所示。
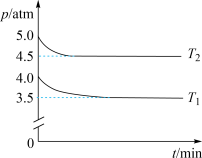
①该反应的速率v = k ca(O2)·cb(HCl)(k为速率常数),下列说法正确的是____________ (填标号)。
A 使用催化剂,k不变
B 温度升高,k增大
C 平衡后分离出水蒸气,k变小
D 平衡后再充入1molO2和4molHCl,反应物转化率都增大
②T1________ T2(填“>”或“<”)。该反应的ΔH______ 0(填“>”或“<”),判断的依据是_________ 。
③T2时,HCl的平衡转化率=________ ,反应的Kx=_____ (Kx为以物质的量分数表示的平衡常数)。
(1)用H2O2制取O2时,分解的热化学方程式为: 2H2O2(aq)=2H2O(l) +O2(g) ΔH= a kJ·mol-1
①相同条件下,H2O2分解时,无论是否使用催化剂,均不会改变的是
A 反应速率 B 反应热 C 活化能 D 生成物
②以Fe3+作催化剂时,H2O2的分解反应分两步进行,第一步反应为: H2O2(aq) + 2Fe3+ (aq)=2Fe2+ (aq) +O2(g) +2H+ (aq)ΔH=b kJ·mol-1
第二步反应的热化学方程式为
(2)工业上用Cl2生产某些含氯有机物时产生HCl副产物,可用O2将其转化为Cl2,实现循环利用[O2(g) + 4HCl(g)
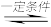 2Cl2(g) + 2H2O(g)]。将1 molO2和4 molHCl充入某恒容密闭容器中,分别在T1和T2的温度下进行实验,测得容器内总压强(p)与反应时间(t)的变化关系如图所示。
2Cl2(g) + 2H2O(g)]。将1 molO2和4 molHCl充入某恒容密闭容器中,分别在T1和T2的温度下进行实验,测得容器内总压强(p)与反应时间(t)的变化关系如图所示。
①该反应的速率v = k ca(O2)·cb(HCl)(k为速率常数),下列说法正确的是
A 使用催化剂,k不变
B 温度升高,k增大
C 平衡后分离出水蒸气,k变小
D 平衡后再充入1molO2和4molHCl,反应物转化率都增大
②T1
③T2时,HCl的平衡转化率=
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】滴定法是实验室和工业生产中常用的一种简便、快速和应用广泛的定量分析方法.在实验室用 溶液分别滴定体积均为
溶液分别滴定体积均为 浓度均为
浓度均为 的盐酸和醋酸溶液,得到溶液
的盐酸和醋酸溶液,得到溶液 随加入
随加入 溶液体积而变化的两条滴定曲线.
溶液体积而变化的两条滴定曲线.

(1)用 溶液滴定醋酸溶液,滴定终点的现象是
溶液滴定醋酸溶液,滴定终点的现象是______________ ,若滴定终点时仰视滴定管刻度线,则会使所测的消耗的 溶液体积
溶液体积______________ (填“偏大”、或“偏小”)
(2)滴定醋酸的曲线是______________ (填“Ⅰ”或“Ⅱ”)
(3)图中 和
和 大小的比较:
大小的比较:
_______________  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(4)下列方法中可使溶液中醋酸的电离程度增大的是______________(填字母序号)
(5)下列图像能说明醋酸钠的水解反应达到平衡的是______________
(6)室温时,向 醋酸溶液中加入等体积的
醋酸溶液中加入等体积的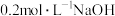 溶液,充分反应后所得溶液显酸性,则所得溶液中的离子大小顺序为
溶液,充分反应后所得溶液显酸性,则所得溶液中的离子大小顺序为______________
 溶液分别滴定体积均为
溶液分别滴定体积均为 浓度均为
浓度均为 的盐酸和醋酸溶液,得到溶液
的盐酸和醋酸溶液,得到溶液 随加入
随加入 溶液体积而变化的两条滴定曲线.
溶液体积而变化的两条滴定曲线.
(1)用
 溶液滴定醋酸溶液,滴定终点的现象是
溶液滴定醋酸溶液,滴定终点的现象是 溶液体积
溶液体积(2)滴定醋酸的曲线是
(3)图中
 和
和 大小的比较:
大小的比较:
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)(4)下列方法中可使溶液中醋酸的电离程度增大的是______________(填字母序号)
| A.适度升温 | B.加少量冰醋酸 |
| C.加少量醋酸钠固体 | D.加少量碳酸钠固体 |
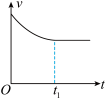
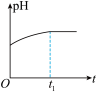
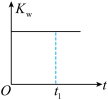
(5)下列图像能说明醋酸钠的水解反应达到平衡的是
A.溶液中 与反应时间t的关系 与反应时间t的关系 | B. 的水解速率与反应时间t的关系 的水解速率与反应时间t的关系 | C.溶液的pH与反应时间t的关系 | D.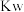 与反应时间t的关系 与反应时间t的关系 |
 |  |  |  |
(6)室温时,向
 醋酸溶液中加入等体积的
醋酸溶液中加入等体积的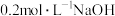 溶液,充分反应后所得溶液显酸性,则所得溶液中的离子大小顺序为
溶液,充分反应后所得溶液显酸性,则所得溶液中的离子大小顺序为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
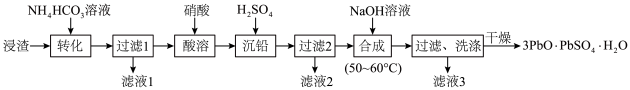
【推荐2】一种从铋冶炼浸渣(浸渣中的铅多数以硫酸铅的形态存在,少量以氧化铅、碳酸铅的形态存在)为原料生产三盐基硫酸铅( )的工艺流程如图所示。
)的工艺流程如图所示。
已知常温下,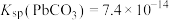 ,
, ,
,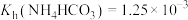 ,
,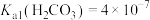
回答下列问题:
(1)常温下, 的电离平衡常数
的电离平衡常数
_______ 。
(2)写出转化过程 发生反应的化学方程式
发生反应的化学方程式_______ ,Pb的转化率随着 用量的增加而增加,醋酸可以促进硫酸铅溶解,但实验表明:Pb的转化率随醋酸用量的增加而减少,这是由于
用量的增加而增加,醋酸可以促进硫酸铅溶解,但实验表明:Pb的转化率随醋酸用量的增加而减少,这是由于_______ 。
(3)测得滤液1中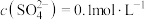 ,则该滤液中
,则该滤液中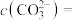
_______  (保留1位小数);滤液2中可以循环利用的物质是
(保留1位小数);滤液2中可以循环利用的物质是_______ ;从滤液3可提取出一种含结晶水的钠盐副产品,若测定该晶体中结晶水的含量,所需的仪器除三脚架、托盘天平、瓷坩埚、干燥器、酒精灯、玻璃棒,还需要的仪器有_______ 。
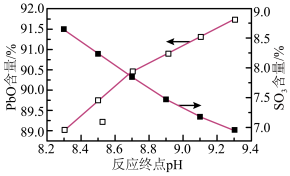
(4)合成三盐基硫酸铅时,影响产品纯度的因素很多,其中反应终点pH对产品中PbO和 含量的影响如下图(将
含量的影响如下图(将 看作是PbO和
看作是PbO和 ,经测定三盐基硫酸铅中PbO理论含量90.10%,
,经测定三盐基硫酸铅中PbO理论含量90.10%, 理论含量8.08%),则反应终点控制pH的范围是_______。(填序号)。
理论含量8.08%),则反应终点控制pH的范围是_______。(填序号)。
 )的工艺流程如图所示。
)的工艺流程如图所示。
已知常温下,
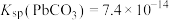 ,
, ,
,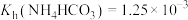 ,
,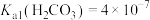
回答下列问题:
(1)常温下,
 的电离平衡常数
的电离平衡常数
(2)写出转化过程
 发生反应的化学方程式
发生反应的化学方程式 用量的增加而增加,醋酸可以促进硫酸铅溶解,但实验表明:Pb的转化率随醋酸用量的增加而减少,这是由于
用量的增加而增加,醋酸可以促进硫酸铅溶解,但实验表明:Pb的转化率随醋酸用量的增加而减少,这是由于(3)测得滤液1中
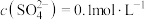 ,则该滤液中
,则该滤液中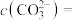
 (保留1位小数);滤液2中可以循环利用的物质是
(保留1位小数);滤液2中可以循环利用的物质是(4)合成三盐基硫酸铅时,影响产品纯度的因素很多,其中反应终点pH对产品中PbO和
 含量的影响如下图(将
含量的影响如下图(将 看作是PbO和
看作是PbO和 ,经测定三盐基硫酸铅中PbO理论含量90.10%,
,经测定三盐基硫酸铅中PbO理论含量90.10%, 理论含量8.08%),则反应终点控制pH的范围是_______。(填序号)。
理论含量8.08%),则反应终点控制pH的范围是_______。(填序号)。
| A.<8.4 | B.8.4~8.8 | C.8.8~9.2 | D.>9.2 |
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
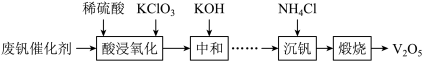
【推荐3】五氧化二钒(V2O5)广泛用作合金添加剂及有机化工催化剂。从废钒催化剂(含有V2O5、VOSO4及少量Fe2O3、Al2O3等杂质)回收V2O5的部分工艺流程如下:
已知:
a.常温下,部分含钒物质在水中的溶解性见下表:
b.+5价钒在溶液中的主要存在形式与溶液pH的关系见下表;
(1)“酸浸、氧化”时VO2+发生反应的离子方程式为_______ 。
(2)“中和”时调节pH为7的目的,一是沉淀部分杂质离子;二是_______ 。
(3)①“沉钒”前需将溶液先进行“离子交换”和“洗脱”,再加入NH4Cl生成NH4VO3;“离子交换”和“洗脱”两步操作可简单表示为: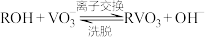 (ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_______ (填“酸性”或“碱性”),理由是_______ 。
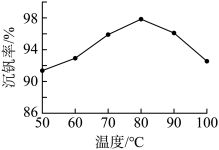
②用沉钒率(NH4VO3沉淀中V的质量和废钒催化剂中V的质量之比)表示该工艺钒的回收率。题14-1图中是沉钒率随温度变化的关系曲线,沉钒时,温度超过80℃以后,沉钒率下降的可能原因是_______ 。
(4)在Ar气氛中加热“煅烧”NH4VO3,测得加热升温过程中固体的质量变化如图所示,加热分解NH4VO3制备V2O5需要控制的温度为_______ (写出计算推理过程)。

(5)新型催化材料磷化钒(VP)的晶胞结构如图所示,V作简单六方棱柱体排列,P交替地填入一半的V的正三棱柱中心空隙。与V原子距离相等且最近的P原子有_______ 个。


已知:
a.常温下,部分含钒物质在水中的溶解性见下表:
| 物质 | V2O5 | VOSO4 | (VO2)2SO4 | NH4VO3 |
| 溶解性 | 难溶 | 可溶 | 易溶 | 难溶 |
| pH | <6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |
(2)“中和”时调节pH为7的目的,一是沉淀部分杂质离子;二是
(3)①“沉钒”前需将溶液先进行“离子交换”和“洗脱”,再加入NH4Cl生成NH4VO3;“离子交换”和“洗脱”两步操作可简单表示为:
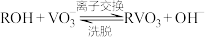 (ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈②用沉钒率(NH4VO3沉淀中V的质量和废钒催化剂中V的质量之比)表示该工艺钒的回收率。题14-1图中是沉钒率随温度变化的关系曲线,沉钒时,温度超过80℃以后,沉钒率下降的可能原因是

(4)在Ar气氛中加热“煅烧”NH4VO3,测得加热升温过程中固体的质量变化如图所示,加热分解NH4VO3制备V2O5需要控制的温度为

(5)新型催化材料磷化钒(VP)的晶胞结构如图所示,V作简单六方棱柱体排列,P交替地填入一半的V的正三棱柱中心空隙。与V原子距离相等且最近的P原子有

您最近半年使用:0次



