名校
1 . NA为阿伏加德罗常数的值,下列说法正确的是
| A.常温下,2.7g铝片投入足量的浓硫酸中,铝失去的电子数为0.3NA |
B.含0.5molCr2O 的酸性溶液与足量H2O2反应生成 的酸性溶液与足量H2O2反应生成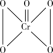 ,转移电子数4NA ,转移电子数4NA |
| C.1molXeF4中氙的价层电子对数为4NA |
| D.标准状况下,22.4LCH4和44.8LCl2在光照下充分反应后的分子数为3NA |
您最近一年使用:0次
2 . 某化学兴趣小组模拟侯氏制碱法制取Na2CO3产品并回收NH4Cl,设计如下实验方案。
Ⅰ.NaHCO3的制备,实验装置如图甲:
②向反应器中通入CO2气体,待溶液变为无色后,再加入10mL浓氨水,继续通入CO2.
③再加入10mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO2至生成大量NaHCO3晶体。
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO3晶体。
Ⅱ.Na2CO3的制备
将制得的NaHCO3晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,冷却到室温并称量。
Ⅲ.NH4Cl的回收
加热母液使NH4HCO3分解,滴加氨水至溶液呈碱性,操作b,抽滤,洗涤,置于干燥器中干燥,称重。
(1)仪器a的名称是_____ 。
(2)步骤③中通入过量CO2生成NaHCO3晶体的离子方程式为_____ 。
(3)已知0℃时NaHCO3的溶解度是0.8mol·L-1,不考虑溶液混合时体积的变化及对NaHCO3溶解度的影响,若10.0gNaCl全部转化成NaHCO3,则在0℃时从溶液中能析出NaHCO3固体_____ g(保留1位小数)。
(4)已知碳酸氢钠分解反应的ΔH=+135.6kJ·mol-1·K-1、ΔS=+333.3J·mol-1·K-1。在下列哪些温度下该反应能自发进行_____(填标号)。
(5)①回收NH4Cl时加入氨水的目的是_____ 。
②结合图乙,简单说明操作b的过程_____ 。
(6)若制得的NaHCO3中含有未反应的NaCl,则分解后所得固体的质量_____ (填“大于”、“小于”或“等于”)理论上生成Na2CO3的质量。
Ⅰ.NaHCO3的制备,实验装置如图甲:

②向反应器中通入CO2气体,待溶液变为无色后,再加入10mL浓氨水,继续通入CO2.
③再加入10mL浓氨水,充分振荡,使NaCl完全溶解,继续通入过量CO2至生成大量NaHCO3晶体。
④将反应器冷却,然后抽滤,回收母液。用无水乙醇洗涤沉淀,收集NaHCO3晶体。
Ⅱ.Na2CO3的制备
将制得的NaHCO3晶体转移到已称量的蒸发皿中,加热至质量不再改变,停止加热,冷却到室温并称量。
Ⅲ.NH4Cl的回收
加热母液使NH4HCO3分解,滴加氨水至溶液呈碱性,操作b,抽滤,洗涤,置于干燥器中干燥,称重。
(1)仪器a的名称是
(2)步骤③中通入过量CO2生成NaHCO3晶体的离子方程式为
(3)已知0℃时NaHCO3的溶解度是0.8mol·L-1,不考虑溶液混合时体积的变化及对NaHCO3溶解度的影响,若10.0gNaCl全部转化成NaHCO3,则在0℃时从溶液中能析出NaHCO3固体
(4)已知碳酸氢钠分解反应的ΔH=+135.6kJ·mol-1·K-1、ΔS=+333.3J·mol-1·K-1。在下列哪些温度下该反应能自发进行_____(填标号)。
| A.308K | B.373K | C.421K | D.573K |
(5)①回收NH4Cl时加入氨水的目的是
②结合图乙,简单说明操作b的过程
(6)若制得的NaHCO3中含有未反应的NaCl,则分解后所得固体的质量
您最近一年使用:0次
3 . 下列气体去除杂质的方法中,不能实现目的的是
| 气体(杂质) | 方法 | |
| A | 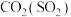 | 通过酸性高锰酸钾溶液 |
| B |  | 通过饱和的食盐水 |
| C | 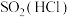 | 饱和  溶液 溶液 |
| D | 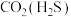 | 通过氢氧化钠溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
4 . 下列离子方程式中,书写正确的是
A.碳酸钠溶液中滴加少量盐酸: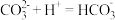 | B.向 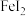 溶液中通入少量 溶液中通入少量 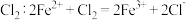 |
C.向 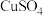 溶液中通入 溶液中通入  气体: 气体: | D.浓盐酸与铁屑反应: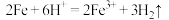 |
您最近一年使用:0次
名校
解题方法
5 . 阿伏加德罗常数的值为 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是A.常温常压下 和 和 混合气体中氧原子总数为 混合气体中氧原子总数为 |
B.电解精炼铜时阳极质量减轻 ,电路中转移电子数目一定为 ,电路中转移电子数目一定为 |
C. 和 和 于密闭容器中充分反应后,其分子总数为 于密闭容器中充分反应后,其分子总数为 |
D.常温下,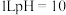 的氨水溶液中,发生电离的水分子数为 的氨水溶液中,发生电离的水分子数为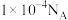 |
您最近一年使用:0次
6 . 下列叙述正确的是
| A.在标准状况下,22.4L水中含有1mol H2O分子 |
| B.0.1mol Cl2被NaOH溶液充分吸收,转移电子数为0.2NA |
| C.在标准状况下,2.24L O2和CO的混合气体中含C、O原子共0.2mol |
D.0.1mol FeCl3形成Fe(OH)3胶体,Fe(OH)3胶粒的数目为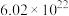 |
您最近一年使用:0次
2024-01-20更新
|
98次组卷
|
2卷引用:湖南省永州市蓝山县第二中学2023-2024学年高一上学期第三次月考化学试卷
名校
7 . 某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。回答下列问题:
实验一:利用下图所示装置制取氯酸钾和氯水(加热装置和夹持装置已略去)

(1)仪器a的名称是___________ 。
(2)丙溶液中存在的分子有___________ 种。
(3)甲烧瓶中离子方程式是___________ ,若反应中消耗的固体质量为43.5克,则被氧化的HCl的物质的量为___________ 。
(4)氯气与30%KOH溶液反应生成氯酸钾和氯化钾,温度需控制在70~80℃之间,宜采用的加热方式是___________ ,该反应中氧化剂和还原剂的物质的量之比为___________ 。
(5)若丙中为石灰乳,则制得的漂白粉主要成分是___________ (填化学式)。
实验一:利用下图所示装置制取氯酸钾和氯水(加热装置和夹持装置已略去)

(1)仪器a的名称是
(2)丙溶液中存在的分子有
(3)甲烧瓶中离子方程式是
(4)氯气与30%KOH溶液反应生成氯酸钾和氯化钾,温度需控制在70~80℃之间,宜采用的加热方式是
(5)若丙中为石灰乳,则制得的漂白粉主要成分是
您最近一年使用:0次
名校
解题方法
8 . 化学上用分类法学习化学物质的共性,用比较法学习化学物质的特性,物质的氧化性与还原性尤为重要。回答下列问题:
(1)磷元素的含氧酸有H3PO4、H3PO3(亚磷酸)、H3PO2(次磷酸)等多种,其中已知:H3PO3+2NaOH(过量)=Na2HPO3+2H2O。H3PO3属于___________ (填“一”“二”或“三”)元酸。Na2HPO3属于___________ (填“正盐”或“酸式盐”)。
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式。___________
______Fe(OH)3+______CH4+______H+ ______Fe2++______HCO
______Fe2++______HCO +_______。
+_______。
(3)强酸反应体系中发生的一个离子反应中,反应物和生成物共六种微粒:Fe2+、NO 、Fe3+、NH
、Fe3+、NH 、H+和H2O,写出该反应的离子方程式
、H+和H2O,写出该反应的离子方程式___________ 。
(4)NaBH4(B为+3价)常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1 mol NaBH4的还原能力相当于___________ mol H2的还原能力。ClO2是一种新型消毒剂,其消毒效率(单位质量得电子的能力)是Cl2的___________ 倍。(保留2位小数)
(1)磷元素的含氧酸有H3PO4、H3PO3(亚磷酸)、H3PO2(次磷酸)等多种,其中已知:H3PO3+2NaOH(过量)=Na2HPO3+2H2O。H3PO3属于
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式。
______Fe(OH)3+______CH4+______H+
 ______Fe2++______HCO
______Fe2++______HCO +_______。
+_______。(3)强酸反应体系中发生的一个离子反应中,反应物和生成物共六种微粒:Fe2+、NO
 、Fe3+、NH
、Fe3+、NH 、H+和H2O,写出该反应的离子方程式
、H+和H2O,写出该反应的离子方程式(4)NaBH4(B为+3价)常用作还原剂,H2也是常见的还原剂。与相同氧化剂反应时,1 mol NaBH4的还原能力相当于
您最近一年使用:0次
解题方法
9 . 下列氧化还原反应中电子转移的表示方法正确的是
A. | B.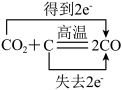 |
C.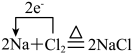 | D.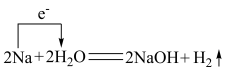 |
您最近一年使用:0次
解题方法
10 . 妈妈教小鲁蒸馒头:先用酵头发面,面团发酵至两倍大后,再加纯碱调节酸性,然后将面团揉切后上锅蒸即可。小鲁查阅资料得知,酵头可使面团在微生物作用下产生CO2气体,从而使面团疏松,但同时也会产生乳酸、醋酸等有机酸。
(1)下列关于纯碱的认识正确的是________(填字母)。
(2)小鲁探究用Na2CO3调节面团酸度,而不用NaHCO3的原因。
相同质量的碳酸钠与碳酸氢钠与足量的盐酸反应,消耗盐酸较多的是________ 。
(3)小餐实际操作时,发现面团发得不好;面团内的气孔少,略有酸味。妈妈指导小鲁将Na2CO3改用NaHCO3,继续揉面,上锅蒸煮后果然蒸出了松软的馒头。该过程中NaHCO3发生的反应,其化学反应方程式为________ 。
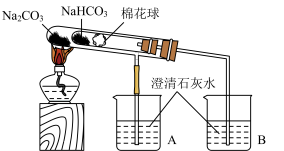
(4)用套管实验装置可以更好地比较Na2CO3和NaHCO3的热稳定性,其中小试管内有沾有无水硫酸铜粉末的棉花球,实验装置如图。
实验时,观察小试管内棉花球上的无水硫酸铜颜色变化是________ 。烧杯________ (填“A”或“B”)中澄清石灰水变浑浊。
若将大小试管中的Na2CO3和NaHCO3位置互换,________ (填“能”或“不能”)得出相同的实验结论。
(1)下列关于纯碱的认识正确的是________(填字母)。
| A.受热易分解 | B.水溶液显碱性 | C.属于碱 | D.可与酸反应。 |
(2)小鲁探究用Na2CO3调节面团酸度,而不用NaHCO3的原因。
相同质量的碳酸钠与碳酸氢钠与足量的盐酸反应,消耗盐酸较多的是
(3)小餐实际操作时,发现面团发得不好;面团内的气孔少,略有酸味。妈妈指导小鲁将Na2CO3改用NaHCO3,继续揉面,上锅蒸煮后果然蒸出了松软的馒头。该过程中NaHCO3发生的反应,其化学反应方程式为
(4)用套管实验装置可以更好地比较Na2CO3和NaHCO3的热稳定性,其中小试管内有沾有无水硫酸铜粉末的棉花球,实验装置如图。
实验时,观察小试管内棉花球上的无水硫酸铜颜色变化是
若将大小试管中的Na2CO3和NaHCO3位置互换,

您最近一年使用:0次



