1 . 某离子反应涉及到H2O、ClO-、NH 、OH-、N2、Cl-等微粒,其中N2、ClO-的粒子数随时间变化的曲线如图所示,下列说法正确的是。
、OH-、N2、Cl-等微粒,其中N2、ClO-的粒子数随时间变化的曲线如图所示,下列说法正确的是。

 、OH-、N2、Cl-等微粒,其中N2、ClO-的粒子数随时间变化的曲线如图所示,下列说法正确的是。
、OH-、N2、Cl-等微粒,其中N2、ClO-的粒子数随时间变化的曲线如图所示,下列说法正确的是。
| A.该反应中 Cl-为氧化产物 |
| B.氧化剂与还原剂的物质的量之比为3:2 |
| C.反应后溶液的碱性减弱 |
| D.反应中每生成 1mol N2转移3NA个电子 |
您最近一年使用:0次
名校
2 . 已知氧化性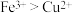 ,向物质的量浓度均为
,向物质的量浓度均为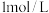 的
的 、
、 的
的 混合液中加入
混合液中加入 铁粉,充分反应后,下列说法正确的是
铁粉,充分反应后,下列说法正确的是
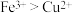 ,向物质的量浓度均为
,向物质的量浓度均为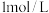 的
的 、
、 的
的 混合液中加入
混合液中加入 铁粉,充分反应后,下列说法正确的是
铁粉,充分反应后,下列说法正确的是A.当 时,发生的反应为 时,发生的反应为 |
B.当固体有剩余时,溶液中存一定存在 、 、 离子 离子 |
C.当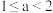 时,溶液中 时,溶液中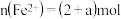 |
| D.若有固体剩余,则固体中一定有铁,可能有铜 |
您最近一年使用:0次
名校
解题方法
3 . 过氧化钠可在呼吸面具和潜水艇中作供氧剂,实验室可用如图装置进行验证(A是实验室中制取CO2的装置,C中盛放的是过氧化钠)。下列说法不正确的是
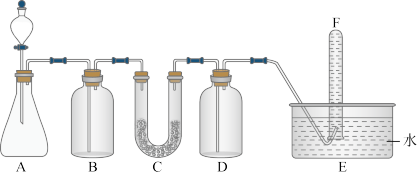

A.A中发生的反应离子方程式为: +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
| B.B中盛放饱和NaHCO3溶液,目的是除去CO2中的HCl气体 |
| C.C中每转移0.2mol电子,产生O2 0.1mol |
| D.D装置是安全瓶,防止E中水倒流进入C中 |
您最近一年使用:0次
2022-03-22更新
|
745次组卷
|
3卷引用:江西省宜春市奉新县第一中学2021-2022学年高一下学期第一次月考化学试题
名校
4 . 某企业利用下列流程综合处理工厂排放的含有SO2的烟气,以减少其对环境造成的污染。下列有关说法正确的是
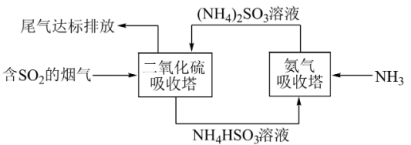

A.二氧化硫吸收塔中加入亚硫酸铵发生的反应为SO2+SO +H2O=HSO +H2O=HSO |
B.氨气吸收塔中发生的反应为HSO +OH-=H2O+SO +OH-=H2O+SO |
| C.上述流程利用的是氧化还原反应原理 |
| D.上述流程中SO2不可循环利用 |
您最近一年使用:0次
名校
5 . 根据相关递变规律及物质结构特点,下列判断错误的是
A.碱性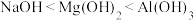 |
B.最高正价: |
| C.熔沸点:HF>HI>HBr>HCl |
| D.金属钾密度小于钠,均可保存在煤油中 |
您最近一年使用:0次
名校
6 . 下列物质中,既能和盐酸反应,又能和氢氧化钠反应的是
| A.NaHCO3 | B.Na2CO3 | C.Al2O3 | D.Fe(OH)3 |
您最近一年使用:0次
2022-03-02更新
|
135次组卷
|
2卷引用:江西省抚州市临川区第一中学2021-2022学年高一下学期第一次月考化学试题
7 . 在常温下发生以下几个反应,根据反应判断下列结论正确的是
①16H++10Z− +2XO =2X2++5Z2+8H2O
=2X2++5Z2+8H2O
②2A2++5B2=2A3++2B−
③2B−+ Z2=B2+2Z−
①16H++10Z− +2XO
 =2X2++5Z2+8H2O
=2X2++5Z2+8H2O②2A2++5B2=2A3++2B−
③2B−+ Z2=B2+2Z−
| A.溶液中不能发生: Z2+2A2+=2A3++2Z− |
| B.Z元素在①③反应中均被氧化 |
C.氧化性由弱到强的顺序是:XO 、 Z2、B2、A3+ 、 Z2、B2、A3+ |
D.XO 可以被A2+还原 可以被A2+还原 |
您最近一年使用:0次
2022-01-23更新
|
639次组卷
|
3卷引用:江西省南昌市第十九中学2022-2023学年高一上学期第一次月考(10月)化学试题
名校
8 . 几种短周期元素的原子半径及主要化合价如下表所示:
根据表中信息,判断以下说法正确的是
| 元素符号 | X | Y | Z | R | T |
| 原子半径(nm) | 0.160 | 0.089 | 0.102 | 0.143 | 0.074 |
| 主要化合价 |  |  |  、 、 、 、 |  |  |
A.单质与稀硫酸反应的剧烈程度: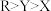 |
B.离子半径: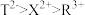 |
| C.Y的氯化物中,各原子的最外层均满足8电子稳定结构 |
D.相同条件下,简单气态氢化物的稳定性: |
您最近一年使用:0次
名校
9 . 1943年侯德榜发明联合制碱法,其生产流程可简要表示为:

下列说法错误的是

下列说法错误的是
A.第②步涉及的主要反应为 |
B.流程中若先通入 再通入 再通入 可达同样效果 可达同样效果 |
| C.若实验室进行第③步操作,需要用到的玻璃仪器有:烧杯和漏斗 |
D.用 溶液可鉴别 溶液可鉴别 与 与 |
您最近一年使用:0次
2022-01-23更新
|
291次组卷
|
2卷引用:江西省2021-2022学年高一上学期期末调研化学试题
名校
10 . 下列叙述错误的是
A. 的热稳定性弱于 的热稳定性弱于 |
B.向 中加少量水, 中加少量水, 能溶解,伴随放热现象 能溶解,伴随放热现象 |
C. 长期放置在空气中,最终都变成 长期放置在空气中,最终都变成 |
D.保持温度不变,向 饱和溶液中通入 饱和溶液中通入 ,有 ,有 晶体析出 晶体析出 |
您最近一年使用:0次



