1 . 某工业烟气中含有CO、 、
、 等气体,用
等气体,用 溶液吸收并回收
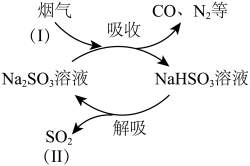
溶液吸收并回收 的过程如图所示。
的过程如图所示。
(1) 的浓度:Ⅰ
的浓度:Ⅰ__________ Ⅱ(填“>”或“<”)。
(2)图示过程中可以循环利用的物质是___________________________________ (填化学式)。
(3)上述吸收过程中发生的主要反应的化学方程式是____________________________________ 。
(4)解吸过程需要加热,在这个过程中常伴有少量 产生。
产生。
①证明产物中含 的实验方法是:取少量解吸后的溶液,
的实验方法是:取少量解吸后的溶液,_______________________________ (填操作和现象)。
②产生 的原因是
的原因是_________________________________________________________________ 。
 、
、 等气体,用
等气体,用 溶液吸收并回收
溶液吸收并回收 的过程如图所示。
的过程如图所示。(1)
 的浓度:Ⅰ
的浓度:Ⅰ(2)图示过程中可以循环利用的物质是
(3)上述吸收过程中发生的主要反应的化学方程式是
(4)解吸过程需要加热,在这个过程中常伴有少量
 产生。
产生。①证明产物中含
 的实验方法是:取少量解吸后的溶液,
的实验方法是:取少量解吸后的溶液,②产生
 的原因是
的原因是
您最近半年使用:0次
2020-10-02更新
|
447次组卷
|
7卷引用:【区级联考】北京市朝阳区2018-2019学年高一上学期期末考试化学试题
【区级联考】北京市朝阳区2018-2019学年高一上学期期末考试化学试题新人教版必修2同步测试:5.1.3不同价态含硫物质的转化人教版(2019)必修第二册第五章第一节课时1山东省淄博市第七中学2019-2020学年高一3月线上考试化学试题必修第二册RJ第5章第一节 硫及其化合物 课时1 硫和二氧化硫高一必修第一册(苏教2019版)专题4 第一单元 含硫化合物的性质 课时1 二氧化硫的性质和应用(已下线)第14讲 硫、二氧化硫【暑假自学课】2022年新高一化学暑假精品课(鲁科版2019必修第一册)
解题方法
2 . 市场上一些看起来非常白而又鲜亮诱人的银耳竟然是用硫黄熏蒸而成的。央视记者暗访银耳变白内幕:工人们不停地对白色银耳进行翻炒,散发出一股刺鼻的气味;一名工人抓起淡黄色块状的东西放进一个小锅里,用火点燃,紧接着把小锅放进有薄膜覆盖的银耳地里。请回答下列问题:
(1)“工人抓起淡黄色块状的东西放进一个小锅里,用火点燃”。其中“淡黄色块状的东西”是__ (写化学式),其在空气中燃烧时火焰的颜色为__ 。该反应的化学方程式为__ 。
(2)用硫黄来熏蒸食品的主要目的是__ (填“增加营养”或“漂白”)。
(3)焦亚硫酸钠是一种食品添加剂,通常为白色或微黄色结晶粉末,其对应的酸是焦亚硫酸,焦亚硫酸可以看作两分子的H2SO3缩掉一分子水而形成的物质,所以焦亚硫酸的分子式为__ ,焦亚硫酸钠在工业上通常是通过将SO2通入饱和碳酸钠溶液中制得的,请写出该反应的化学方程式:__ ,该反应是__ (填“氧化还原反应”或“非氧化还原反应”)。焦亚硫酸钠在水溶液中反应可以生成SO ,所以溶液中存在SO
,所以溶液中存在SO ,由此可推断能够对食品进行漂白、杀菌的有效成分是
,由此可推断能够对食品进行漂白、杀菌的有效成分是__ ,该成分可以与有色物质结合,生成无色物质,该无色物质的特性是__ ,由此可见,食品中该物质超标时,容易导致食用者中毒。
(4)下列食品肯定不会用SO2熏制的是__ (填序号)。
A.色泽鲜艳的干黄花菜 B.苍白亮丽的馒头
C.鲜嫩无比的鲜菠菜 D.晶莹剔透的干鱼片
(5)小明的妈妈在农贸市场买了一些干燥的银耳,颜色为亮丽的白色。可是,一个月后拿出来准备食用时,发现银耳变为暗暗的淡黄色。请你判断该银耳是否用SO2熏蒸过,并说明理由:__ 。
(1)“工人抓起淡黄色块状的东西放进一个小锅里,用火点燃”。其中“淡黄色块状的东西”是
(2)用硫黄来熏蒸食品的主要目的是
(3)焦亚硫酸钠是一种食品添加剂,通常为白色或微黄色结晶粉末,其对应的酸是焦亚硫酸,焦亚硫酸可以看作两分子的H2SO3缩掉一分子水而形成的物质,所以焦亚硫酸的分子式为
 ,所以溶液中存在SO
,所以溶液中存在SO ,由此可推断能够对食品进行漂白、杀菌的有效成分是
,由此可推断能够对食品进行漂白、杀菌的有效成分是(4)下列食品肯定不会用SO2熏制的是
A.色泽鲜艳的干黄花菜 B.苍白亮丽的馒头
C.鲜嫩无比的鲜菠菜 D.晶莹剔透的干鱼片
(5)小明的妈妈在农贸市场买了一些干燥的银耳,颜色为亮丽的白色。可是,一个月后拿出来准备食用时,发现银耳变为暗暗的淡黄色。请你判断该银耳是否用SO2熏蒸过,并说明理由:
您最近半年使用:0次
2020-09-16更新
|
99次组卷
|
2卷引用:鲁科版(2019)高一必修第一册第三章易错疑难集训(二)
19-20高一·全国·课时练习
解题方法
3 . 下表是部分城市某日空气质量日报:
(1)由表可知,空气质量日报中涉及的污染物主要是________ 和可吸入颗粒物(PM10)。
(2)SO2的排放是造成酸雨的主要因素。形成酸雨的原因之一可简单表示如图:
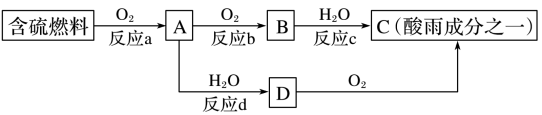
请回答下列问题:
①酸雨的pH________ (填“>”“<”或“=”)5.6。
②反应b的化学方程式为_________ 。
③在一段时间内连续不断测定溶液D的pH,发现pH变小,表示该变化的化学方程式是______ 。
④若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出该反应的离子方程式:_________ 。
| 城市 | 污染指数 | 首要污染物 | 空气质量等级 | ||
| SO2 | NO2 | PM10 | |||
| A | 98 | 23 | 67 | SO2 | Ⅱ |
| B | 47 | 29 | 35 | SO2 | Ⅰ |
| C | 62 | 80 | 113 | PM10 | Ⅲ |
| D | 52 | 76 | 59 | NO2 | Ⅰ |
(2)SO2的排放是造成酸雨的主要因素。形成酸雨的原因之一可简单表示如图:

请回答下列问题:
①酸雨的pH
②反应b的化学方程式为
③在一段时间内连续不断测定溶液D的pH,发现pH变小,表示该变化的化学方程式是
④若用足量的氢氧化钠溶液吸收含二氧化硫的工业废气,写出该反应的离子方程式:
您最近半年使用:0次
解题方法
4 . 某兴趣小组为探究 的性质,将
的性质,将 固体隔绝空气加热进行实验。已知加热会生成硫酸钠和另一种中学常见物质,加热前后,固体的质量没有变化。取加热后的固体溶于水,滴加稀盐酸,出现淡黄色沉淀。
固体隔绝空气加热进行实验。已知加热会生成硫酸钠和另一种中学常见物质,加热前后,固体的质量没有变化。取加热后的固体溶于水,滴加稀盐酸,出现淡黄色沉淀。
(1)生成的淡黄色沉淀是________ (填名称)。
(2)写出 固体隔绝空气加热的化学方程式
固体隔绝空气加热的化学方程式_________ 。
(3)设计实验证明分解后产物中的硫酸钠固体__________ 。
 的性质,将
的性质,将 固体隔绝空气加热进行实验。已知加热会生成硫酸钠和另一种中学常见物质,加热前后,固体的质量没有变化。取加热后的固体溶于水,滴加稀盐酸,出现淡黄色沉淀。
固体隔绝空气加热进行实验。已知加热会生成硫酸钠和另一种中学常见物质,加热前后,固体的质量没有变化。取加热后的固体溶于水,滴加稀盐酸,出现淡黄色沉淀。(1)生成的淡黄色沉淀是
(2)写出
 固体隔绝空气加热的化学方程式
固体隔绝空气加热的化学方程式(3)设计实验证明分解后产物中的硫酸钠固体
您最近半年使用:0次
5 . I已知:还原性HSO >I-,氧化性IO
>I-,氧化性IO > I2 。
> I2 。
(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目_______ 。
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式_______ ;当溶液中I-与I2的物质的量之比为5:3时,加入的NaIO3为_______ mol。

II 已知:KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2、KHSO4等物质。写出该反应的化学方程式________________ 。
 >I-,氧化性IO
>I-,氧化性IO > I2 。
> I2 。(1)在NaIO3溶液中滴加少量NaHSO3溶液,发生下列反应。配平反应方程式并用单线桥标出电子转移的方向和数目
囗NaIO3+囗NaHSO3→ 囗I2+囗Na2SO4+囗H2SO4+囗H2O
(2)在含5molNaHSO3的溶液中逐滴加入NaIO3溶液。加入NaIO3的物质的量和析出I2单质的物质的量的关系曲线如图所示。写出反应过程中与AB段曲线对应的离子方程式

II 已知:KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2,还生成CO2、KHSO4等物质。写出该反应的化学方程式
您最近半年使用:0次
解题方法
6 . 从宏观和微观两个角度认识氯、硫、铁、铝等元素的单质及其化合物是学好中学化学的重要基础。完成下列填空:
(1)Cl在元素周期表中的位置为______________ ,由此可知,其最高价氧化物对应的水化物的化学式 为:______________ ,次氯酸分子的结构式为:_____________ 。
(2)Cl、S、Na三种元素形成简单离子其半径由大到小的顺序是_______________________ (用离子符号 表示)。铝最高价氧化物对应的水化物表现出了独特的性质,其在水溶液中的电离方程式 为____________________________________________________________________________ 。
(3)硫和氯的非金属性强弱关系是_________________ ,试从原子结构的角度解释其原因。______________
(4)现有试剂:溴水、硫化钠溶液、Na2SO3溶液、稀硫酸、NaOH溶液、氨水。 要证明Na2SO3具有还原 性,应选用的试剂有______________ ,看到的现象是 ____________________ 。要证明Na2SO3具有氧化性,应选用的试剂有___________________ ,反应的离子方程式是 ________________________________ 。
(1)Cl在元素周期表中的位置为
(2)Cl、S、Na三种元素形成简单离子其半径由大到小的顺序是
(3)硫和氯的非金属性强弱关系是
(4)现有试剂:溴水、硫化钠溶液、Na2SO3溶液、稀硫酸、NaOH溶液、氨水。 要证明Na2SO3具有还原 性,应选用的试剂有
您最近半年使用:0次
名校
解题方法
7 . 硫是生物必需的大量营养元素之一,下图是自然界中硫的循环图,请分析此图并回答有关问题。
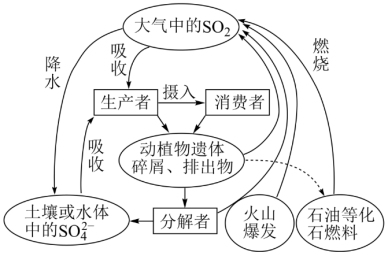
(1)氮循环和硫循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是________ 。
(2)分解者可将含硫有机物分解为H2S,硫磺细菌和硫化细菌可将H2S进一步变为硫单质或硫酸盐,下列关于硫化氢说法正确的是_______ 。
A.H2S分子很稳定,受热难分解
B. H2S分子中所有原子的最外层都达到8电子结构
C.将H2S通入FeSO4溶液,产生沉淀
D.H2S中硫元素为-2价,因此H2S只有还原性,没有氧化性
E.H2S是一种无色臭鸡蛋气味的有毒气体
(3)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。检验某次降雨是否为酸雨的方法是_________________ ,收集某次酸雨样品,发现8小时内,样品pH一直在减小,其原因可能是________________ 。(用化学方程式表示)
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是_______ (填化学式)。

(1)氮循环和硫循环是自然界中两种重要的元素循环过程,下列关于这两种循环的说法正确的是
| 选项 | 比较 | 氮循环 | 硫循环 |
| A | 异 | 氮元素会进入大气 | 硫元素不会进入大气 |
| B | 氮循环过程有生物圈参与 | 硫循环过程无生物圈参与 | |
| C | 同 | 人类活动对氮循环和硫循环都造成巨大影响 | |
| D | 氮循环和硫循环对环境的影响是都能导致温室效应 | ||
A.H2S分子很稳定,受热难分解
B. H2S分子中所有原子的最外层都达到8电子结构
C.将H2S通入FeSO4溶液,产生沉淀
D.H2S中硫元素为-2价,因此H2S只有还原性,没有氧化性
E.H2S是一种无色臭鸡蛋气味的有毒气体
(3)大气中的SO2经过一系列转化最终生成H2SO4,导致降水具有较强酸性,称为酸雨。检验某次降雨是否为酸雨的方法是
(4)为了防治酸雨,工业上常采用“钙基固硫法”即将生石灰和含硫的煤混合后燃烧,燃烧时硫、氧气和生石灰共同作用,使硫元素转移到炉渣中,大部分硫元素最终转化为固体盐是
您最近半年使用:0次
名校
解题方法
8 . 根据信息写方程式:
(1)Pb与C同主族,化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物,已知PbO2具有强氧化性,与浓盐酸共热可生成一种黄绿色气体。试写出Pb3O4与浓盐酸反应的化学方程式:__________________________________ 。
(2)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定度的I2溶液进行滴定,滴定反应的离子方程式为________________________________ 。
(3)向菱镁矿(主要成分为MgCO3,含少量FeCO3)中,首先加入稀硫酸,过滤后,再加入H2O2。写出加入H2O2氧化时发生反应的化学方程式:________________________________________ 。
(1)Pb与C同主族,化合价有+2价和+4价,PbO与PbO2是铅的两种常见氧化物,已知PbO2具有强氧化性,与浓盐酸共热可生成一种黄绿色气体。试写出Pb3O4与浓盐酸反应的化学方程式:
(2)利用I2的氧化性可测定钢铁中硫的含量。做法是将钢样中的硫转化成H2SO3,然后用一定度的I2溶液进行滴定,滴定反应的离子方程式为
(3)向菱镁矿(主要成分为MgCO3,含少量FeCO3)中,首先加入稀硫酸,过滤后,再加入H2O2。写出加入H2O2氧化时发生反应的化学方程式:
您最近半年使用:0次
2019高三·全国·专题练习
9 . 联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题:
联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是______ 。联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀。理论上1kg的联氨可除去水中溶解的O2____ kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 _______ 。
联氨是一种常用的还原剂。向装有少量AgBr的试管中加入联氨溶液,观察到的现象是
您最近半年使用:0次
名校
解题方法
10 . 氧化还原反应在生产、生活中具有广泛的用途。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是_____ (选填编号)。
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。
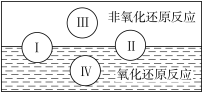
试写出有水参加且符合反应类型 IV 的一个化学方程式:___________________ 。
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
_____ NaIO3+ NaHSO3→ I2+ Na2SO4+ H2SO4+ H2O
②该反应还原剂是_____ ,_____ 元素被还原,若生成 1mol 氧化产物则转移电子数目为_____ NA。
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-_____ I-(填“>”或“<”),完成该反应_____________________________________ 。
(1)下列生产、生活中的事例中没有发生氧化还原反应的是
a. 海水提溴 b. 工业制氯碱 c. 海水晒盐 d. 海带提碘
(2)水是人体的重要组成部分,是人体中含量最多的一种物质。“四种基本反应类型与氧化还原反应的关”可用下图表示。

试写出有水参加且符合反应类型 IV 的一个化学方程式:
(3)工业上利用 NaIO3和 NaHSO3反应来制取单质 I2。
①配平下列化学方程式并标明电子转移的方向和数目:
②该反应还原剂是
(4)已知:HSO3-、I2、I-、SO42-和一些未知物组成的一个氧化还原反应,其中SO42-是氧化产物,该反应中还原性HSO3-
您最近半年使用:0次
2017-12-22更新
|
280次组卷
|
2卷引用:上海交通大学附属中学2017-2018学年高一12月月考化学试题



