名校
解题方法
1 . 化学与生活、生产和社会发展密切相关。下列说法正确的是
| A.医用口罩所用的熔喷布是一种聚丙烯材料,聚丙烯可以使溴水褪色 |
| B.用二氧化硅可以制成计算机、通信设备和家用电器等的芯片 |
C. 能将某些色素氧化褪色,可用作有色布匹的漂白剂 能将某些色素氧化褪色,可用作有色布匹的漂白剂 |
| D.液氨汽化时吸收大量热,可用作制冷剂 |
您最近一年使用:0次
2 . 某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣(已除去葡萄糖溶液过滤得到的),对甘蔗渣进行综合利用不仅可以提高经济效益,而且还能防止环境污染。生产流程如图所示。 的产量可以用来衡量一个国家石油化学工业的发展水平,
的产量可以用来衡量一个国家石油化学工业的发展水平, 的分子中含有醛基,
的分子中含有醛基, 是具有香味的液体。完成下列各题。
是具有香味的液体。完成下列各题。
(1)A的名称为___________ ; 的名称为
的名称为___________ 。
(2)B的结构简式为___________ ; 的结构简式为
的结构简式为___________ , 的官能团名称为
的官能团名称为___________ 。
(3)写出 的化学方程式:
的化学方程式:___________ 。
(4)写出 的化学方程式:
的化学方程式:___________ 。
(5)写出 的同分异构体中与
的同分异构体中与 互为同系物的结构简式:
互为同系物的结构简式:___________ 。

 的产量可以用来衡量一个国家石油化学工业的发展水平,
的产量可以用来衡量一个国家石油化学工业的发展水平, 的分子中含有醛基,
的分子中含有醛基, 是具有香味的液体。完成下列各题。
是具有香味的液体。完成下列各题。(1)A的名称为
 的名称为
的名称为(2)B的结构简式为
 的结构简式为
的结构简式为 的官能团名称为
的官能团名称为(3)写出
 的化学方程式:
的化学方程式:(4)写出
 的化学方程式:
的化学方程式:(5)写出
 的同分异构体中与
的同分异构体中与 互为同系物的结构简式:
互为同系物的结构简式:
您最近一年使用:0次
3 . 下列分离、提纯、鉴别物质的方法错误的是
A.用丁达尔效应鉴别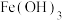 胶体和 胶体和 溶液 溶液 |
B.用溶解、过滤的方法除去 中的 中的 |
C.用加热方法除去 中的 中的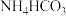 |
D.用加热、蒸发的方法除去粗盐中的 杂质 杂质 |
您最近一年使用:0次
4 . I.化学小组的同学用10mol/L的浓硫酸配制100mL物质的量浓度为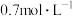 的稀硫酸,以备实验使用。
的稀硫酸,以备实验使用。
(1)需要量取________ mL上述浓硫酸进行配制。
(2)为配制上述稀硫酸,除了量筒、烧杯、胶头滴管外,还需用到的玻璃仪器是________ 。
(3)下列实验操作可能导致配制的硫酸溶液浓度偏高的是________ (填序号)。
a.定容时俯视观察
b.往容量瓶转移时,有少量液体溅出
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
II.化学小组同学通过实验探究某补铁药品中含亚铁盐,实验过程如下:
(4)取一定量药品溶于水,静置,过滤,得澄清溶液。
(5)甲同学取少量溶液,先加入2滴KSCN溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为________ 。
(6)乙同学也取少量溶液,滴加NaOH溶液,有沉淀生成;将其露置于空气中可观察到的现象是________ ;产生该现象原因是________________ (用化学方程式解释)。
(7)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是________ 。
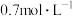 的稀硫酸,以备实验使用。
的稀硫酸,以备实验使用。(1)需要量取
(2)为配制上述稀硫酸,除了量筒、烧杯、胶头滴管外,还需用到的玻璃仪器是
(3)下列实验操作可能导致配制的硫酸溶液浓度偏高的是
a.定容时俯视观察
b.往容量瓶转移时,有少量液体溅出
c.浓硫酸在烧杯中加水稀释后,未冷却就向容量瓶中转移
d.定容后经振荡、摇匀、静置后,发现液面下降,再加适量的蒸馏水
II.化学小组同学通过实验探究某补铁药品中含亚铁盐,实验过程如下:
(4)取一定量药品溶于水,静置,过滤,得澄清溶液。
(5)甲同学取少量溶液,先加入2滴KSCN溶液,溶液无明显变化;再加入几滴新制氯水,溶液变红。氯水与亚铁盐反应的离子方程式为
(6)乙同学也取少量溶液,滴加NaOH溶液,有沉淀生成;将其露置于空气中可观察到的现象是
(7)丙同学取少量甲同学实验后的溶液,加入过量铁粉,溶液红色又消失。此实验能证明的是
您最近一年使用:0次
名校
解题方法
5 . 以 作催化剂,可用乙烯脱除烟气中
作催化剂,可用乙烯脱除烟气中 并回收单质硫。某兴趣小组同学设计实验验证该反应并检验产物中的
并回收单质硫。某兴趣小组同学设计实验验证该反应并检验产物中的 ,实验装置(夹持装置已略)如图所示:
,实验装置(夹持装置已略)如图所示:
回答下列问题:
(1)装置a中的作用是___________ 。(答出2点即可)
(2)装置b中有S、 、
、 生成,则发生反应的化学方程式为
生成,则发生反应的化学方程式为___________ 。
(3)装置c用冷水水浴的目的是___________ 。
(4)有同学认为可将溴水换成酸性高锰酸钾溶液,你认为是否可行,说明你的理由___________ 。
(5)装置e中品红溶液的作用是___________ 。
 作催化剂,可用乙烯脱除烟气中
作催化剂,可用乙烯脱除烟气中 并回收单质硫。某兴趣小组同学设计实验验证该反应并检验产物中的
并回收单质硫。某兴趣小组同学设计实验验证该反应并检验产物中的 ,实验装置(夹持装置已略)如图所示:
,实验装置(夹持装置已略)如图所示: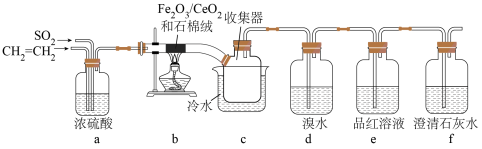
回答下列问题:
(1)装置a中的作用是
(2)装置b中有S、
 、
、 生成,则发生反应的化学方程式为
生成,则发生反应的化学方程式为(3)装置c用冷水水浴的目的是
(4)有同学认为可将溴水换成酸性高锰酸钾溶液,你认为是否可行,说明你的理由
(5)装置e中品红溶液的作用是
您最近一年使用:0次
名校
解题方法
6 . 下列各组物质:
① 和
和
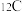 和
和
④ 和
和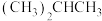
⑤癸烷和十六烷
⑥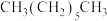 和
和
(1)互为同位素的是___________ 。
(2)互为同分异构体的是___________ 。
(3)互为同素异形体的是___________ 。
(4)互为同系物的是___________ 。
(5)同一种物质的是___________ 。
①
 和
和
②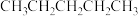 和
和
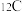 和
和
④
 和
和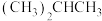
⑤癸烷和十六烷
⑥
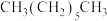 和
和
⑦ 和
和
(1)互为同位素的是
(2)互为同分异构体的是
(3)互为同素异形体的是
(4)互为同系物的是
(5)同一种物质的是
您最近一年使用:0次
名校
7 . X、Y、Z、W为原子半径依次增大的短周期p区元素,由四种元素形成的微粒Q可作为绿色催化剂和溶剂离子液体的阴离子,Q的结构如图所示下列说法正确的是

A.氢化物的沸点: |
B.电负性: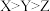 |
| C.W的氧化物对应的水化物属于强酸 |
| D.该阴离子中Y不满足8电子稳定结构 |
您最近一年使用:0次
名校
8 . 苯烯莫德是一种小分子药物,因可用于抑制多种自身免疫疾病而成为研究热点,其结构简式如图所示。下列说法正确的是

A.该有机物的分子式为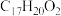 | B.苯环上的一溴代物有5种 |
| C.分子中所有碳原子可能处于同一平面 | D.完全氢化后所得产物中含有2个手性碳原子 |
您最近一年使用:0次
9 . 下列做法不可行的是
| A.用溴水鉴别辛烷和庚烷 |
| B.用水鉴别苯和四氯化碳 |
| C.通过燃烧法鉴别甲烷和乙炔 |
| D.向96%的乙醇溶液中加入生石灰再蒸馏制取无水乙醇 |
您最近一年使用:0次
名校
解题方法
10 . 研究化学反应的原理,对掌握物质的应用有重要的意义。
Ⅰ.某化学课外小组的同学通过铁和稀盐酸的反应探究外界条件对化学反应速率的影响,下农是实验过程中的数据及相关信息:
(注:气体体积均在相同条件下测得)
(1)实验①和②探究盐酸浓度对反应速率的影响,即V1为_______ mL;实验②和③探究_______ 对反应速率的影响。
(2)实验室在制氢气时,可在锌和盐酸反应的容器中加入少量硫酸铜固体,目的是_______ (用文字表达)。
(3)分析其中一组实验,发现产生氢气的速率随时间的变化情况都是开始速率慢慢增大,后来慢慢减小。前期速率慢慢增大的主要原因是_______ ,后期速率慢慢减小的主要原因是_______ 。
Ⅱ.研究NOx、SO2、CO等气体的无害化处理对治理大气污染、建设生态文明有重要意义。
(4)一定温度下,在恒容的密闭容器中充入lmolCO和2molH2,发生CO(g)+ 2H2(g) CH3OH(g),对于该反应,下列说法正确的是_______ (填序号)。
CH3OH(g),对于该反应,下列说法正确的是_______ (填序号)。
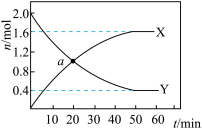
(5)利用反应2NO(g)+2CO(g) N2(g)+2CO2(g)、可实现汽车尾气的无害化处理。一定温度下,在体积为2L的恒容密闭容器中加入等物质的量的NO和CO,测得部分物质的物质的量随时间的变化如图所示。
N2(g)+2CO2(g)、可实现汽车尾气的无害化处理。一定温度下,在体积为2L的恒容密闭容器中加入等物质的量的NO和CO,测得部分物质的物质的量随时间的变化如图所示。
①X代表的物质是_______ ;a点正反应速率_______ 逆反应速率(填“>”、“<”或“=”)。_______ 。
Ⅰ.某化学课外小组的同学通过铁和稀盐酸的反应探究外界条件对化学反应速率的影响,下农是实验过程中的数据及相关信息:
| 序号 | 反应温度/℃ | c(HCl)/(mol/L) | V(HCl)/mL | V(H2O)/mL | 10gFe的形状 | t/min |
| ① | 20 | 2 | 5 | V1 | 块状 | 1 |
| ② | 20 | 2 | 10 | 0 | 块状 | 1 |
| ③ | 20 | 2 | 10 | 0 | 粉末 | 1 |
| ④ | 40 | 2 | 10 | 0 | 块状 | 1 |
(1)实验①和②探究盐酸浓度对反应速率的影响,即V1为
(2)实验室在制氢气时,可在锌和盐酸反应的容器中加入少量硫酸铜固体,目的是
(3)分析其中一组实验,发现产生氢气的速率随时间的变化情况都是开始速率慢慢增大,后来慢慢减小。前期速率慢慢增大的主要原因是
Ⅱ.研究NOx、SO2、CO等气体的无害化处理对治理大气污染、建设生态文明有重要意义。
(4)一定温度下,在恒容的密闭容器中充入lmolCO和2molH2,发生CO(g)+ 2H2(g)
 CH3OH(g),对于该反应,下列说法正确的是_______ (填序号)。
CH3OH(g),对于该反应,下列说法正确的是_______ (填序号)。| A.反应过程中n(CO)∶n(H2)不变 |
| B.(升高温度,正反应速率减小 |
| C.往容器中充入He,压强增大,反应速率加快 |
| D.容器内混合气体的平均摩尔质量保持不变时说明反应已达平衡 |
(5)利用反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)、可实现汽车尾气的无害化处理。一定温度下,在体积为2L的恒容密闭容器中加入等物质的量的NO和CO,测得部分物质的物质的量随时间的变化如图所示。
N2(g)+2CO2(g)、可实现汽车尾气的无害化处理。一定温度下,在体积为2L的恒容密闭容器中加入等物质的量的NO和CO,测得部分物质的物质的量随时间的变化如图所示。①X代表的物质是
您最近一年使用:0次



