1 . 回答下列问题
(1)乙醇的结构简式为___________ ,其官能团名称为___________ 。
(2)甲烷与乙烷互为___________ 。
(3)乙酸的结构简式为___________ ,其官能团名称为___________ 。
(1)乙醇的结构简式为
(2)甲烷与乙烷互为
(3)乙酸的结构简式为
您最近一年使用:0次
2 . 硼是第ⅢA族中唯一的非金属元素,可以形成众多的化合物。回答下列问题:
(1)硼烷泛指一切硼和氢组成的化合物。乙硼烷( )是最简单的硼烷,可以在
)是最简单的硼烷,可以在_______ (填“乙酸”或“乙醚”或“水”)介质中使用 还原
还原 获得,
获得, 的电子式为
的电子式为_______ ,制备乙硼烷的化学方程式为_______ 。 )的溶解度
)的溶解度
(2)操作1是蒸发浓缩、冷却结晶、过滤、_______ ,干燥;整个流程中可循环利用的物质是_______ 。
(3)硼酸( )是一元弱酸,在溶液中存在平衡:
)是一元弱酸,在溶液中存在平衡: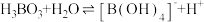 (常温下:
(常温下: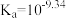 ),
), 与NaOH溶液反应可制备硼砂。常温下,在
与NaOH溶液反应可制备硼砂。常温下,在 硼砂溶液中,
硼砂溶液中,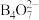 水解生成等物质的量浓度的
水解生成等物质的量浓度的 和
和 ,该溶液pH=
,该溶液pH=_______ 。常温常压下,硼酸( )晶体结构为层状,其二维平面结构如图所示:
)晶体结构为层状,其二维平面结构如图所示:_______ 。
(4)相关化学键的键能如下表所示,简要分析和解释下列事实。
自然界中不存在硼单质,硼氢化物也很少,主要是含氧化合物,其原因为_______ 。
(1)硼烷泛指一切硼和氢组成的化合物。乙硼烷(
 )是最简单的硼烷,可以在
)是最简单的硼烷,可以在 还原
还原 获得,
获得, 的电子式为
的电子式为
 )的溶解度
)的溶解度| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 80 |
| 溶解度/g | 2.77 | 3.65 | 4.87 | 6.77 | 8.90 | 23.54 |
(2)操作1是蒸发浓缩、冷却结晶、过滤、
(3)硼酸(
 )是一元弱酸,在溶液中存在平衡:
)是一元弱酸,在溶液中存在平衡: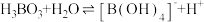 (常温下:
(常温下: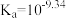 ),
), 与NaOH溶液反应可制备硼砂。常温下,在
与NaOH溶液反应可制备硼砂。常温下,在 硼砂溶液中,
硼砂溶液中,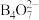 水解生成等物质的量浓度的
水解生成等物质的量浓度的 和
和 ,该溶液pH=
,该溶液pH= )晶体结构为层状,其二维平面结构如图所示:
)晶体结构为层状,其二维平面结构如图所示: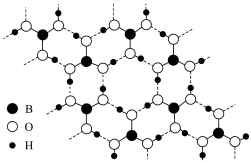
H3BO3的层状结构
从氢键的角度解释硼酸在冷水中的溶解度小而加热时溶解度增大的原因:(4)相关化学键的键能如下表所示,简要分析和解释下列事实。
| 化学键 |  |  |  |
键能( ) ) | 389 | 561 | 293 |
您最近一年使用:0次
3 . 在工业流程题中常使用 作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对
作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对 与Mn+的反应情况进行了以下探究:
与Mn+的反应情况进行了以下探究:
已知:①Ca2++2 =CaCO3↓+CO2↑+H2O K1=5×104
=CaCO3↓+CO2↑+H2O K1=5×104
②Ca2++2 =Ca(OH)2↓+2CO2↑ K2=1×10-10
=Ca(OH)2↓+2CO2↑ K2=1×10-10
③Cu2++2 =CuCO3↓+CO2↑+H2O K3=8×106
=CuCO3↓+CO2↑+H2O K3=8×106
④Cu2++2 =Cu(OH)2↓+2CO2↑ K4=3×104
=Cu(OH)2↓+2CO2↑ K4=3×104
下列关于该探究实验的叙述正确的是
 作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对
作为沉淀剂沉淀Fe2+/Mn2+/Co2+等金属离子,为了证实这一结论,对 与Mn+的反应情况进行了以下探究:
与Mn+的反应情况进行了以下探究:| 操作 | 现象 | |
| 1 | 0.5mol·L-1CaCl2溶液与NaHCO3溶液混合 | 产生气泡,生成白色沉淀 |
| 2 | 0.5mol·L-1CuCl2溶液与NaHCO3溶液混合 | 产生气泡,生成蓝色沉淀 |
| 3 | 0.5mol·L-1FeCl3溶液与NaHCO3溶液混合 | 产生大量气泡,生成红褐色沉淀 |
| 4 | 取2中的蓝色沉淀加热并将产物依次通过无水CuSO4和澄清石灰水 | 无水CuSO4变蓝,澄清石灰水变浑浊 |
 =CaCO3↓+CO2↑+H2O K1=5×104
=CaCO3↓+CO2↑+H2O K1=5×104②Ca2++2
 =Ca(OH)2↓+2CO2↑ K2=1×10-10
=Ca(OH)2↓+2CO2↑ K2=1×10-10③Cu2++2
 =CuCO3↓+CO2↑+H2O K3=8×106
=CuCO3↓+CO2↑+H2O K3=8×106④Cu2++2
 =Cu(OH)2↓+2CO2↑ K4=3×104
=Cu(OH)2↓+2CO2↑ K4=3×104下列关于该探究实验的叙述正确的是
| A.实验1生成的沉淀为Ca(OH)2 |
| B.实验2生成的沉淀为Cu(OH)2 |
C. 与M2+反应生成MCO3沉淀的离子方程式为M2++ 与M2+反应生成MCO3沉淀的离子方程式为M2++ =MCO3↓+H+ =MCO3↓+H+ |
D.实验3发生反应的离子方程式为Fe3++3 =Fe(OH)3↓+3CO2↑ =Fe(OH)3↓+3CO2↑ |
您最近一年使用:0次
名校
解题方法
4 . 化学创造美好生活。下列应用实例与所述的化学知识没有关联的是
| 选项 | 应用实例 | 化学知识 |
| A | 利用聚苯乙烯制作泡沫包装材料 | 聚苯乙烯燃烧生成 和 和 |
| B | 用 作潜水艇中的供氧剂 作潜水艇中的供氧剂 |  与 与 或 或 反应生成 反应生成 |
| C | 将液态植物油制成人造奶油 | 液态植物油能与 发生加成反应 发生加成反应 |
| D | 从海带灰中提取碘单质 | 海带灰中的 可被氧化 可被氧化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-05-12更新
|
785次组卷
|
2卷引用:2024届黑龙江省哈尔滨市第九中学高三下学期第四次模拟考试化学试卷
名校
解题方法
5 .  经催化加氢可以生成低碳有机物,实现
经催化加氢可以生成低碳有机物,实现 的综合利用和“碳达峰、碳中和”的目标。
的综合利用和“碳达峰、碳中和”的目标。 合成甲醇涉及以下三个反应:
合成甲醇涉及以下三个反应:
①

②

③

已知:反应①、③是低温条件的自发反应。回答下列问题:
(1)上述三个反应的平衡常数 与温度关系如图1所示。图1中c线表示的反应是
与温度关系如图1所示。图1中c线表示的反应是___________ (填“①”、“②”或“③”),
___________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。 加氢制甲醇反应机理如图2所示。
加氢制甲醇反应机理如图2所示。___________ (填字母)。
A.羧基物种 和甲酸盐物种
和甲酸盐物种 为两种中间体
为两种中间体
B.该反应使用的催化剂既加快了反应速率,又提高了 的平衡转化率
的平衡转化率
C.反应过程中有极性键和非极性键的断裂和形成
(3)某温度下,向一恒容密闭容器中充入等物质的量的 和
和 ,在催化剂作用下发生反应③并达到平衡状态。下列图像正确的是
,在催化剂作用下发生反应③并达到平衡状态。下列图像正确的是___________ (填字母)。 和
和 )
)
(4)在密闭容器中,充入 和
和 合成
合成 ,发生反应①和②。不同温度下达到平衡时
,发生反应①和②。不同温度下达到平衡时 、
、 及
及 的体积分数如图3所示。
的体积分数如图3所示。 ,则曲线a代表
,则曲线a代表___________ 。
② 时,
时, 的平衡转化率为
的平衡转化率为___________ (保留两位有效数字,下同),此温度下反应②的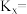
___________ (用平衡物质的量分数代替平衡浓度计算)。
 经催化加氢可以生成低碳有机物,实现
经催化加氢可以生成低碳有机物,实现 的综合利用和“碳达峰、碳中和”的目标。
的综合利用和“碳达峰、碳中和”的目标。 合成甲醇涉及以下三个反应:
合成甲醇涉及以下三个反应:①


②


③


已知:反应①、③是低温条件的自发反应。回答下列问题:
(1)上述三个反应的平衡常数
 与温度关系如图1所示。图1中c线表示的反应是
与温度关系如图1所示。图1中c线表示的反应是
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。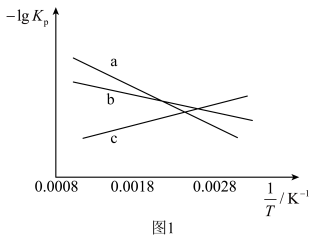
 加氢制甲醇反应机理如图2所示。
加氢制甲醇反应机理如图2所示。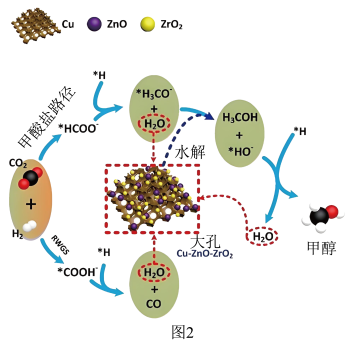
A.羧基物种
 和甲酸盐物种
和甲酸盐物种 为两种中间体
为两种中间体B.该反应使用的催化剂既加快了反应速率,又提高了
 的平衡转化率
的平衡转化率C.反应过程中有极性键和非极性键的断裂和形成
(3)某温度下,向一恒容密闭容器中充入等物质的量的
 和
和 ,在催化剂作用下发生反应③并达到平衡状态。下列图像正确的是
,在催化剂作用下发生反应③并达到平衡状态。下列图像正确的是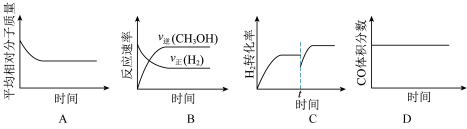
 和
和 )
)(4)在密闭容器中,充入
 和
和 合成
合成 ,发生反应①和②。不同温度下达到平衡时
,发生反应①和②。不同温度下达到平衡时 、
、 及
及 的体积分数如图3所示。
的体积分数如图3所示。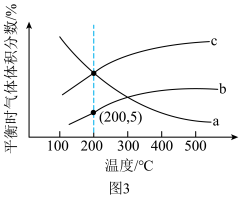
 ,则曲线a代表
,则曲线a代表②
 时,
时, 的平衡转化率为
的平衡转化率为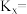
您最近一年使用:0次
2024-05-11更新
|
297次组卷
|
2卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
名校
6 . 苏沃雷生 是一种新型抗失眠药物,利用手性催化剂合成H的路线如图:
是一种新型抗失眠药物,利用手性催化剂合成H的路线如图:
(1)H中含氧官能团的名称为___________ 。
(2)C的结构简式为___________ 。
(3) 的反应类型为
的反应类型为___________ 。
(4) 的化学方程式为
的化学方程式为___________ 。
(5)G的结构简式为___________ 。
(6)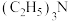 是一种有机碱,名称为三乙胺。
是一种有机碱,名称为三乙胺。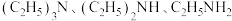 三者中碱性最弱的是
三者中碱性最弱的是___________ (填化学式)。
(7)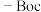 为叔丁氧羰基
为叔丁氧羰基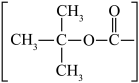 ,
,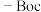 与
与 相连形成物质M。
相连形成物质M。
①写出满足下列条件的M的所有同分异构体的结构简式___________ 。
i.含四元环
ii.核磁共振氢谱显示只有一组吸收峰
②满足下列条件的M的同分异构体有___________ 种(不考虑立体结构)。
i.含酮羰基
ii.能与金属钠反应
iii.分子中只含有一个手性碳原子
 是一种新型抗失眠药物,利用手性催化剂合成H的路线如图:
是一种新型抗失眠药物,利用手性催化剂合成H的路线如图:
(1)H中含氧官能团的名称为
(2)C的结构简式为
(3)
 的反应类型为
的反应类型为(4)
 的化学方程式为
的化学方程式为(5)G的结构简式为
(6)
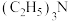 是一种有机碱,名称为三乙胺。
是一种有机碱,名称为三乙胺。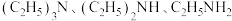 三者中碱性最弱的是
三者中碱性最弱的是(7)
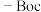 为叔丁氧羰基
为叔丁氧羰基 ,
,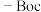 与
与 相连形成物质M。
相连形成物质M。①写出满足下列条件的M的所有同分异构体的结构简式
i.含四元环
ii.核磁共振氢谱显示只有一组吸收峰
②满足下列条件的M的同分异构体有
i.含酮羰基
ii.能与金属钠反应
iii.分子中只含有一个手性碳原子
您最近一年使用:0次
2024-05-11更新
|
334次组卷
|
2卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
名校
7 . 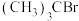 在碱性条件下水解生成
在碱性条件下水解生成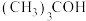 ,进程中势能变化如图。下列说法错误的是
,进程中势能变化如图。下列说法错误的是
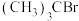 在碱性条件下水解生成
在碱性条件下水解生成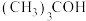 ,进程中势能变化如图。下列说法错误的是
,进程中势能变化如图。下列说法错误的是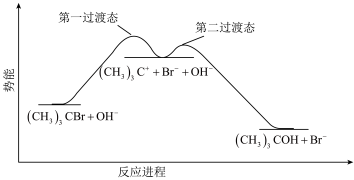
A.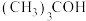 名称为2-甲基-2-丙醇 名称为2-甲基-2-丙醇 |
B. 中碳原子的杂化轨道类型有两种 中碳原子的杂化轨道类型有两种 |
C.增大 浓度,水解反应速率变化不大 浓度,水解反应速率变化不大 |
| D.升温既能加快反应速率又能促进平衡正向移动 |
您最近一年使用:0次
2024-05-11更新
|
312次组卷
|
2卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
名校
8 . 尼龙6是电子电器、军工、铁路、汽车、纺织、农业配件等领域的重要应用材料,一种合成尼龙6的路线如图。下列说法错误的是

| A.化合物甲能发生加成、氧化和取代反应 |
| B.化合物乙和化合物丙互为同分异构体 |
| C.此路线中各物质的氮原子杂化轨道类型均相同 |
| D.若某尼龙6的平均相对分子质量为12448,则平均聚合度约为110 |
您最近一年使用:0次
2024-05-11更新
|
403次组卷
|
2卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
名校
9 . 以下类比结论中正确的是
A. 的沸点高于 的沸点高于 ,则 ,则 的沸点高于 的沸点高于 |
B. 分子结构为直线形,则 分子结构为直线形,则 分子结构也是直线形 分子结构也是直线形 |
C. 能与 能与 溶液发生反应,则 溶液发生反应,则 也能与 也能与 溶液发生反应 溶液发生反应 |
D. 用作耐火材料,则 用作耐火材料,则 也可用作耐火材料 也可用作耐火材料 |
您最近一年使用:0次
2024-05-11更新
|
296次组卷
|
2卷引用:2024届黑龙江省哈尔滨师范大学附属中学高三下学期三模化学试题
名校
10 . 中国科学技术大学化学与材料科学学院报道了由胍阳离子和硼酸盐阴离子([B(OCH3)4]3[C(NH2)3]4Cl·4CH3OH)构成的离子型氢键有机骨架在室温下对甲醇的可逆自动吸附/解吸,其中[C(NH2)3]+为平面结构。下列说法正确的是
| A.基态原子半径:O<N<B |
| B.第二电离能:B<C |
| C.晶体中B、C和O原子轨道的杂化类型相同 |
| D.该晶体中存在配位键、离子键、氢键等化学键 |
您最近一年使用:0次



