名校
1 . 下列各组离子,能在水溶液中大量共存的是
A.H+、Na+、Cl-、HCO | B.SO 、K+、Na+、Ba2+ 、K+、Na+、Ba2+ |
C.Ag+、NO 、Na+、Cl- 、Na+、Cl- | D.Cl-、K+、Na+、SO |
您最近一年使用:0次
名校
2 . 已知实验室常用二氧化锰粉末和浓盐酸制取氯气,其反应的化学方程式为: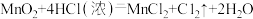 ,某实验小组用下图所示装置制取纯净干燥的氯气。
,某实验小组用下图所示装置制取纯净干燥的氯气。
(1)B是除杂装置,盛放的试剂是___________ (填“饱和食盐水”或“饱和NaHCO3溶液”);
(2)C装置利用了浓硫酸的___________ (填“吸水性”“脱水性”或“强氧化性”);
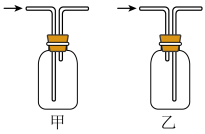
(3)D处是排空气法收集氯气的装置,应选用___________ (填“甲”或“乙”);___________ 。
(5)欲制取2.24L标准状况下的Cl2,至少需要MnO2的质量为___________ g。
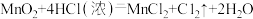 ,某实验小组用下图所示装置制取纯净干燥的氯气。
,某实验小组用下图所示装置制取纯净干燥的氯气。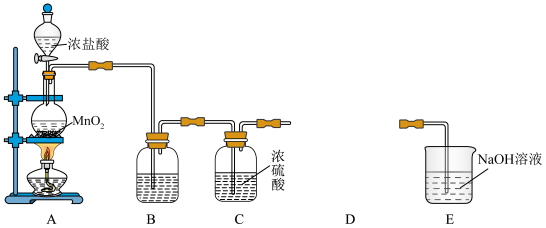
(1)B是除杂装置,盛放的试剂是
(2)C装置利用了浓硫酸的
(3)D处是排空气法收集氯气的装置,应选用
(5)欲制取2.24L标准状况下的Cl2,至少需要MnO2的质量为
您最近一年使用:0次
名校
3 . 非金属元素在生产生活中扮演着重要角色。请根据题意填空:
(1)浓硫酸是一种重要的化工原料,在浓硫酸的运输过程中,可选择___________ (填“铁”或“铜”)作为罐体材料。
(2)浓硫酸能使蔗糖变黑,体现出的性质为___________ (填“吸水性”或“脱水性”或“氧化性”),并膨胀、产生大量CO2、SO2气体,可用___________ (填“品红溶液”或“石蕊溶液”或“澄清石灰水”)检验SO2。
(1)浓硫酸是一种重要的化工原料,在浓硫酸的运输过程中,可选择
(2)浓硫酸能使蔗糖变黑,体现出的性质为
您最近一年使用:0次
4 . I.某同学设计了利用废铁屑制取硫酸亚铁晶体的简单流程如下:
(1)操作a是___________ ;
(2)“酸浸”时的离子反应方程式是___________ 。
Ⅱ.一定温度下,在容积为2L的密闭容器中发生N、M、P三种气体间的转化反应,M、N、P的物质的量随时间变化的曲线如图所示:___________ ;
(4)1-3min这段时间内,以M的浓度变化表示的平均反应速率为___________ ;
(5)平衡时N的转化率为___________ 。
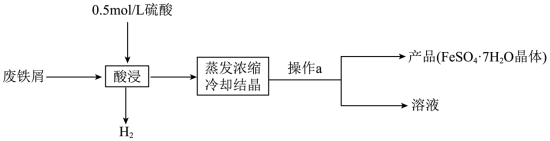
(1)操作a是
(2)“酸浸”时的离子反应方程式是
Ⅱ.一定温度下,在容积为2L的密闭容器中发生N、M、P三种气体间的转化反应,M、N、P的物质的量随时间变化的曲线如图所示:
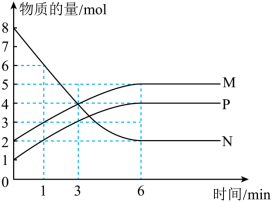
(4)1-3min这段时间内,以M的浓度变化表示的平均反应速率为
(5)平衡时N的转化率为
您最近一年使用:0次
5 . 下列行为中符合安全要求的是
| A.用水浇灭由金属钠引起的火灾 |
| B.节日期间,在开阔的广场燃放烟花爆竹 |
| C.用点燃的火柴在液化气钢瓶口检验是否漏气 |
| D.实验时,将水倒入浓硫酸中配制稀硫酸 |
您最近一年使用:0次
名校
6 . 下表是元素周期表的一部分,表中的每个编号表示一种元素,请根据要求回答下列问题。
(1)⑥号元素的原子结构示意图为___________ ;
(2)最高价氧化物对应水化物碱性最强的是___________ (填化学式);
(3)氢化物热稳定性最强的是___________ (填电子式);
(4)③④⑤的原子半径从大到小的顺序是___________ (填元素符号)。
| 族 周期 | ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ② | ③ | ④ | ||||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | |||||
(2)最高价氧化物对应水化物碱性最强的是
(3)氢化物热稳定性最强的是
(4)③④⑤的原子半径从大到小的顺序是
您最近一年使用:0次
名校
7 . 下列关于物质的量的叙述正确的是
| A.40g NaOH固体溶解在1L水中,所得溶液的物质的量浓度为1mol/L |
| B.标准状况下,22.4L H2O的质量约为18g |
| C.0.5mol Na2SO4中含有Na+的物质的量为1mol |
| D.1mol/L KOH溶液中含有6.02×1023个OH- |
您最近一年使用:0次
8 . 某抗氧化剂Z可由如图反应制得:
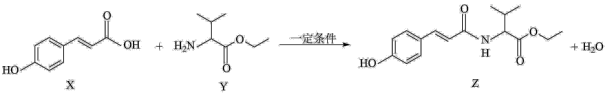
| A.Y中元素的电负性:O>C>H |
| B.X和Y均含有1个手性碳原子 |
| C.X可以发生加聚反应,也可以发生缩聚反应 |
D.一定条件下,1mol Z与足量 水溶液反应,最多消耗3mol 水溶液反应,最多消耗3mol |
您最近一年使用:0次
名校
9 . 2020年9月22日,中国政府在第75届联合国大会上提出:“中国将提高国家自主贡献力度,采取更有力的政策和措施。二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。” 碳中和也叫碳补偿(Carbon Offset),是现代人为减缓全球变暖所作的努力之一。碳中和的实现方式包括两种:一是通过植树造林等方式增加CO2的吸收量,二是通过技术手段减少CO2的排放量。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g) ⇌ CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)⇌ CO(g)+H2O(g) △H1=+41kJ·mol-1
②CO(g)+2H2(g) ⇌ CH3OH(g) △H2= —99kJ·mol-1
(1)总反应的
_______ kJ·mol-1;
(2)氢氧燃料电池具有启动快,效率高等优点,若电解质为酸性,氢氧燃料电池的正极反应为_______
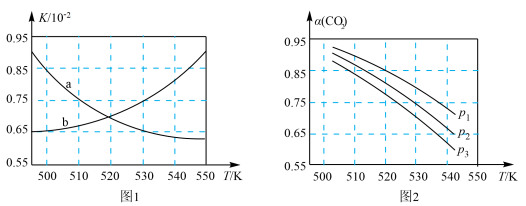
(3)图1中能正确反映平衡常数K随温度变化关系的曲线为_______ (填曲线标记字母),体系中的CO2平衡转化率(a)与温度和压强的关系如图2所示,则图2中的压强由大到小为_______ 。_______ (用含a的式子表示)。
Ⅱ. 和
和 的催化重整对温室气体的减排具有重要意义,其反应为:
的催化重整对温室气体的减排具有重要意义,其反应为: 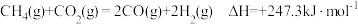 。回答下列问题:
。回答下列问题:
(5)该反应体系的熵值变化为_______ (填“增加”或“减小”);根据公式△G=△H—T△S判断:此反应在_______ (填“低温”或“高温”)条件下可以自发进行。
(6)其它条件相同,在不同催化剂(A、B)作用下,反应 进行相同时间后,
进行相同时间后, 的产率随反应温度的变化如图3所示。
的产率随反应温度的变化如图3所示。_______ ,在催化剂A、B作用下,它们反应活化能分别用 、
、 表示,则
表示,则
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(7)将原料 和
和 按等物质的量充入密闭容器中,保持体系压强为
按等物质的量充入密闭容器中,保持体系压强为 发生反应:
发生反应: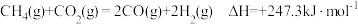 。达到平衡时,
。达到平衡时, 体积分数与温度的关系如图4所示,则在
体积分数与温度的关系如图4所示,则在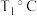 、
、 下,达平衡时
下,达平衡时 转化率=
转化率=_______ 。
Ⅰ.二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g) ⇌ CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)⇌ CO(g)+H2O(g) △H1=+41kJ·mol-1
②CO(g)+2H2(g) ⇌ CH3OH(g) △H2= —99kJ·mol-1
(1)总反应的

(2)氢氧燃料电池具有启动快,效率高等优点,若电解质为酸性,氢氧燃料电池的正极反应为
(3)图1中能正确反映平衡常数K随温度变化关系的曲线为
Ⅱ.
 和
和 的催化重整对温室气体的减排具有重要意义,其反应为:
的催化重整对温室气体的减排具有重要意义,其反应为: 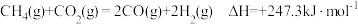 。回答下列问题:
。回答下列问题:(5)该反应体系的熵值变化为
(6)其它条件相同,在不同催化剂(A、B)作用下,反应
 进行相同时间后,
进行相同时间后, 的产率随反应温度的变化如图3所示。
的产率随反应温度的变化如图3所示。 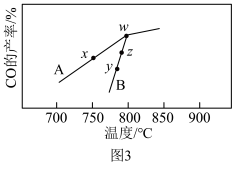
 、
、 表示,则
表示,则
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(7)将原料
 和
和 按等物质的量充入密闭容器中,保持体系压强为
按等物质的量充入密闭容器中,保持体系压强为 发生反应:
发生反应: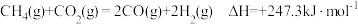 。达到平衡时,
。达到平衡时, 体积分数与温度的关系如图4所示,则在
体积分数与温度的关系如图4所示,则在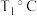 、
、 下,达平衡时
下,达平衡时 转化率=
转化率=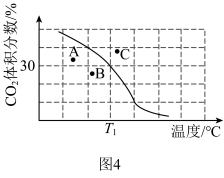
您最近一年使用:0次
名校
解题方法
10 . 下列离子方程式正确的是
A.向Na2SiO3溶液中通入过量CO2: |
B.将等物质的量浓度的 和NH4HSO4溶液以体积比 和NH4HSO4溶液以体积比 混合: 混合: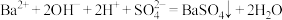 |
C.FeO溶于稀HNO3溶液: |
D.向AlCl3溶液中滴加过量NaOH溶液: |
您最近一年使用:0次
7日内更新
|
256次组卷
|
2卷引用:湖南省名校联考联合体2023-2024学年高一下学期5月期中联合考试化学试题



