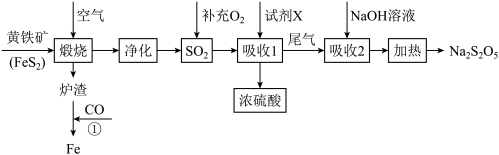
1 . 以黄铁矿(主要成分FeS2)为原料生产硫酸,并将产出的炉渣和尾气进行资源综合利用,减轻对环境的污染,其中一种流程如图所示。
已知:S2O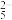 与Ba2+反应生成沉淀,与盐酸反应生成SO2。
与Ba2+反应生成沉淀,与盐酸反应生成SO2。
(1)Na2S2O5中硫元素的化合价为______ 。
(2)煅烧时主要发生的反应为4FeS2+11O2 2Fe2O3+8SO2,则反应①化学方程式为
2Fe2O3+8SO2,则反应①化学方程式为______ 。
(3)试剂X是______ 。
(4)尾气中某种气体可用品红溶液检验,则该气体是______ ,利用了该气体______ (填性质)。
(5)吸收2后得NaHSO3溶液,加热后得Na2S2O5和水,写出加热反应的化学方程式______ 。
(6)Na2S2O5在保存过程中易变质生成Na2SO4。欲检验Na2S2O5是否变质的实验方法为:______ 。
(7)环保部门为了测定某硫酸厂周围空气中的SO2含量进行了如下实验。取标准状况下1.000L空气(含N2、O2、CO2、SO2)。在所得溶液中通入过量的H2S气体,至不再产生黄色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为0.096g。则空气样品中SO2的体积分数为______ 。

已知:S2O
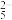 与Ba2+反应生成沉淀,与盐酸反应生成SO2。
与Ba2+反应生成沉淀,与盐酸反应生成SO2。(1)Na2S2O5中硫元素的化合价为
(2)煅烧时主要发生的反应为4FeS2+11O2
 2Fe2O3+8SO2,则反应①化学方程式为
2Fe2O3+8SO2,则反应①化学方程式为(3)试剂X是
(4)尾气中某种气体可用品红溶液检验,则该气体是
(5)吸收2后得NaHSO3溶液,加热后得Na2S2O5和水,写出加热反应的化学方程式
(6)Na2S2O5在保存过程中易变质生成Na2SO4。欲检验Na2S2O5是否变质的实验方法为:
(7)环保部门为了测定某硫酸厂周围空气中的SO2含量进行了如下实验。取标准状况下1.000L空气(含N2、O2、CO2、SO2)。在所得溶液中通入过量的H2S气体,至不再产生黄色沉淀,过滤后将沉淀洗涤、干燥,称得其质量为0.096g。则空气样品中SO2的体积分数为
您最近一年使用:0次
2 . I.用下图装置制取SO2并验证SO2的某些性质。回答下列问题:
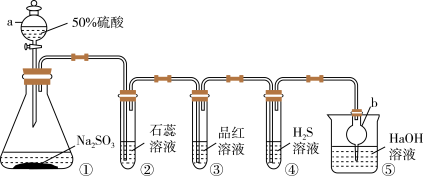
(1)仪器a的名称是___________ ,仪器b的作用是___________ ;
(2)装置②中的实验现象是___________ 。反应结束后,对装置③的试管加热可观察到的现象是___________ ;
(3)装置④中发生反应的化学方程式为___________ ,在该反应中氧化产物与还原产物物质的量之比为___________ ;
(4)SO2可用于杀菌、消毒。葡萄酒里含有微量SO2,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了SO2的___________ 性。氯水和SO2都有漂白性,有人为增强漂白效果,将Cl2和SO2混合使用,结果适得其反,几乎没有漂白效果,用离子方程式表示其原因:___________ 。
Ⅱ.完成下列问题
(5)实验室需配制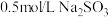 溶液230mL,现需要用托盘天平称取
溶液230mL,现需要用托盘天平称取 晶体
晶体___________ g,配制溶液所用到的玻璃仪器有:玻璃棒、烧杯、量筒和___________ 。
(6)配置过程中所用蒸馏水需煮沸、冷却后才能使用,煮沸蒸馏水的目的是___________ 。
(7)下列操作会使所配溶液浓度偏高的是___________。
(8) 放在空气中容易被氧化变质。检验
放在空气中容易被氧化变质。检验 溶液是否变质的方法是
溶液是否变质的方法是___________ 。

(1)仪器a的名称是
(2)装置②中的实验现象是
(3)装置④中发生反应的化学方程式为
(4)SO2可用于杀菌、消毒。葡萄酒里含有微量SO2,起保鲜、杀菌和抗氧化作用,其中抗氧化作用是利用了SO2的
Ⅱ.完成下列问题
(5)实验室需配制
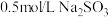 溶液230mL,现需要用托盘天平称取
溶液230mL,现需要用托盘天平称取 晶体
晶体(6)配置过程中所用蒸馏水需煮沸、冷却后才能使用,煮沸蒸馏水的目的是
(7)下列操作会使所配溶液浓度偏高的是___________。
| A.所选用的溶质已经失去部分结晶水 |
| B.转移溶液时玻璃棒靠在刻度线上方 |
| C.定容时俯视容量瓶的刻度线 |
| D.摇匀后溶液低于刻度线,再加入蒸馏水使液面最低点与刻度线相切 |
 放在空气中容易被氧化变质。检验
放在空气中容易被氧化变质。检验 溶液是否变质的方法是
溶液是否变质的方法是
您最近一年使用:0次
3 . 孔雀石是含铜的碳酸盐矿物,主要成分为 Cu2(OH)2CO3,工业上以孔雀石(主要杂质有FeCO3、FeO、SiO2)制备胆矾的一般流程如下:
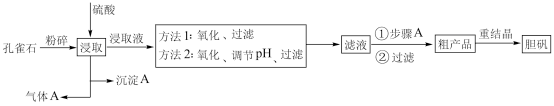
注:重结晶目的是为了除尽Fe3+
回答下列问题:
(1)写出气体A 的电子式______________ 。
(2)方法 1 的原理是用微酸性的高锰酸钾溶液将二价铁氧化为 Fe(OH)3,使之与 MnO2 共沉淀,易于过滤,除铁效果好,稍有过量,溶液即显微红色,便于掌握。稍过量的高锰酸钾会自动分解,产生 MnO2 和一种无毒的气体,请完善此反应的离子反应方程式:_____ MnO4- +________ H+ = __ MnO2↓ + ____ + _____
(3)方法 1 的不足之处是在酸性条件下会发生副反应__________________ (写出离子方程式),产物Mn2+进入溶液,需要后续步骤除去,同时 Fe3+水解也不易彻底。因而实际生产中更多采用的是方法 2,用过氧化氢作为氧化剂,优点是____ 。氧化后调节pH 沉淀出氢氧化铁,但需注意pH 不可过高,否则造成的影响是_____ 。
(4)若在实验室进行步骤A 操作,需要用到的硅酸盐仪器有_________________ 。
(5)CuSO4·5H2O 含量的测定:称取 0.5g 样品,溶于水,移入 100mL 容量瓶中,稀释至刻度,量取 25.00mL,稀释至 100mL,加入10mL 氨-氯化铵缓冲溶液(pH=10)及 0.2g 红紫酸铵混合指示剂,摇匀,用浓度为 cmol·L-1 EDTA 标准溶液滴定至溶液呈紫蓝色不变,重复三次,平均消耗的标准溶液体积为VmL。 (EDTA 能与大多数金属离子形成稳定的 1:1 络合物,是络合滴定中的常用滴定试剂)
①计算CuSO4·5H2O 质量分数______________ 。
②若不进行重结晶操作,计算出的质量分数结果会__________ 。(填偏低、偏高或者无影响)。

注:重结晶目的是为了除尽Fe3+
回答下列问题:
(1)写出气体A 的电子式
(2)方法 1 的原理是用微酸性的高锰酸钾溶液将二价铁氧化为 Fe(OH)3,使之与 MnO2 共沉淀,易于过滤,除铁效果好,稍有过量,溶液即显微红色,便于掌握。稍过量的高锰酸钾会自动分解,产生 MnO2 和一种无毒的气体,请完善此反应的离子反应方程式:
(3)方法 1 的不足之处是在酸性条件下会发生副反应
(4)若在实验室进行步骤A 操作,需要用到的硅酸盐仪器有
(5)CuSO4·5H2O 含量的测定:称取 0.5g 样品,溶于水,移入 100mL 容量瓶中,稀释至刻度,量取 25.00mL,稀释至 100mL,加入10mL 氨-氯化铵缓冲溶液(pH=10)及 0.2g 红紫酸铵混合指示剂,摇匀,用浓度为 cmol·L-1 EDTA 标准溶液滴定至溶液呈紫蓝色不变,重复三次,平均消耗的标准溶液体积为VmL。 (EDTA 能与大多数金属离子形成稳定的 1:1 络合物,是络合滴定中的常用滴定试剂)
①计算CuSO4·5H2O 质量分数
②若不进行重结晶操作,计算出的质量分数结果会
您最近一年使用:0次



