解题方法
1 .  具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为
具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为 、
、 ,含少量
,含少量 、
、 、
、 和其他不溶于酸、碱的杂质)为原料制备纳米
和其他不溶于酸、碱的杂质)为原料制备纳米 的流程如下。已知:
的流程如下。已知: 熔点高,硬度大,不溶于酸、碱;常温下,
熔点高,硬度大,不溶于酸、碱;常温下, 、
、 、
、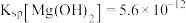 ;溶液中离子的浓度小于
;溶液中离子的浓度小于 时可视为该离子沉淀完全。请回答下列问题:
时可视为该离子沉淀完全。请回答下列问题:___________ ;加入 的目的是
的目的是___________ 。
(2)滤渣1的主要成分为___________ 、___________ 及不溶于酸、碱的杂质;加入 调节溶液的
调节溶液的 为13后,溶液中的
为13后,溶液中的
___________ 。
(3)若通入过量 ,发生的主要反应的离子方程式为
,发生的主要反应的离子方程式为___________ 。
(4)写出洗去固体A表面杂质的简要操作:___________ 。
(5)“煅烧”固体A反应的化学方程式为___________ 。
 具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为
具有耐高温的惰性,高活性,可广泛应用于制作各种塑料、橡胶、陶瓷、耐火材料等。工业上以油页岩灰渣(主要成分为 、
、 ,含少量
,含少量 、
、 、
、 和其他不溶于酸、碱的杂质)为原料制备纳米
和其他不溶于酸、碱的杂质)为原料制备纳米 的流程如下。已知:
的流程如下。已知: 熔点高,硬度大,不溶于酸、碱;常温下,
熔点高,硬度大,不溶于酸、碱;常温下, 、
、 、
、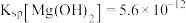 ;溶液中离子的浓度小于
;溶液中离子的浓度小于 时可视为该离子沉淀完全。请回答下列问题:
时可视为该离子沉淀完全。请回答下列问题:
 的目的是
的目的是(2)滤渣1的主要成分为
 调节溶液的
调节溶液的 为13后,溶液中的
为13后,溶液中的
(3)若通入过量
 ,发生的主要反应的离子方程式为
,发生的主要反应的离子方程式为(4)写出洗去固体A表面杂质的简要操作:
(5)“煅烧”固体A反应的化学方程式为
您最近一年使用:0次
2024-04-25更新
|
195次组卷
|
3卷引用:2024届陕西省榆林市高三上学期第一次模拟检测理综试题-高中化学
解题方法
2 . 氨基甲酸铵是一种有机化合物,化学式为 ,为白色固体,易分解,易水解,是化学工业中尿素生产过程的中间产物,也用于医药氨化剂。利用如图所示的装置制备氨基甲酸铵并测定其在室温下(25℃)分解的分压平衡常数。
,为白色固体,易分解,易水解,是化学工业中尿素生产过程的中间产物,也用于医药氨化剂。利用如图所示的装置制备氨基甲酸铵并测定其在室温下(25℃)分解的分压平衡常数。
已知: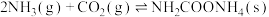
 ,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则容易发生副反应生成无机盐。
,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则容易发生副反应生成无机盐。
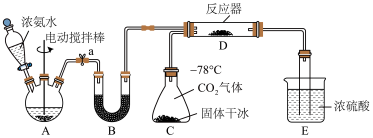
I.制备氨基甲酸铵,部分实验装置如图所示:_______ 。
(2)装置A和B中装有相同的固体,则该固体为_______ 。
(3)若缺少装置B,反应器中可能发生的副反应的化学方程式为_______ 。
(4)装置E中浓硫酸的作用为_______ 。
II.测定室温下(25℃)氨基甲酸铵分解的分压平衡常数:
①将氨基甲酸铵装入球泡中,调整旋塞位于d位置,调节恒温槽温度为25℃,将E处接至真空泵,打开K,降低体系内压强,利用水银压差计测得初始状态的压强为 ,关闭K。
,关闭K。
②达到分解平衡时,利用水银压差计测得体系内压强为 。
。
③反应结束后,调节旋塞的位置,然后E处接真空泵,经洗气瓶和干燥剂抽出氨基甲酸铵的分解产物。
(5)实验步骤③中调节旋塞位置为_______ (填“a”、“b”、“c”或“d”)。
(6)根据实验测得数据计算氨基甲酸铵固体分解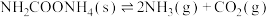 的分压平衡常数为
的分压平衡常数为_______ 。
(7)达到分解平衡时,氨基甲酸铵应有少量剩余,若实验结束时发现无固体剩余,可能会对结果产生影响,分析原因:_______ 。
 ,为白色固体,易分解,易水解,是化学工业中尿素生产过程的中间产物,也用于医药氨化剂。利用如图所示的装置制备氨基甲酸铵并测定其在室温下(25℃)分解的分压平衡常数。
,为白色固体,易分解,易水解,是化学工业中尿素生产过程的中间产物,也用于医药氨化剂。利用如图所示的装置制备氨基甲酸铵并测定其在室温下(25℃)分解的分压平衡常数。已知:
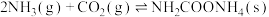
 ,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则容易发生副反应生成无机盐。
,该反应在干燥条件下仅生成氨基甲酸铵,若有水存在则容易发生副反应生成无机盐。I.制备氨基甲酸铵,部分实验装置如图所示:
(2)装置A和B中装有相同的固体,则该固体为
(3)若缺少装置B,反应器中可能发生的副反应的化学方程式为
(4)装置E中浓硫酸的作用为
II.测定室温下(25℃)氨基甲酸铵分解的分压平衡常数:

①将氨基甲酸铵装入球泡中,调整旋塞位于d位置,调节恒温槽温度为25℃,将E处接至真空泵,打开K,降低体系内压强,利用水银压差计测得初始状态的压强为
 ,关闭K。
,关闭K。②达到分解平衡时,利用水银压差计测得体系内压强为
 。
。③反应结束后,调节旋塞的位置,然后E处接真空泵,经洗气瓶和干燥剂抽出氨基甲酸铵的分解产物。
(5)实验步骤③中调节旋塞位置为
(6)根据实验测得数据计算氨基甲酸铵固体分解
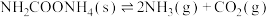 的分压平衡常数为
的分压平衡常数为(7)达到分解平衡时,氨基甲酸铵应有少量剩余,若实验结束时发现无固体剩余,可能会对结果产生影响,分析原因:
您最近一年使用:0次
3 . 锡是“五金”之一,无论在工业生产还是日常生活中都发挥着举足轻重的作用。我国有丰富的锡矿,黄锡矿是目前已发现的具有工业意义的锡矿物之一、工业上用黄锡矿(主要含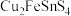 )为原料制备高纯度
)为原料制备高纯度 的工艺流程如图所示(部分条件和产物省略):
的工艺流程如图所示(部分条件和产物省略): 、
、 ,二价锡易被氧化;
,二价锡易被氧化;
② 常温下为无色液体,熔点
常温下为无色液体,熔点 ℃,沸点114℃;
℃,沸点114℃;
③ 极易水解,在潮湿的空气中出现“发烟”现象的同时又生成
极易水解,在潮湿的空气中出现“发烟”现象的同时又生成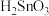 ;
;
④ :
: ,
, ;
; :
: ,
, 。
。
回答下列问题:
(1)“煅烧炉”中矿粉和空气逆流,以及将金属锡熔融,冷却制成锡花,其共同的目的是_______ 。
(2)工业上通常用足量的纯碱溶液吸收“煅烧炉”中产生的气体,写出该反应的离子方程式:_______ 。
(3)若“锡花”或 未完全干燥则会出现“发烟”现象,相关反应的化学方程式为
未完全干燥则会出现“发烟”现象,相关反应的化学方程式为_______ 。
(4)反应釜中需加入适当过量的Sn,其作用有_______ ;反应完成后加浓盐酸的目的是_______ 。
(5)上述流程中“系列操作”包含_______ 。
(6)某化学小组通过下列方法测定所用“熔融锡”的纯度(杂质不参与反应):
①将试样溶于足量稀硫酸,发生反应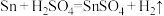 ;
;
②加入过量 溶液充分反应;
溶液充分反应;
③用已知浓度的 溶液滴定②中生成的
溶液滴定②中生成的 。
。
步骤③滴定过程中达到滴定终点的现象为_______ ;取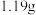 锡粉,经上述各步反应后,共用去
锡粉,经上述各步反应后,共用去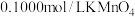 溶液
溶液 ,锡粉中锡的质量分数为
,锡粉中锡的质量分数为_______ 。
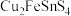 )为原料制备高纯度
)为原料制备高纯度 的工艺流程如图所示(部分条件和产物省略):
的工艺流程如图所示(部分条件和产物省略):
 、
、 ,二价锡易被氧化;
,二价锡易被氧化;②
 常温下为无色液体,熔点
常温下为无色液体,熔点 ℃,沸点114℃;
℃,沸点114℃;③
 极易水解,在潮湿的空气中出现“发烟”现象的同时又生成
极易水解,在潮湿的空气中出现“发烟”现象的同时又生成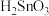 ;
;④
 :
: ,
, ;
; :
: ,
, 。
。回答下列问题:
(1)“煅烧炉”中矿粉和空气逆流,以及将金属锡熔融,冷却制成锡花,其共同的目的是
(2)工业上通常用足量的纯碱溶液吸收“煅烧炉”中产生的气体,写出该反应的离子方程式:
(3)若“锡花”或
 未完全干燥则会出现“发烟”现象,相关反应的化学方程式为
未完全干燥则会出现“发烟”现象,相关反应的化学方程式为(4)反应釜中需加入适当过量的Sn,其作用有
(5)上述流程中“系列操作”包含
(6)某化学小组通过下列方法测定所用“熔融锡”的纯度(杂质不参与反应):
①将试样溶于足量稀硫酸,发生反应
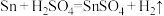 ;
;②加入过量
 溶液充分反应;
溶液充分反应;③用已知浓度的
 溶液滴定②中生成的
溶液滴定②中生成的 。
。步骤③滴定过程中达到滴定终点的现象为
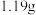 锡粉,经上述各步反应后,共用去
锡粉,经上述各步反应后,共用去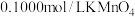 溶液
溶液 ,锡粉中锡的质量分数为
,锡粉中锡的质量分数为
您最近一年使用:0次
4 . 西安是首批国家历史文化名城,历史上有13个朝代在此建都,是世界四大古都之一,不仅拥有厚重的历史,同时也展现着现代大都市的活力和浪漫。下列说法错误的是
| A.半坡出土的“人面鱼纹彩陶盆”是新石器时代仰韶文化的遗物,该陶盆的材料属于传统无机非金属材料 |
| B.西安城墙又称西安明城墙,是中国现存规模最大、保存最完整的古代城垣,城垣上青灰色砖瓦的颜色主要是因为其中含有氧化铁 |
| C.大唐芙蓉园的灯光秀吸引着中外游客,激光灯柱透过空气呈现着优美的图案,同时也体现着胶体的性质——丁达尔效应 |
| D.“长安塔”位于西安世界园艺博览会园区制高点小终南山上,采用了大量钢材结构、玻璃和不锈钢,其中不锈钢、钢材均属于金属材料 |
您最近一年使用:0次
解题方法
5 . 铋酸钠( ,难溶于水)是一种新型光催化剂,也被广泛应用于制药业。以辉铋矿(主要成分为
,难溶于水)是一种新型光催化剂,也被广泛应用于制药业。以辉铋矿(主要成分为 ,含
,含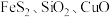 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图。
的工艺流程如图。
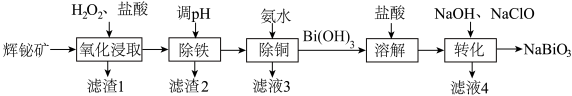
已知:“氧化浸取”时,铋元素转化为 ,硫元素转化为硫单质。回答下列问题:
,硫元素转化为硫单质。回答下列问题:
(1) 中铋元素的化合价为
中铋元素的化合价为___________ 价;“氧化浸取”时温度不能过高的原因是___________ ;“氧化浸取”时 发生反应的化学方程式为
发生反应的化学方程式为___________ 。
(2)“滤渣1”的主要成分为硫单质和___________ (写化学式)。
(3)“除铜”时,发生反应 ,该反应的平衡常数
,该反应的平衡常数
___________ 。{已知
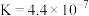 }
}
(4)在酸性介质中, 可将
可将 氧化为
氧化为 ,反应后
,反应后 元素呈
元素呈 价,则向足量稀硫酸和
价,则向足量稀硫酸和 稀溶液的混合溶液中加入
稀溶液的混合溶液中加入 时,反应中n(氧化剂):n(还原剂)=
时,反应中n(氧化剂):n(还原剂)=___________ 。
(5)“转化”时生成 反应的离子方程式为
反应的离子方程式为___________ 。
 ,难溶于水)是一种新型光催化剂,也被广泛应用于制药业。以辉铋矿(主要成分为
,难溶于水)是一种新型光催化剂,也被广泛应用于制药业。以辉铋矿(主要成分为 ,含
,含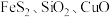 等杂质)为原料制备
等杂质)为原料制备 的工艺流程如图。
的工艺流程如图。
已知:“氧化浸取”时,铋元素转化为
 ,硫元素转化为硫单质。回答下列问题:
,硫元素转化为硫单质。回答下列问题:(1)
 中铋元素的化合价为
中铋元素的化合价为 发生反应的化学方程式为
发生反应的化学方程式为(2)“滤渣1”的主要成分为硫单质和
(3)“除铜”时,发生反应
 ,该反应的平衡常数
,该反应的平衡常数

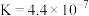 }
}(4)在酸性介质中,
 可将
可将 氧化为
氧化为 ,反应后
,反应后 元素呈
元素呈 价,则向足量稀硫酸和
价,则向足量稀硫酸和 稀溶液的混合溶液中加入
稀溶液的混合溶液中加入 时,反应中n(氧化剂):n(还原剂)=
时,反应中n(氧化剂):n(还原剂)=(5)“转化”时生成
 反应的离子方程式为
反应的离子方程式为
您最近一年使用:0次
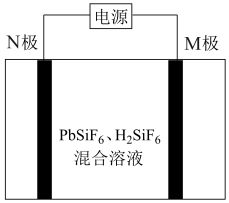
6 . 工业上用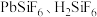 ;混合溶液作电解液,用电解法实现粗铅(主要杂质为
;混合溶液作电解液,用电解法实现粗铅(主要杂质为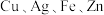 ,杂质总质量分数约为4%)提纯,装置示意图如图所示,M极附近析出金属单质。下列说法错误的是
,杂质总质量分数约为4%)提纯,装置示意图如图所示,M极附近析出金属单质。下列说法错误的是
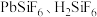 ;混合溶液作电解液,用电解法实现粗铅(主要杂质为
;混合溶液作电解液,用电解法实现粗铅(主要杂质为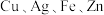 ,杂质总质量分数约为4%)提纯,装置示意图如图所示,M极附近析出金属单质。下列说法错误的是
,杂质总质量分数约为4%)提纯,装置示意图如图所示,M极附近析出金属单质。下列说法错误的是
| A.M极与电源的负极相连 | B.电子由M极流出,经电源流回N极 |
C.N极发生的电极反应之一为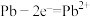 | D.工作一段时间后,溶液中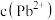 减小 减小 |
您最近一年使用:0次
7 . 化学与生产、科技、生活密切相关,下列说法错误的是
A.月壤中富含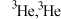 是 是 元素的一种核素 元素的一种核素 |
| B.用于食品保鲜袋中作干燥剂的二氧化硅气凝胶可产生丁达尔效应 |
| C.利用高温加热方式灭活细菌或病毒制取灭活疫苗的过程,与蛋白质变性有关 |
| D.战斗机的隐身涂层中含石墨烯,石墨烯是一种有机高分子材料 |
您最近一年使用:0次
解题方法
8 . 电化学原理在污染治理方面有着重要的作用。回答下列问题:
I.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示:
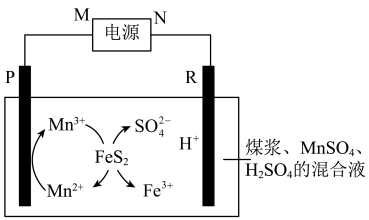
已知:两电极为完全相同的惰性电极。
(1)M为电源的___________ 极。
(2)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式___________ 。
(3)电解池工作时,混合液中 的物质的量
的物质的量___________ (填“变大”、“变小”或“不变”)。
(4)电解过程中,混合溶液中的pH将___________ (填“变大”、“变小”或“不变”),理由是___________ 。
II.电解还原法处理酸性含铬废水:以铁板做阴、阳极,电解含铬废水,示意如图:
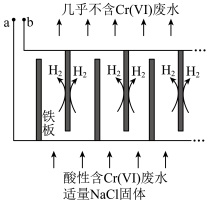
(5)酸性废水中的 在该电池中发生的离子反应方程式为
在该电池中发生的离子反应方程式为___________ 。
(6)为了使 和
和 转化为
转化为 和
和 沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中
沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中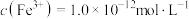 ,则溶液中
,则溶液中
___________  。{已知
。{已知 ,
,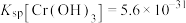 }
}
(7)随着电解的进行,阳极铁板会发生钝化,表面形成 的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:
的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:___________ 。
I.煤在直接燃烧前要进行脱硫处理。采用电解法脱硫的基本原理如图所示:

已知:两电极为完全相同的惰性电极。
(1)M为电源的
(2)电解池工作时,观察到R电极上有无色气体产生,写出电极反应式
(3)电解池工作时,混合液中
 的物质的量
的物质的量(4)电解过程中,混合溶液中的pH将
II.电解还原法处理酸性含铬废水:以铁板做阴、阳极,电解含铬废水,示意如图:

(5)酸性废水中的
 在该电池中发生的离子反应方程式为
在该电池中发生的离子反应方程式为(6)为了使
 和
和 转化为
转化为 和
和 沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中
沉淀,向反应后的溶液中加入一定量的烧碱,若溶液中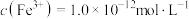 ,则溶液中
,则溶液中
 。{已知
。{已知 ,
,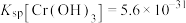 }
}(7)随着电解的进行,阳极铁板会发生钝化,表面形成
 的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:
的钝化膜,使电解池不能正常工作。将阴极铁板与阳极铁板交换使用,一段时间后,钝化膜消失,结合有关反应,解释钝化膜消失的原因:
您最近一年使用:0次
名校
解题方法
9 .  的综合利用成为研究热点,
的综合利用成为研究热点, 作为碳源加氢是再生能源的有效方法。回答下列问题:
作为碳源加氢是再生能源的有效方法。回答下列问题:
Ⅰ.工业上利用 和
和 制备
制备 ,已知温度为T、压强为p时的摩尔生成焓
,已知温度为T、压强为p时的摩尔生成焓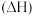 如表所示:
如表所示:
已知:一定温度下,由元素的最稳定单质生成 纯物质的热效应称为该物质的摩尔生成焓。
纯物质的热效应称为该物质的摩尔生成焓。
(1)温度为T、压强为p时,反应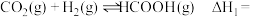
___________  。
。
(2)已知:温度为 时,
时,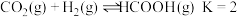 。实验测得:
。实验测得: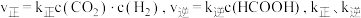 为速率常数。
为速率常数。
① 时,
时,
___________ 。
②若 时,
时,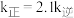 ,则
,则
___________ (填“>”“<”或“=”) 。
。
Ⅱ.在催化剂作用下, 可被氢气还原为甲醇:
可被氢气还原为甲醇: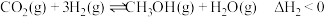 [同时有副反应
[同时有副反应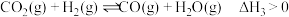 发生],
发生], 平衡转化率随温度和压强的变化如图。
平衡转化率随温度和压强的变化如图。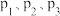 的大小关系:
的大小关系:___________ 。解释压强一定时, 的平衡转化率呈现如图变化的原因:
的平衡转化率呈现如图变化的原因:___________ 。同时增大 的平衡转化率和
的平衡转化率和 的产率可采取的措施是
的产率可采取的措施是___________ 。
(4)向压强为p的恒温恒压密闭容器中加入 和
和 ,进行反应,达到平衡状态时,
,进行反应,达到平衡状态时, 的转化率为20%,生成
的转化率为20%,生成 的物质的量为
的物质的量为 ,则甲醇的选择性为
,则甲醇的选择性为___________ %[甲醇选择性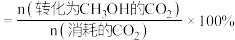 ];在该温度下,
];在该温度下, 的压强平衡常数
的压强平衡常数
___________ (列出计算式,分压=总压×物质的量分数)。
 的综合利用成为研究热点,
的综合利用成为研究热点, 作为碳源加氢是再生能源的有效方法。回答下列问题:
作为碳源加氢是再生能源的有效方法。回答下列问题:Ⅰ.工业上利用
 和
和 制备
制备 ,已知温度为T、压强为p时的摩尔生成焓
,已知温度为T、压强为p时的摩尔生成焓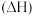 如表所示:
如表所示:| 气态物质 |  |  |  |
摩尔生成焓/ | 0 |  |  |
 纯物质的热效应称为该物质的摩尔生成焓。
纯物质的热效应称为该物质的摩尔生成焓。(1)温度为T、压强为p时,反应
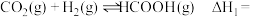
 。
。(2)已知:温度为
 时,
时,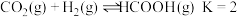 。实验测得:
。实验测得: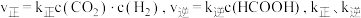 为速率常数。
为速率常数。①
 时,
时,
②若
 时,
时,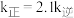 ,则
,则
 。
。Ⅱ.在催化剂作用下,
 可被氢气还原为甲醇:
可被氢气还原为甲醇: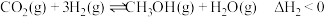 [同时有副反应
[同时有副反应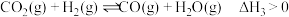 发生],
发生], 平衡转化率随温度和压强的变化如图。
平衡转化率随温度和压强的变化如图。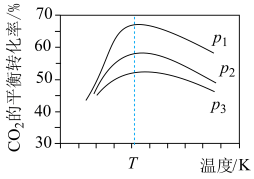
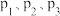 的大小关系:
的大小关系: 的平衡转化率呈现如图变化的原因:
的平衡转化率呈现如图变化的原因: 的平衡转化率和
的平衡转化率和 的产率可采取的措施是
的产率可采取的措施是(4)向压强为p的恒温恒压密闭容器中加入
 和
和 ,进行反应,达到平衡状态时,
,进行反应,达到平衡状态时, 的转化率为20%,生成
的转化率为20%,生成 的物质的量为
的物质的量为 ,则甲醇的选择性为
,则甲醇的选择性为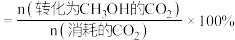 ];在该温度下,
];在该温度下, 的压强平衡常数
的压强平衡常数
您最近一年使用:0次
2024-04-01更新
|
521次组卷
|
5卷引用:2024届陕西省榆林市高三下学期第二次模拟检测理科综合试题-高中化学
2024届陕西省榆林市高三下学期第二次模拟检测理科综合试题-高中化学湖南省资兴市立中等多校联考2023-2024学年高二下学期3月月考化学试题(已下线)题型11 反应原理综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)2024届新疆名校联盟高三下学期第二次质量联合监测理科综合试题-高中化学江西省九校联考2023-2024学年高三下学期3月月考化学试题
10 . 合金是重要的金属材料。回答下列问题:
I.2023年5月,由中国自主研发的C919大型客机开启常态化商业运行。飞机上广泛应用了各种铝合金材料。
(1)铝合金和碳纤维复合材料是飞机、火箭的常用材料,这主要利用了它们具有的共同性能是___________ (填字母)。
A.密度小、强度好 B.密度大、硬度大 C.熔点低、硬度小
(2)铝的金属活动性比铁强,空气中铝却比铁具有更好的抗腐蚀性,原因是___________ 。
(3)起落架可用铝镁合金制造。合金焊接前需用碱洗,写出该过程发生的离子反应方程式___________ 。
II.某工厂合金废料的主要成分为 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该废料制取氯化铝、绿矾晶体(
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该废料制取氯化铝、绿矾晶体( )和胆矾晶体。
)和胆矾晶体。
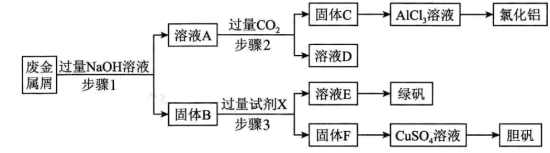
(4)试剂X是___________ ;固体F是___________ 。
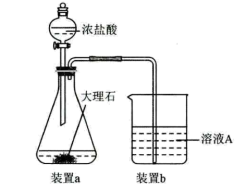
(5)在步骤2时,用如图装置制取 并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可在装置a和b间加一个盛有饱和
并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可在装置a和b间加一个盛有饱和___________ (填化学式)溶液的洗气瓶。
(6)溶液E中含有 ,生成该物质的原因是
,生成该物质的原因是___________ (用离子方程式表示)。
I.2023年5月,由中国自主研发的C919大型客机开启常态化商业运行。飞机上广泛应用了各种铝合金材料。
(1)铝合金和碳纤维复合材料是飞机、火箭的常用材料,这主要利用了它们具有的共同性能是
A.密度小、强度好 B.密度大、硬度大 C.熔点低、硬度小
(2)铝的金属活动性比铁强,空气中铝却比铁具有更好的抗腐蚀性,原因是
(3)起落架可用铝镁合金制造。合金焊接前需用碱洗,写出该过程发生的离子反应方程式
II.某工厂合金废料的主要成分为
 、
、 和
和 ,此外还含有少量
,此外还含有少量 和
和 ,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该废料制取氯化铝、绿矾晶体(
,为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用该废料制取氯化铝、绿矾晶体( )和胆矾晶体。
)和胆矾晶体。
(4)试剂X是
(5)在步骤2时,用如图装置制取
 并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可在装置a和b间加一个盛有饱和
并通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为避免固体C减少,可在装置a和b间加一个盛有饱和
(6)溶液E中含有
 ,生成该物质的原因是
,生成该物质的原因是
您最近一年使用:0次



