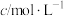1 . 铜、硫及其化合物在工业中用途广泛。请回答下列问题:
(1)基态铜原子的核外电子排布式为___________ 。
(2)硫酰氟 常温常压下为无色气体,固态
常温常压下为无色气体,固态 的晶体类型为
的晶体类型为___________ ,其F-S-F键角___________ (填“>”或“<”)硫酰氯 中的
中的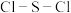 键角。
键角。
(3)硫酸四氨合铜晶体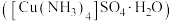 常用作杀虫剂、媒染剂。实验室制备
常用作杀虫剂、媒染剂。实验室制备 的流程如下:
的流程如下:
①写出过程 发生反应的离子方程式
发生反应的离子方程式___________ 。
②过程c加入 乙醇的作用是
乙醇的作用是___________ 。
③根据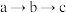 的现象,写出
的现象,写出 与
与 结合由弱到强的顺序
结合由弱到强的顺序___________ 。
(4)硫化铜的立方晶胞结构如图所示,已知 与
与 的核间距最小为
的核间距最小为 ,则该晶胞的棱长=
,则该晶胞的棱长=___________  (用含
(用含 的代数式表示)。
的代数式表示)。
(1)基态铜原子的核外电子排布式为
(2)硫酰氟
 常温常压下为无色气体,固态
常温常压下为无色气体,固态 的晶体类型为
的晶体类型为 中的
中的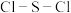 键角。
键角。(3)硫酸四氨合铜晶体
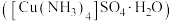 常用作杀虫剂、媒染剂。实验室制备
常用作杀虫剂、媒染剂。实验室制备 的流程如下:
的流程如下: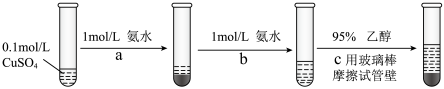
①写出过程
 发生反应的离子方程式
发生反应的离子方程式②过程c加入
 乙醇的作用是
乙醇的作用是③根据
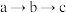 的现象,写出
的现象,写出 与
与 结合由弱到强的顺序
结合由弱到强的顺序(4)硫化铜的立方晶胞结构如图所示,已知
 与
与 的核间距最小为
的核间距最小为 ,则该晶胞的棱长=
,则该晶胞的棱长= (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解题方法
2 . 下列关于共价键说法错误的是
A.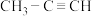 中碳碳三键中的碳原子为 中碳碳三键中的碳原子为 杂化,碳碳单键中的碳原子为 杂化,碳碳单键中的碳原子为 杂化 杂化 |
B.甲烷分子中的 键为 键为 键 键 |
C. 键是原子轨道“肩并肩”重叠, 键是原子轨道“肩并肩”重叠, 键是原子轨道“头碰头”重叠 键是原子轨道“头碰头”重叠 |
| D.成键原子间共用电子对偏移的程度越大,共价键极性越强,在反应中越容易发生断裂 |
您最近一年使用:0次
解题方法
3 . 化学与社会、生产及生活密切相关。下列叙述错误的是
| A.光(辐射)是电子跃迁释放能量的重要形式 |
| B.冬天雪花的形状体现了晶体的自范性 |
| C.金属晶体发生形变时,内部金属离子与“自由电子”的相互作用消失 |
D. 技术所需的LCP在一定加热状态下会变成液晶,其既有液体的流动性,又有类似晶体的各向异性 技术所需的LCP在一定加热状态下会变成液晶,其既有液体的流动性,又有类似晶体的各向异性 |
您最近一年使用:0次
名校
4 . 以下说法错误的是
| A.苯的邻二氯代物只有一种证明苯没有单双键交替的结构 |
| B.甲苯使高锰酸钾溶液褪色说明苯环对甲基有影响 |
C.CH3CHBrCH2CH3与 的醇溶液共热反应有机产物有2种(不考虑顺反异构) 的醇溶液共热反应有机产物有2种(不考虑顺反异构) |
| D.甲苯在一定条件下发生硝化反应产物只有TNT一种 |
您最近一年使用:0次
7日内更新
|
299次组卷
|
2卷引用:陕西省咸阳市武功县普集高级中学2023-2024学年高二下学期6月月考化学试题
名校
解题方法
5 . 为改变生橡胶受热发粘遇冷变硬的不良性能,工业上常将橡胶硫化来改善橡胶的性能, 和
和 均为改善橡胶性能的重要化工产品。
均为改善橡胶性能的重要化工产品。
Ⅰ.已知反应: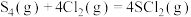 。下列为部分化学键的键能及
。下列为部分化学键的键能及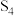 的结构式(键能是指化学键形成时放出的能量或化学键断裂时吸收的能量):
的结构式(键能是指化学键形成时放出的能量或化学键断裂时吸收的能量):
(1)则该反应是一个__________ (填“吸热”或“放热”)反应。
Ⅱ. 通常是一种金黄色液体,沸点为138 ℃,遇水反应生成S、
通常是一种金黄色液体,沸点为138 ℃,遇水反应生成S、 和HCl,热稳定性较差。实验室采用如下装置(加热和夹持仪器已略去)将氯气通入熔融硫黄(熔点为113 ℃)模拟工业生产
和HCl,热稳定性较差。实验室采用如下装置(加热和夹持仪器已略去)将氯气通入熔融硫黄(熔点为113 ℃)模拟工业生产 ,已知装置B的加热温度控制在140 ℃,回答下列问题:
,已知装置B的加热温度控制在140 ℃,回答下列问题:__________ ,A中发生的化学反应方程式为______________________________ 。
(3)装置接口从左到右的顺序为:a→__________ (填小写字母)。
(4)证明实验中有 生成的现象是
生成的现象是____________________ 。装置C中所装碱石灰的作用是____________________ 。
(5)实验结束时,装置B中烧瓶底部有少量硫附着,可用热的NaOH浓溶液洗涤,该反应的离子方程式为____________________ (产物为 和
和 )。
)。
(6)同学们联想到铁与硫单质也能反应。在空气中加热硫粉和铁粉的混合物,可观察到下列现象:
①有淡蓝色火焰,且生成刺激性气味的气体;
②混合物变红,放出热量,最后变成黑色固体;
③不时有火星从混合物中射出。
请写出产生现象②发生反应的化学方程式:________________________________ 。
 和
和 均为改善橡胶性能的重要化工产品。
均为改善橡胶性能的重要化工产品。Ⅰ.已知反应:
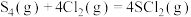 。下列为部分化学键的键能及
。下列为部分化学键的键能及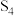 的结构式(键能是指化学键形成时放出的能量或化学键断裂时吸收的能量):
的结构式(键能是指化学键形成时放出的能量或化学键断裂时吸收的能量):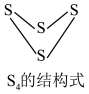
化学键 | S-S | S-Cl | Cl-Cl |
键能/(kJ/mol) | 266 | 255 | 243 |
(1)则该反应是一个
Ⅱ.
 通常是一种金黄色液体,沸点为138 ℃,遇水反应生成S、
通常是一种金黄色液体,沸点为138 ℃,遇水反应生成S、 和HCl,热稳定性较差。实验室采用如下装置(加热和夹持仪器已略去)将氯气通入熔融硫黄(熔点为113 ℃)模拟工业生产
和HCl,热稳定性较差。实验室采用如下装置(加热和夹持仪器已略去)将氯气通入熔融硫黄(熔点为113 ℃)模拟工业生产 ,已知装置B的加热温度控制在140 ℃,回答下列问题:
,已知装置B的加热温度控制在140 ℃,回答下列问题: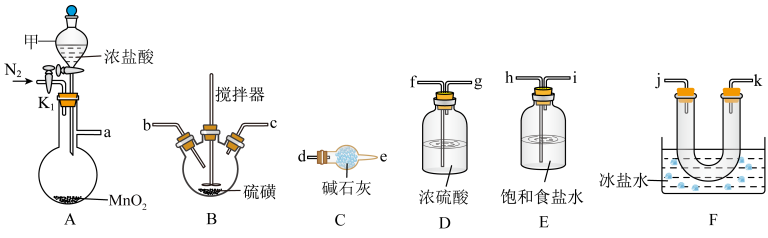
(3)装置接口从左到右的顺序为:a→
(4)证明实验中有
 生成的现象是
生成的现象是(5)实验结束时,装置B中烧瓶底部有少量硫附着,可用热的NaOH浓溶液洗涤,该反应的离子方程式为
 和
和 )。
)。(6)同学们联想到铁与硫单质也能反应。在空气中加热硫粉和铁粉的混合物,可观察到下列现象:
①有淡蓝色火焰,且生成刺激性气味的气体;
②混合物变红,放出热量,最后变成黑色固体;
③不时有火星从混合物中射出。
请写出产生现象②发生反应的化学方程式:
您最近一年使用:0次
名校
6 . 根据原电池原理,人们研制出了性能各异的化学电池。
(1)某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,如图所示:__________ 。负极材料是__________ ,负极反应式为____________________ 。
②该电池工作时,下列说法错误的是__________ (填字母)。
A.锌片的质量减小
B.电流由铜片经LED灯流向锌片
C.化学能全部转化为电能
D.发生了氧化还原反应
③若将锌片和铜片从柠檬中拿出,用蒸馏水洗净干燥后相互接触,LED灯__________ (填“会”或“不会”)亮,原因是____________________________________________________________ 。
(2)某锂-空气电池的总反应为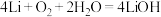 ,其工作原理示意图如图所示:
,其工作原理示意图如图所示: 发生
发生__________ (填“氧化”或“还原”)反应。
②锂离子向电池__________ (填“正”或“负”)极移动。
③石墨电极__________ (填“参与”或“不参与”)电极反应。
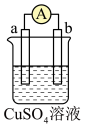
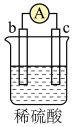
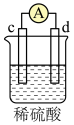
(3)现有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下表所示:
由上表可判断a、b、c、d四种金属的活动性由大到小排列为__________ (填字母)。
(1)某兴趣小组同学用大小相同的铜片和锌片作电极研究水果电池,如图所示:

②该电池工作时,下列说法错误的是
A.锌片的质量减小
B.电流由铜片经LED灯流向锌片
C.化学能全部转化为电能
D.发生了氧化还原反应
③若将锌片和铜片从柠檬中拿出,用蒸馏水洗净干燥后相互接触,LED灯
(2)某锂-空气电池的总反应为
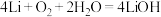 ,其工作原理示意图如图所示:
,其工作原理示意图如图所示:
 发生
发生②锂离子向电池
③石墨电极
(3)现有a、b、c、d四个金属电极,有关的实验装置及部分实验现象如下表所示:
实验装置 |
|
|
|
|
部分实验现象 | b极质量增大 | 外电路电流 从a流向d | c极上有气泡产生 | d极溶解 |
您最近一年使用:0次
名校
解题方法
7 . 蛋白质是生命活动的主要物质基础。下列说法错误的是
| A.蛋白质与氨基酸类似,也是两性分子 |
| B.加热牛奶和蛋清混合物制作双皮奶,该过程涉及蛋白质的变性 |
| C.食物中的蛋白质可在蛋白酶的作用下水解生成氨基酸 |
D.蛋白质中加入 溶液产生盐析现象 溶液产生盐析现象 |
您最近一年使用:0次
名校
解题方法
8 . 运用化学反应原理研究化学反应有重要的意义。请回答下列问题:
(1)工业上利用反应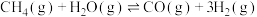 生产
生产 。一定温度下,向2 L恒容密闭容器中充入1.6 mol
。一定温度下,向2 L恒容密闭容器中充入1.6 mol  和2.4 mol
和2.4 mol  发生上述反应,CO(g)的物质的量随时间的变化如图所示:
发生上述反应,CO(g)的物质的量随时间的变化如图所示: =
=______  。
。
②下列不能说明上述反应达到平衡状态的是______ (填字母)。
A.恒温恒容时,容器内的总压强不随时间而变化
B.恒温恒容时,容器内混合气体的密度保持不变
C. 、CO(g)的浓度保持不变
、CO(g)的浓度保持不变
D.断开3mol H-H键的同时断开2 mol O-H键
(2)某研究性学习小组利用 溶液和硫酸的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
溶液和硫酸的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
【实验原理】
已知: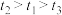 。请回答:
。请回答:
①配制0.1 的
的 溶液100 mL,需要的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
溶液100 mL,需要的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和______ 。
②实验过程使用了“控制变量法”,实验1、2探究的是 溶液浓度对反应速率的影响,则
溶液浓度对反应速率的影响,则 =
=______ ,得到的结论是____________ 。
③实验1、3探究的是温度对反应速率的影响,则 =
=______ ,得到的结论是____________ 。
④甲同学认为,也可通过排水法测量单位时间内产生气体体积的方法,来探究影响该反应速率的因素。你认为甲同学的方案是否可行?______ (填“可行”或“不可行”)理由是____________ 。
(1)工业上利用反应
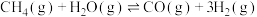 生产
生产 。一定温度下,向2 L恒容密闭容器中充入1.6 mol
。一定温度下,向2 L恒容密闭容器中充入1.6 mol  和2.4 mol
和2.4 mol  发生上述反应,CO(g)的物质的量随时间的变化如图所示:
发生上述反应,CO(g)的物质的量随时间的变化如图所示:
 =
= 。
。②下列不能说明上述反应达到平衡状态的是
A.恒温恒容时,容器内的总压强不随时间而变化
B.恒温恒容时,容器内混合气体的密度保持不变
C.
 、CO(g)的浓度保持不变
、CO(g)的浓度保持不变D.断开3mol H-H键的同时断开2 mol O-H键
(2)某研究性学习小组利用
 溶液和硫酸的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:
溶液和硫酸的反应探究“外界条件的改变对化学反应速率的影响”,进行了如下实验:【实验原理】

实验序号 | 实验温度/K | 有关物质 | 溶液变浑浊所需时间/s | ||||
|
|
| |||||
V/mL |
| V/mL |
| V/mL | |||
1 | 298 | 2 | 0.1 | 5 | 0.1 | 0 |
|
2 | 298 | 2 | 0.1 | 4 | 0.1 |
|
|
3 | 313 | 2 | 0.1 |
| 0.1 | 0 |
|
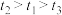 。请回答:
。请回答:①配制0.1
 的
的 溶液100 mL,需要的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和
溶液100 mL,需要的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管和②实验过程使用了“控制变量法”,实验1、2探究的是
 溶液浓度对反应速率的影响,则
溶液浓度对反应速率的影响,则 =
=③实验1、3探究的是温度对反应速率的影响,则
 =
=④甲同学认为,也可通过排水法测量单位时间内产生气体体积的方法,来探究影响该反应速率的因素。你认为甲同学的方案是否可行?
您最近一年使用:0次
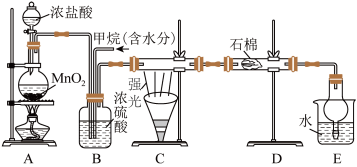
9 . 美国宇航局科学家确认火星大气中存在甲烷气体,可能来自火星火山活动或者生命活动,这一发现将为寻找火星生命带来希望。某课外活动小组利用如图所示装置探究烃类物质的性质,根据题意,回答下列问题:
Ⅰ.烷烃可以发生取代反应。向下图的A制取氯气,并向B中通入一定量的甲烷气体,于C处用强光照射硬质玻璃管。______ 。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③______ 。
(3)写出装置C中 与
与 反应生成氯仿的化学方程式
反应生成氯仿的化学方程式____________ 。
(4)装置D的石棉浸有足量 溶液,装置E中盛有
溶液,装置E中盛有 溶液,均用于除去尾气中的
溶液,均用于除去尾气中的 、
、 等,其中E中倒置球形干燥管的作用是
等,其中E中倒置球形干燥管的作用是______ 。
(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为______(选填编号)。
(6)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法______ (填“正确”或“不正确”),理由是______ 。
(7)实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应的化学方程式为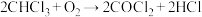 。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是______ 。
A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
Ⅱ.丙烯是三大合成材料的基本原料之一,其用量最大的是生产聚丙烯。
(8)丙烯能够使溴的四氯化碳溶液褪色,该反应的化学方程式为____________ 。
(9)聚丙烯(PP)可制成薄膜、包装材料等,丙烯在催化剂条件下合成聚丙烯的化学方程式是____________ 。
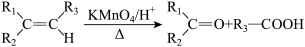
(10)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:______ 。
Ⅰ.烷烃可以发生取代反应。向下图的A制取氯气,并向B中通入一定量的甲烷气体,于C处用强光照射硬质玻璃管。
(2)B有三种功能:①控制气流速度;②混匀混合气体;③
(3)写出装置C中
 与
与 反应生成氯仿的化学方程式
反应生成氯仿的化学方程式(4)装置D的石棉浸有足量
 溶液,装置E中盛有
溶液,装置E中盛有 溶液,均用于除去尾气中的
溶液,均用于除去尾气中的 、
、 等,其中E中倒置球形干燥管的作用是
等,其中E中倒置球形干燥管的作用是(5)E中除盐酸外,还含有机物,从E中分离出盐酸的最佳方法为______(选填编号)。
| A.结晶法 | B.蒸馏法 | C.萃取分液法 | D.水洗分液法 |
(6)有人认为E中有氯化氢产生,不能证明甲烷与氯气发生了取代反应,你认为他的看法
(7)实验中生成的油状液滴中的氯仿可作局部麻醉剂,常因保存不慎而被空气氧化,产生剧毒气体——光气,反应的化学方程式为
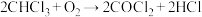 。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是
。为防止事故发生,在使用前检验氯仿是否变质可选用的试剂是A.氢氧化钠溶液 B.硝酸银溶液 C.稀盐酸 D.水
E.湿润的蓝色石蕊试纸 F.湿润的无色酚酞试纸
Ⅱ.丙烯是三大合成材料的基本原料之一,其用量最大的是生产聚丙烯。
(8)丙烯能够使溴的四氯化碳溶液褪色,该反应的化学方程式为
(9)聚丙烯(PP)可制成薄膜、包装材料等,丙烯在催化剂条件下合成聚丙烯的化学方程式是
(10)烯烃与酸性高锰酸钾溶液反应的氧化产物有如下的反应关系:
您最近一年使用:0次
名校
解题方法
10 . 完成下列问题。
(1)化学反应同时伴随着能量变化,是人类获取能量的重要途径。
A.镁与盐酸的反应 B.氢氧化钠与盐酸的反应 C.水的汽化 D.浓硫酸的稀释
E. 晶体与
晶体与 晶体的反应
晶体的反应
①以上变化过程,能用图a表示其能量变化的是___________ ,此类过程中有能量变化的原因是:断开反应物中的化学键需吸收的总能量___________ (填“大于”或“小于”)形成生成物中的化学键需释放的总能量。___________ 。
③拆开1mol共价键所吸收的能量或形成1mol共价键所释放的能量称为键能。已知H-H键能为436kJ/mol,H-N键能为391kJ/mol,N≡N键能为946kJ/mol。根据键能计算工业合成氨时消耗1molN2能___________ (填“吸收”或“放出”)___________ kJ热量。
(2)如图所示,是原电池的装置图。请回答: 设计成如图所示的原电池装置,则A极(负极)材料为
设计成如图所示的原电池装置,则A极(负极)材料为___________ ,B极电极反应式为___________ 。
②若C为 溶液,两电极材料分别为Zn和Cu,则Cu电极发生
溶液,两电极材料分别为Zn和Cu,则Cu电极发生___________ 反应,(填“氧化”或者“还原”),反应过程溶液中
___________ (填“变大”“变小”或“不变”)。
(3)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。___________ 。
②在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是___________ 。
(1)化学反应同时伴随着能量变化,是人类获取能量的重要途径。
A.镁与盐酸的反应 B.氢氧化钠与盐酸的反应 C.水的汽化 D.浓硫酸的稀释
E.
 晶体与
晶体与 晶体的反应
晶体的反应①以上变化过程,能用图a表示其能量变化的是

③拆开1mol共价键所吸收的能量或形成1mol共价键所释放的能量称为键能。已知H-H键能为436kJ/mol,H-N键能为391kJ/mol,N≡N键能为946kJ/mol。根据键能计算工业合成氨时消耗1molN2能
(2)如图所示,是原电池的装置图。请回答:

 设计成如图所示的原电池装置,则A极(负极)材料为
设计成如图所示的原电池装置,则A极(负极)材料为②若C为
 溶液,两电极材料分别为Zn和Cu,则Cu电极发生
溶液,两电极材料分别为Zn和Cu,则Cu电极发生
(3)以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。

②在电池反应中,每消耗1mol氧气,理论上生成标准状况下二氧化碳的体积是
您最近一年使用:0次


 溶液
溶液