1 . 一种稳定的水溶性(Co)配合物的结构简式如图(Ac表示 ),该分子可做催化剂,具有高氧态,可以促进水氧化,具有很好的发展前景。
),该分子可做催化剂,具有高氧态,可以促进水氧化,具有很好的发展前景。

回答下列问题:
(1)基态Co的价电子排布式为______ 。Co元素在元素周期表的位置为______ 。
(2)Na、K等金属在焰色试验中可以观察到焰色,Fe、Co等金属则观察不到焰色,请解释原因:______ 。
(3)关于如图所示的配合物,下列说法正确的是______(填标号)。
(4)Co可以形成多种配合物,一种配合物的化学式为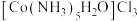 ,该配合物的配体为
,该配合物的配体为______ (填化学式),配位原子的杂化方式为______ 。
(5) 具有钙钛矿型结构,其晶胞结构如图所示,晶胞的另一种表示中Co原子处在各顶点位置,则F原子处于
具有钙钛矿型结构,其晶胞结构如图所示,晶胞的另一种表示中Co原子处在各顶点位置,则F原子处于______ 位置(填“顶点”“棱心”“面心”或“体心”)。已知 的晶体密度为
的晶体密度为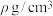 ),晶胞中两个相邻的F原子间的距离为a pm,则阿伏加德罗常数的
),晶胞中两个相邻的F原子间的距离为a pm,则阿伏加德罗常数的 可表示为
可表示为______  (填表达式)。
(填表达式)。

 ),该分子可做催化剂,具有高氧态,可以促进水氧化,具有很好的发展前景。
),该分子可做催化剂,具有高氧态,可以促进水氧化,具有很好的发展前景。
回答下列问题:
(1)基态Co的价电子排布式为
(2)Na、K等金属在焰色试验中可以观察到焰色,Fe、Co等金属则观察不到焰色,请解释原因:
(3)关于如图所示的配合物,下列说法正确的是______(填标号)。
| A.中心原子Co的配体数为6 |
| B.分子式中所含元素电负性最大的是O |
| C.分子中第二周期元素中第一电离能最大的是N |
| D.分子中2个六元环都是平面正六边形 |
(4)Co可以形成多种配合物,一种配合物的化学式为
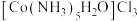 ,该配合物的配体为
,该配合物的配体为(5)
 具有钙钛矿型结构,其晶胞结构如图所示,晶胞的另一种表示中Co原子处在各顶点位置,则F原子处于
具有钙钛矿型结构,其晶胞结构如图所示,晶胞的另一种表示中Co原子处在各顶点位置,则F原子处于 的晶体密度为
的晶体密度为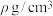 ),晶胞中两个相邻的F原子间的距离为a pm,则阿伏加德罗常数的
),晶胞中两个相邻的F原子间的距离为a pm,则阿伏加德罗常数的 可表示为
可表示为 (填表达式)。
(填表达式)。
您最近一年使用:0次
2024-05-11更新
|
71次组卷
|
2卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学
解题方法
2 . 下列说法不正确的是
| A.玻璃、水泥、陶瓷是三大传统的无机非金属材料 |
B.工业上用焦炭还原石英砂制取粗硅原理:SiO2+2C Si+2CO↑ Si+2CO↑ |
| C.海水淡化的方法主要有蒸馏法、电渗析法和离子交换法等 |
| D.绿色化学的核心思想就是先污染后用化学方法治理 |
您最近一年使用:0次
名校
解题方法
3 . W是一种抗肿瘤药物,其合成路线如下图所示,回答下列问题(部分反应条件已略去)。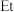 ”代表乙基;“
”代表乙基;“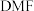 ”代表N,N—二甲基甲酰胺。
”代表N,N—二甲基甲酰胺。
(1)化合物A的分子式为___________ 。
(2)由D转化为E的反应类型为___________ ,化合物G中含氧官能团的名称为___________ 。
(3)化合物B中手性碳原子有___________ 个。
(4)写出由F生成G的化学方程式___________ 。
(5)A的同分异构体有多种,其中满足下列条件的同分异构体有___________ 种(考虑立体异构)。
①与A含有相同的官能团,“ ”与苯环直接相连 ②苯环上有2个取代基
”与苯环直接相连 ②苯环上有2个取代基
写出核磁共振氢谱有4组峰,且峰的面积之比为 的结构简式
的结构简式___________ 。
(6)写出 和
和 合成
合成 的路线(无机试剂任选)。
的路线(无机试剂任选)。_______
已知: 能与酯基反应;在
能与酯基反应;在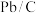 催化下,
催化下, 能将硝基转化为氨基。
能将硝基转化为氨基。

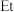 ”代表乙基;“
”代表乙基;“ ”代表N,N—二甲基甲酰胺。
”代表N,N—二甲基甲酰胺。(1)化合物A的分子式为
(2)由D转化为E的反应类型为
(3)化合物B中手性碳原子有
(4)写出由F生成G的化学方程式
(5)A的同分异构体有多种,其中满足下列条件的同分异构体有
①与A含有相同的官能团,“
 ”与苯环直接相连 ②苯环上有2个取代基
”与苯环直接相连 ②苯环上有2个取代基写出核磁共振氢谱有4组峰,且峰的面积之比为
 的结构简式
的结构简式(6)写出
 和
和 合成
合成 的路线(无机试剂任选)。
的路线(无机试剂任选)。已知:
 能与酯基反应;在
能与酯基反应;在 催化下,
催化下, 能将硝基转化为氨基。
能将硝基转化为氨基。
您最近一年使用:0次
2024-03-08更新
|
830次组卷
|
8卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学
陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学甘肃省张掖市某重点校2023-2024学年高三下学期模拟考化学试题(已下线)第三章 烃的衍生物(B卷)(已下线)大题预测卷01 (新高考通用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)(已下线)大题预测卷(江西专用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)陕西省西安工业大学附属中学2023-2024学年高三下学期3月月考理科综合试题-高中化学(已下线)化学(全国卷旧教材)-2024年高考押题预测卷2024届宁夏回族自治区石嘴山市平罗县平罗中学高三下学期模拟预测理综试题-高中化学
4 . 我国锰矿资源主要为贫碳酸锰矿(主要成分为 ,还含有少量
,还含有少量 、
、 、
、 、
、 、
、 、
、 ),利用贫碳酸锰矿制取
),利用贫碳酸锰矿制取 的流程如图所示,回答下列问题。
的流程如图所示,回答下列问题。 ,
, 。
。
(1) 中锰元素的价态有+2价和+3价,则下列表示
中锰元素的价态有+2价和+3价,则下列表示 组成的式子正确的是___________(填标号)。
组成的式子正确的是___________(填标号)。
(2)“滤渣1”的主要成分是___________ (填化学式)。
(3)“氧化”的目的是将 转化为
转化为 ,写出发生反应的离子方程式
,写出发生反应的离子方程式___________ ,检测 是否完全氧化的试剂是
是否完全氧化的试剂是___________ (写试剂名称)。
(4)“除钙镁”后的滤液中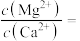
___________ 。
(5)“碳化”过程需要加热,但温度不能太高,试分析温度不能太高的原因___________ 。
(6)“焙烧”过程中随温度不同生成的锰的氧化物也不同。图中A点对应的氧化物是___________ ,为了获得 ,需要加热到
,需要加热到___________  (已知:A、B、C三点对应的物质均为纯净氧化物)。
(已知:A、B、C三点对应的物质均为纯净氧化物)。
 ,还含有少量
,还含有少量 、
、 、
、 、
、 、
、 、
、 ),利用贫碳酸锰矿制取
),利用贫碳酸锰矿制取 的流程如图所示,回答下列问题。
的流程如图所示,回答下列问题。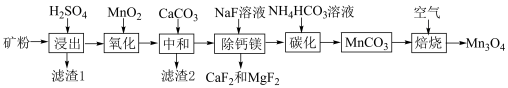
 ,
, 。
。(1)
 中锰元素的价态有+2价和+3价,则下列表示
中锰元素的价态有+2价和+3价,则下列表示 组成的式子正确的是___________(填标号)。
组成的式子正确的是___________(填标号)。A.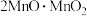 | B.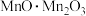 | C.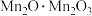 | D. |
(2)“滤渣1”的主要成分是
(3)“氧化”的目的是将
 转化为
转化为 ,写出发生反应的离子方程式
,写出发生反应的离子方程式 是否完全氧化的试剂是
是否完全氧化的试剂是(4)“除钙镁”后的滤液中
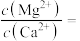
(5)“碳化”过程需要加热,但温度不能太高,试分析温度不能太高的原因
(6)“焙烧”过程中随温度不同生成的锰的氧化物也不同。图中A点对应的氧化物是
 ,需要加热到
,需要加热到 (已知:A、B、C三点对应的物质均为纯净氧化物)。
(已知:A、B、C三点对应的物质均为纯净氧化物)。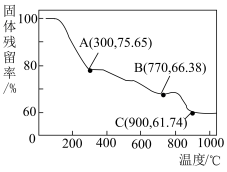
您最近一年使用:0次
2024-03-08更新
|
238次组卷
|
4卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学
陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学甘肃省张掖市某重点校2023-2024学年高三下学期模拟考化学试题(已下线)大题预测卷(黑龙江、吉林专用)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)陕西省西安工业大学附属中学2023-2024学年高三下学期3月月考理科综合试题-高中化学
名校
5 . 蚁酸甲酯是医药行业重要的原料,常利用 脱氢反应制取[
脱氢反应制取[ ],回答下列问题。
],回答下列问题。
(1)已知:①

②

③

则甲醇脱氢制蚁酸甲酯反应的
___________  。
。
(2)实际生产中还会发生副反应: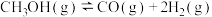
 。保持压强为
。保持压强为 制备蚁酸甲酯,各组分平衡物质的量分数随温度的变化如图所示。
制备蚁酸甲酯,各组分平衡物质的量分数随温度的变化如图所示。___________ 。
②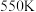 时,甲醇的平衡转化率为
时,甲醇的平衡转化率为___________  (小数点后保留1位数字),副反应的压强平衡常数
(小数点后保留1位数字),副反应的压强平衡常数
___________  (用包含
(用包含 的代数式表示)。
的代数式表示)。
(3)甲醇脱氢制蚁酸甲酯的反应机理如下(带“*”的物质表示自由基或原子, 和
和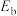 为活化能,
为活化能, 、
、 、
、 为平衡常数)。
为平衡常数)。
步骤1:


步骤2:

步骤3:
步骤4:

①利用量子力学模拟计算,发现步骤1还有可能发生反应:
 ,但实际检测发现生成的
,但实际检测发现生成的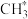 量很少,试分析其原因
量很少,试分析其原因___________ 。
②将步骤3发生的反应补充完整:________ 。
③反应 的平衡常数
的平衡常数
___________ (用包含 、
、 、
、 的式子表示)。
的式子表示)。
 脱氢反应制取[
脱氢反应制取[ ],回答下列问题。
],回答下列问题。(1)已知:①


②


③


则甲醇脱氢制蚁酸甲酯反应的

 。
。(2)实际生产中还会发生副反应:
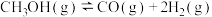
 。保持压强为
。保持压强为 制备蚁酸甲酯,各组分平衡物质的量分数随温度的变化如图所示。
制备蚁酸甲酯,各组分平衡物质的量分数随温度的变化如图所示。
②
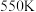 时,甲醇的平衡转化率为
时,甲醇的平衡转化率为 (小数点后保留1位数字),副反应的压强平衡常数
(小数点后保留1位数字),副反应的压强平衡常数
 (用包含
(用包含 的代数式表示)。
的代数式表示)。(3)甲醇脱氢制蚁酸甲酯的反应机理如下(带“*”的物质表示自由基或原子,
 和
和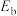 为活化能,
为活化能, 、
、 、
、 为平衡常数)。
为平衡常数)。步骤1:



步骤2:


步骤3:

步骤4:


①利用量子力学模拟计算,发现步骤1还有可能发生反应:

 ,但实际检测发现生成的
,但实际检测发现生成的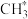 量很少,试分析其原因
量很少,试分析其原因②将步骤3发生的反应补充完整:
③反应
 的平衡常数
的平衡常数
 、
、 、
、 的式子表示)。
的式子表示)。
您最近一年使用:0次
2024-03-08更新
|
144次组卷
|
5卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学
名校
6 . 二硫化碳( )是一种重要有机溶剂,易挥发、易燃烧。利用硅酸作催化剂,甲烷和硫黄在
)是一种重要有机溶剂,易挥发、易燃烧。利用硅酸作催化剂,甲烷和硫黄在 条件下发生反应可制得
条件下发生反应可制得 ,根据所给信息,回答下列问题。
,根据所给信息,回答下列问题。
反应原理:
反应装置: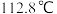 ,沸点
,沸点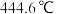 ;
; 的熔点
的熔点 ,沸点
,沸点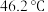 。
。
(1)装置A的名称是___________ ,加热装置A之前,需要先通入一段时间的 ,其目的是
,其目的是___________ (写出一点即可)。
(2)装置B的用途是___________ ,吸收尾气中的硫化氢可使用的试剂是___________ (填试剂名称)。
(3)反应过程中轻轻摇动装置A,使液态硫附着在装置A的内壁上,这样作的目的是___________ 。
(4)实验结束后,将制得的产品用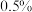 的高锰酸钾溶液洗涤三次,再加入汞不断振荡除去硫单质,分离出
的高锰酸钾溶液洗涤三次,再加入汞不断振荡除去硫单质,分离出 利用无水氯化钙处理后,再经过操作a可获得高纯的
利用无水氯化钙处理后,再经过操作a可获得高纯的 。利用高锰酸钾溶液洗涤是为了除去溶在
。利用高锰酸钾溶液洗涤是为了除去溶在 中的
中的___________ (写化学式),用无水氯化钙处理 的目的是
的目的是___________ ,操作a是___________ (写操作名称)。
(5)工业利用上述原理生产 时,常将副产品
时,常将副产品 利用克劳斯法转化为
利用克劳斯法转化为 ,从而实现循环利用,该方法分两步进行:
,从而实现循环利用,该方法分两步进行: 、
、___________ (写出化学方程式)。
 )是一种重要有机溶剂,易挥发、易燃烧。利用硅酸作催化剂,甲烷和硫黄在
)是一种重要有机溶剂,易挥发、易燃烧。利用硅酸作催化剂,甲烷和硫黄在 条件下发生反应可制得
条件下发生反应可制得 ,根据所给信息,回答下列问题。
,根据所给信息,回答下列问题。反应原理:

反应装置:

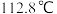 ,沸点
,沸点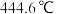 ;
; 的熔点
的熔点 ,沸点
,沸点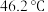 。
。(1)装置A的名称是
 ,其目的是
,其目的是(2)装置B的用途是
(3)反应过程中轻轻摇动装置A,使液态硫附着在装置A的内壁上,这样作的目的是
(4)实验结束后,将制得的产品用
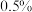 的高锰酸钾溶液洗涤三次,再加入汞不断振荡除去硫单质,分离出
的高锰酸钾溶液洗涤三次,再加入汞不断振荡除去硫单质,分离出 利用无水氯化钙处理后,再经过操作a可获得高纯的
利用无水氯化钙处理后,再经过操作a可获得高纯的 。利用高锰酸钾溶液洗涤是为了除去溶在
。利用高锰酸钾溶液洗涤是为了除去溶在 中的
中的 的目的是
的目的是(5)工业利用上述原理生产
 时,常将副产品
时,常将副产品 利用克劳斯法转化为
利用克劳斯法转化为 ,从而实现循环利用,该方法分两步进行:
,从而实现循环利用,该方法分两步进行: 、
、
您最近一年使用:0次
2024-03-08更新
|
112次组卷
|
4卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学
名校
7 . 海水总溶解无机碳值(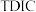 )是影响海洋生态稳定的重要指标,常温,不同
)是影响海洋生态稳定的重要指标,常温,不同 条件下,海水中部分溶解无机碳的百分率如图所示,已知:珊瑚虫通过钙化反应:
条件下,海水中部分溶解无机碳的百分率如图所示,已知:珊瑚虫通过钙化反应: 可形成珊瑚礁。下列说法中不正确的是
可形成珊瑚礁。下列说法中不正确的是
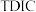 )是影响海洋生态稳定的重要指标,常温,不同
)是影响海洋生态稳定的重要指标,常温,不同 条件下,海水中部分溶解无机碳的百分率如图所示,已知:珊瑚虫通过钙化反应:
条件下,海水中部分溶解无机碳的百分率如图所示,已知:珊瑚虫通过钙化反应: 可形成珊瑚礁。下列说法中不正确的是
可形成珊瑚礁。下列说法中不正确的是
A.常温下,海水的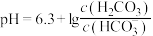 |
B.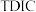 值 值 |
C. 时,海水中 时,海水中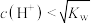 |
| D.与珊瑚共生的藻类通过光合作用可促进珊瑚礁的形成 |
您最近一年使用:0次
2024-03-08更新
|
163次组卷
|
3卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学
名校
8 .  是一种重要的工业原料,利用
是一种重要的工业原料,利用 和
和 直接法合成
直接法合成 的反应历程如图所示,下列说法中不正确的是
的反应历程如图所示,下列说法中不正确的是
 是一种重要的工业原料,利用
是一种重要的工业原料,利用 和
和 直接法合成
直接法合成 的反应历程如图所示,下列说法中不正确的是
的反应历程如图所示,下列说法中不正确的是
A.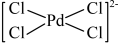 和 和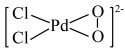 中的Pd的化合价相同 中的Pd的化合价相同 |
B.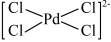 降低了反应的活化能,加快了反应速率 降低了反应的活化能,加快了反应速率 |
C.直接法合成过氧化氢的总反应,原子利用率理论上为 |
D.步骤2中,若有 参与反应,转移电子数目为 参与反应,转移电子数目为 |
您最近一年使用:0次
2024-03-08更新
|
183次组卷
|
4卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学
9 .  是一种高效水处理剂,工业上可利用电解法制备,其原理如图所示。下列说法中正确的是
是一种高效水处理剂,工业上可利用电解法制备,其原理如图所示。下列说法中正确的是
 是一种高效水处理剂,工业上可利用电解法制备,其原理如图所示。下列说法中正确的是
是一种高效水处理剂,工业上可利用电解法制备,其原理如图所示。下列说法中正确的是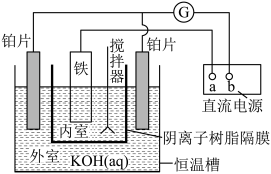
A.图中电极 为直流电源的负极 为直流电源的负极 | B.电解过程中铂片上有 生成 生成 |
C.电解时 由外室进入内室 由外室进入内室 | D.转移 电子,生成 电子,生成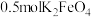 |
您最近一年使用:0次
2024-03-08更新
|
122次组卷
|
3卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学
10 . 下列有关文物的说法中正确的是
| A.玉壶春瓶主要成分是陶瓷,其生产原料为黏土和石灰石 |
| B.人面纹方鼎和蛇纹尊均属于青铜器,青铜属于金属材料 |
| C.素纱单衣由蚕丝编制而成,蚕丝的主要成分为氨基酸 |
D.红色漆器中可能含有朱砂( )、青矾( )、青矾( )等 )等 |
您最近一年使用:0次
2024-03-08更新
|
160次组卷
|
4卷引用:陕西省延安市黄龙县中学2023-2024学年高三下学期开学考试理综试卷-高中化学



