解题方法
1 . 中国高铁对实现“一带一路”的倡议有重要的作用。
(1)高铁上的信息传输系统使用了光导纤维,其主要成分是______ ;乘务员使用的无线通话机的芯片材料是______ 。
(2)SiO2是一种酸性氧化物,能与强碱溶液反应。例如,SiO2与NaOH反应可生成 。
。 的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式
的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式______ 。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为______ 。
(4)氮化硅(Si3N4)可由石英与焦炭在高温的氮气流中通过以下反应制备: 。
。
①以及以上反应中的氧化剂______ ,还原剂 ______ 。
②若该反应生成67.2L一氧化碳(标准状况),则生成氮化硅的质量_______ g。
(1)高铁上的信息传输系统使用了光导纤维,其主要成分是
(2)SiO2是一种酸性氧化物,能与强碱溶液反应。例如,SiO2与NaOH反应可生成
 。
。 的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式
的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。请写出相关反应的化学方程式(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为
(4)氮化硅(Si3N4)可由石英与焦炭在高温的氮气流中通过以下反应制备:
 。
。①以及以上反应中的氧化剂
②若该反应生成67.2L一氧化碳(标准状况),则生成氮化硅的质量
您最近一年使用:0次
解题方法
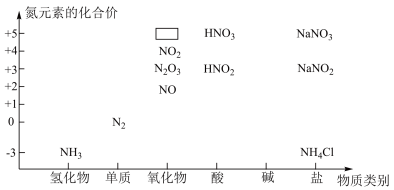
2 . 下图是氮的化合物的“价类二维图”。______ ,该物质的电子式_____ 。
(2)写出实验室制取氨气的化学方程式:______ 。
(3)实验室中硝酸通常保存在棕色瓶中,硝酸保存在棕色瓶中的原因:____ (请用方程式解释。)
(4)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。铜与浓硝酸反应的化学方程式为_____ ;以上反应中酸性与氧化性硝酸的物质的量之比_____ 。
(5)工业生产中为了盛装大量浓硝酸,可选择_____ 作为罐体材料。
a.铜 b.铝 c.铂 d.镁
(2)写出实验室制取氨气的化学方程式:
(3)实验室中硝酸通常保存在棕色瓶中,硝酸保存在棕色瓶中的原因:
(4)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。铜与浓硝酸反应的化学方程式为
(5)工业生产中为了盛装大量浓硝酸,可选择
a.铜 b.铝 c.铂 d.镁
您最近一年使用:0次
3 . 化学在“国之重器”的打造中发挥着重要作用。下列说法不正确的是
| A.“库车绿氢”用光伏发电电解水制氢,能有效减少碳排放 |
B.国产大飞机“ ”使用的芳纶蜂窝材料属于有机高分子材料 ”使用的芳纶蜂窝材料属于有机高分子材料 |
C.国产 “龙芯 “龙芯 ”的主要材料与光导纤维的材料相同 ”的主要材料与光导纤维的材料相同 |
| D.“鲲龙”水陆两栖飞机所用的航空煤油是石油分馏产品 |
您最近一年使用:0次
2024-04-07更新
|
412次组卷
|
2卷引用:2024届陕西省宝鸡市高三下学期三模考试理科综合试题-高中化学
4 . 回答下列问题
(1)有A、B、C、D、E五种元素,它们的核电荷数依次增大,A是元素周期表中原子半径最小的一种元素,B、C、D、E是连继相邻的四种元素,且均比A多一个电子层,其中E是元素周期表中非金属性最强的一种元素,按要求完成下列问题:
①这几种元素中电负性最大的是_______ (填元素符号,下同);
②B、C、D、E的第一电离能由小到大的顺序是_______ ;
③C的最高价氧化物对应的水化物和C的最低价氢物形成的化合物的化学式是_______ 。
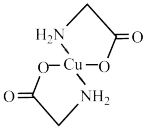
(2)太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:
①硅原子电子占据的最高能级电子云形状为_______ ;
②Fe3+的价电子排布图为_______ ;
③铜位于周期表中_______ 区,铜原子的电子排布式为_______ 。试从核外电子排布角度比较,高温下Cu2O和CuO的稳定性更高的原因是_______ 。
(1)有A、B、C、D、E五种元素,它们的核电荷数依次增大,A是元素周期表中原子半径最小的一种元素,B、C、D、E是连继相邻的四种元素,且均比A多一个电子层,其中E是元素周期表中非金属性最强的一种元素,按要求完成下列问题:
①这几种元素中电负性最大的是
②B、C、D、E的第一电离能由小到大的顺序是
③C的最高价氧化物对应的水化物和C的最低价氢物形成的化合物的化学式是
(2)太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、铁、钴、硼、镓、硒等。其中某种重要的含铜的化合物结构如图。请回答下列问题:

①硅原子电子占据的最高能级电子云形状为
②Fe3+的价电子排布图为
③铜位于周期表中
您最近一年使用:0次
解题方法
5 . 回答下列问题:
(1)实验室配制FeSO4溶液,溶解时先要加入少量的稀硫酸,其原因是
(2)下列盐溶液中能发生水解,
①Na2CO3
②(NH4)2SO4
③泡沫灭火器里盛有Al2(SO4)3溶液和NaHCO3溶液,当灭火时,这两种溶液混合立即喷出大量泡沫,写出水解离子方程式
(3)物质的量浓度均为0.1mol/L的下列溶液:①KNO3、②K2CO3、③KHCO3、④H2SO4、⑤CH3COOH、⑥NaOH、⑦Ba(OH)2,pH由大到小的顺序为:
(4)写出NH4Cl溶液中各
您最近一年使用:0次
6 . 已知某温度下,Mg(OH)2在水中的溶解度为5.8×10-3g/L。
(1)该温度下Mg(OH)2饱和溶液中的溶度积Ksp为_______ ;
(2)Mg(OH)2在0.001mol/L的NaOH溶液中的溶解度为_______ mol/L
(3)若要使Mg(OH)2饱和溶液中沉淀转化为MgCO3沉淀,加入碳酸钠固体使碳酸根离子浓度至少为_______ mol/L(说明:已知Ksp(MgCO3)=6.6×10-5)。
(4)向物质的量浓度均为0.1mol/l的MgCl2和MnCl2溶液中逐滴加入NaOH溶液,最先析出沉淀是_______ ,可否用控制pH值的方法分离上述溶液中的Mg2+和Mn2+ _______ 。(已知KspMn(OH)2=5×10-14,离子浓度降低到1×10-5mol/L时可认为沉淀完全)
(1)该温度下Mg(OH)2饱和溶液中的溶度积Ksp为
(2)Mg(OH)2在0.001mol/L的NaOH溶液中的溶解度为
(3)若要使Mg(OH)2饱和溶液中沉淀转化为MgCO3沉淀,加入碳酸钠固体使碳酸根离子浓度至少为
(4)向物质的量浓度均为0.1mol/l的MgCl2和MnCl2溶液中逐滴加入NaOH溶液,最先析出沉淀是
您最近一年使用:0次
解题方法
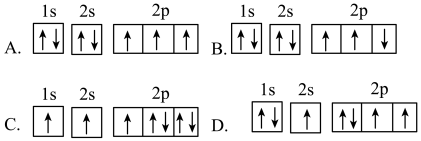
7 . 下列关于元素的说法正确的是
| A.基态原子失去一个电子转化为基态正离子所需要的能量叫做第一电离能 |
| B.钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠 |
| C.金属的电负性小于1.8,而非金属的电负性大于1.8 |
| D.元素的电负性越大,非金属性就越强,元素原子的第一电离就越大 |
您最近一年使用:0次
名校
解题方法
8 . 江西矿产资源丰富,其中铁、锰、钛、钒、铜、锌、金、银等储量居全国前3位,有亚洲最大的铜矿和中国最大的铜冶炼基地。回答下列问题:
(1)Ni元素在元素周期表中位置___________ 。
(2)[Cu(NH3)4]Cl2是一种常见农药,能防治真菌、细菌和霉菌引起的多种病害。
①1mol[Cu(NH3)4]Cl2中含有的σ键数目为___________ NA;NH3分子与Cu2+形成配合物后H-N-H键角___________ (填“变大”“变小”或“不变”)。
②已知[Cu(NH3)4]2+呈平面正方形,则Cu2+的杂化方式可能为___________ (填标号)。
A.sp3 B.dsp2 C.sp2 D.sp
(3)Cu与Fe的第二电离能分别为I2(Cu)=1958kJ•mol﹣1、I2(Fe)=1561kJ•mol﹣1,I2(Cu)大于I2(Fe)的主要原因是___________ 。
(4)在第二周期中,第一电离能比N高的元素是___________ 。氮原子的电子排布图表示的状态中,能量由低到高的顺序是___________ (填序号)。 ,0,
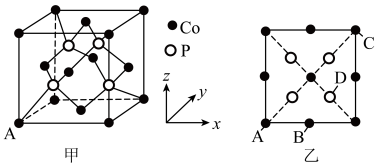
,0, ),则D点坐标为
),则D点坐标为___________ 。
②已知该晶体的密度为ρg•cm-3,设NA表示阿伏加德罗常数的值,则该晶胞中距离最近的Co原子之间的距离为___________ nm(用含ρ、NA的计算式表示)。
(1)Ni元素在元素周期表中位置
(2)[Cu(NH3)4]Cl2是一种常见农药,能防治真菌、细菌和霉菌引起的多种病害。
①1mol[Cu(NH3)4]Cl2中含有的σ键数目为
②已知[Cu(NH3)4]2+呈平面正方形,则Cu2+的杂化方式可能为
A.sp3 B.dsp2 C.sp2 D.sp
(3)Cu与Fe的第二电离能分别为I2(Cu)=1958kJ•mol﹣1、I2(Fe)=1561kJ•mol﹣1,I2(Cu)大于I2(Fe)的主要原因是
(4)在第二周期中,第一电离能比N高的元素是
 ,0,
,0, ),则D点坐标为
),则D点坐标为②已知该晶体的密度为ρg•cm-3,设NA表示阿伏加德罗常数的值,则该晶胞中距离最近的Co原子之间的距离为
您最近一年使用:0次
2024-02-19更新
|
320次组卷
|
2卷引用:陕西省宝鸡中学2023-2024学年高二下学期阶段考试(一)化学试题
名校
9 . 下列说法不正确的是
| A.利用红外光谱可分析分子中含有的化学键或官能团的信息 |
| B.用质谱法可测定分子的相对分子质量 |
C.可利用价层电子对互斥模型分析 和 和 空间结构 空间结构 |
| D.氧原子的基态原子最外层轨道表示式中不需要考虑洪特规则 |
您最近一年使用:0次
2024-02-01更新
|
244次组卷
|
4卷引用:陕西省宝鸡中学2023-2024学年高二下学期阶段考试(一)化学试题
陕西省宝鸡中学2023-2024学年高二下学期阶段考试(一)化学试题 浙江省绍兴市柯桥区2023-2024学年高二上学期期末教学质量调测化学试题(已下线)2.2.1 分子结构的测定和多样性、价层电子对互斥模型课堂例题(已下线)清单04 有机化合物的结构特点与研究方法(考点清单)(讲+练)-2023-2024学年高二化学下学期期末考点大串讲(人教版2019)
解题方法
10 . 某实验小组对一种染料废水进行处理,获得Na2SO4并测定废水的总有机碳(总有机碳是指单位体积水样中溶解或悬浮的有机物碳元素质量总和,是水体评价的综合指标之一)。
实验步骤为:
①取100mL废水(假定有机成分只有萘磺酸钠),在35℃下加入等体积甲醇,充分混合后,冷却、过滤,得到固体A和滤液B。
②经检测,固体A主要成分为Na2SO4,并含有少量Na2SO3和萘磺酸钠;滤液B含2.3g萘磺酸钠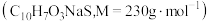 。
。
③一定温度下,从滤液B中回收甲醇;再蒸发浓缩析出萘磺酸钠,过滤,得滤液C,向滤液C中加入适量的NaClO溶液去除少量的 和NH3。
和NH3。
④按下图实验装置(部分装置略)对固体A进行处理,完全反应后Pt坩埚中固体为Na2SO4。
回答下列问题:
(1)实验步骤①中加入甲醇的目的为_______ 。
(2)实验步骤③中回收甲醇的操作名称是_______ ,去除NH3生成N2反应的离子方程式为_______ 。
(3)通入N2的目的是_______ 。
(4)酸性KMnO4溶液的作用是_______ ,试剂 是
是_______ 。
(5)改为通入O2前,需_______(填标号)。
(6)反应后U形管(含试剂)增重0.44g,该废水总有机碳=_______  (用科学记数法表示)。
(用科学记数法表示)。
实验步骤为:
①取100mL废水(假定有机成分只有萘磺酸钠),在35℃下加入等体积甲醇,充分混合后,冷却、过滤,得到固体A和滤液B。
②经检测,固体A主要成分为Na2SO4,并含有少量Na2SO3和萘磺酸钠;滤液B含2.3g萘磺酸钠
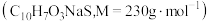 。
。③一定温度下,从滤液B中回收甲醇;再蒸发浓缩析出萘磺酸钠,过滤,得滤液C,向滤液C中加入适量的NaClO溶液去除少量的
 和NH3。
和NH3。④按下图实验装置(部分装置略)对固体A进行处理,完全反应后Pt坩埚中固体为Na2SO4。
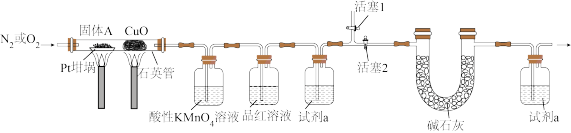
回答下列问题:
(1)实验步骤①中加入甲醇的目的为
(2)实验步骤③中回收甲醇的操作名称是
(3)通入N2的目的是
(4)酸性KMnO4溶液的作用是
 是
是(5)改为通入O2前,需_______(填标号)。
| A.打开活塞1 | B.打开活塞2 | C.关闭活塞1 | D.关闭活塞2 |
(6)反应后U形管(含试剂)增重0.44g,该废水总有机碳=
 (用科学记数法表示)。
(用科学记数法表示)。
您最近一年使用:0次
2024-01-20更新
|
1013次组卷
|
5卷引用:2024届陕西省宝鸡市高三下学期三模考试理科综合试题-高中化学
2024届陕西省宝鸡市高三下学期三模考试理科综合试题-高中化学2024年1月河南普通高等学校招生考试适应性测试化学试题(已下线)T27-实验综合题(已下线)2024年1月“九省联考”河南卷真题完全解读与考后提升(已下线)热点22 定量分析型实验综合题



