真题
解题方法
1 . 高氯酸铵(NH4ClO4)是复合火箭推进剂的重要成分,实验室可通过下列反应制取NaClO4 (aq)+NH4Cl(aq)  NH4ClO4 (aq)+NaCl(aq)
NH4ClO4 (aq)+NaCl(aq)
(1)若NH4Cl用氨气和浓盐酸代替,上述反应不需要外界供热就能进行,其原因是_______ 。
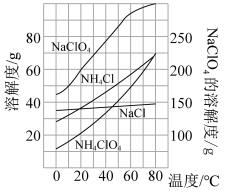
(2)反应得到的混合溶液中NH4ClO4和NaCl的质量分数分别为0.30和0.15(相关物质的溶解度曲线如图)。从混合溶液中获得较多NH4ClO4晶体的实验操作依次为(填操作名称)_______ 、干燥。
(3)样品中NH4ClO4的含量可用蒸馏法进行测定,蒸馏装置如图所示(加热和仪器固定装置已略去),实验步骤如下:
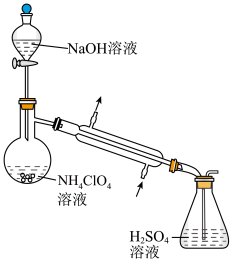
步骤1:按图示组装仪器,检查装置气密性。
步骤2:准确称取样品a g(约0.5g)于蒸馏烧瓶中,加入约150mL水溶解。
步骤3:准确量取40.00mL约 H2SO4 溶解于锥形瓶中。
H2SO4 溶解于锥形瓶中。
步骤4:经滴液漏斗向蒸馏瓶中加入20mL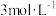 NaOH 溶液。
NaOH 溶液。
步骤5:加热蒸馏至蒸馏烧瓶中剩余约100mL溶液。
步骤6:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤7:向锥形瓶中加入酸碱指示剂,用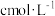 NaOH标准溶液滴定至终点,消耗NaOH标准溶液V1mL
NaOH标准溶液滴定至终点,消耗NaOH标准溶液V1mL
步骤8.将实验步骤1-7重复2次
①步骤3中,准确量取40.00mLH2SO4 溶液的玻璃仪器是_______ 。
②步骤1-7中确保生成的氨被稀硫酸完全吸收的实验是_______ (填写步骤号)。
③为获得样品中NH4ClO4 的含量,还需补充的实验是_______
 NH4ClO4 (aq)+NaCl(aq)
NH4ClO4 (aq)+NaCl(aq)(1)若NH4Cl用氨气和浓盐酸代替,上述反应不需要外界供热就能进行,其原因是
(2)反应得到的混合溶液中NH4ClO4和NaCl的质量分数分别为0.30和0.15(相关物质的溶解度曲线如图)。从混合溶液中获得较多NH4ClO4晶体的实验操作依次为(填操作名称)

(3)样品中NH4ClO4的含量可用蒸馏法进行测定,蒸馏装置如图所示(加热和仪器固定装置已略去),实验步骤如下:

步骤1:按图示组装仪器,检查装置气密性。
步骤2:准确称取样品a g(约0.5g)于蒸馏烧瓶中,加入约150mL水溶解。
步骤3:准确量取40.00mL约
 H2SO4 溶解于锥形瓶中。
H2SO4 溶解于锥形瓶中。步骤4:经滴液漏斗向蒸馏瓶中加入20mL
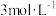 NaOH 溶液。
NaOH 溶液。步骤5:加热蒸馏至蒸馏烧瓶中剩余约100mL溶液。
步骤6:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤7:向锥形瓶中加入酸碱指示剂,用
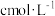 NaOH标准溶液滴定至终点,消耗NaOH标准溶液V1mL
NaOH标准溶液滴定至终点,消耗NaOH标准溶液V1mL步骤8.将实验步骤1-7重复2次
①步骤3中,准确量取40.00mLH2SO4 溶液的玻璃仪器是
②步骤1-7中确保生成的氨被稀硫酸完全吸收的实验是
③为获得样品中NH4ClO4 的含量,还需补充的实验是
您最近一年使用:0次
真题
2 . 本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容。请选定其中一题,并在相应的答题区域内作答。若两题都做,则按A题评分。
A.乙炔是有机合成工业的一种原料。工业上曾用 与水反应生成乙炔。
与水反应生成乙炔。
(1) 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为_______ ;1mol 中含有的
中含有的 键数目为
键数目为___________ 。
(2)将乙炔通入 溶液生成
溶液生成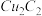 红棕色沉淀。
红棕色沉淀。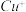 基态核外电子排布式为
基态核外电子排布式为_________________________ 。
(3)乙炔与氢氰酸反应可得丙烯腈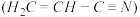 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是________________ ;分子中处于同一直线上的原子数目最多为__________________ 。
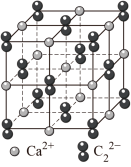
(4) 晶体的晶胞结构与
晶体的晶胞结构与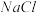 晶体相似(如图所示),但
晶体相似(如图所示),但 晶体中含有的中哑铃形
晶体中含有的中哑铃形 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。 晶体中1个
晶体中1个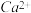 周围距离最近的
周围距离最近的 数目为
数目为______________ 。
B.对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。

一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在 溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
(l)上述实验中过滤的目的是_________________ 。
(2) 滤液在分液漏斗中洗涤静置后,有机层处于_______ 层(填“上”或'下”);放液时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还有_____________ 。
(3) 下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
①NaHSO4催化制备对硝基甲苯时,催化剂与甲苯的最佳物质的量之比为______________ 。
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是____________________ 。
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有_________ 、_________ 。
A.乙炔是有机合成工业的一种原料。工业上曾用
 与水反应生成乙炔。
与水反应生成乙炔。(1)
 中
中 与
与 互为等电子体,
互为等电子体, 的电子式可表示为
的电子式可表示为 中含有的
中含有的 键数目为
键数目为(2)将乙炔通入
 溶液生成
溶液生成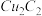 红棕色沉淀。
红棕色沉淀。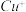 基态核外电子排布式为
基态核外电子排布式为(3)乙炔与氢氰酸反应可得丙烯腈
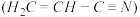 。丙烯腈分子中碳原子轨道杂化类型是
。丙烯腈分子中碳原子轨道杂化类型是(4)
 晶体的晶胞结构与
晶体的晶胞结构与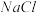 晶体相似(如图所示),但
晶体相似(如图所示),但 晶体中含有的中哑铃形
晶体中含有的中哑铃形 的存在,使晶胞沿一个方向拉长。
的存在,使晶胞沿一个方向拉长。 晶体中1个
晶体中1个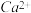 周围距离最近的
周围距离最近的 数目为
数目为
B.对硝基甲苯是医药、染料等工业的一种重要有机中间体,它常以浓硝酸为硝化剂,浓硫酸为催化剂,通过甲苯的硝化反应制备。

一种新的制备对硝基甲苯的实验方法是:以发烟硝酸为硝化剂,固体NaHSO4为催化剂(可循环使用),在
 溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。
溶液中,加入乙酸酐(有脱水作用),45℃反应1h 。反应结束后,过滤,滤液分别用5% NaHCO3,溶液、水洗至中性,再经分离提纯得到对硝基甲苯。(l)上述实验中过滤的目的是
(2) 滤液在分液漏斗中洗涤静置后,有机层处于
(3) 下列给出了催化剂种类及用量对甲苯硝化反应影响的实验结果。
| 催化剂 | 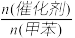 | 硝化产物中各种异构体质量分数(%) | 总产率(%) | ||
| 对硝基甲苯 | 邻硝基甲苯 | 间硝基甲苯 | |||
| 浓H2SO4 | 1.0 | 35.6 | 60.2 | 4.2 | 98.0 |
| 1.2 | 36.5 | 59.5 | 4.0 | 99.8 | |
| NaHSO4 | 0.15 | 44.6 | 55.1 | 0.3 | 98.9 |
| 0.25 | 46.3 | 52.8 | 0.9 | 99.9 | |
| 0.32 | 47.9 | 51.8 | 0.3 | 99.9 | |
| 0.36 | 45.2 | 54.2 | 0.6 | 99.9 | |
②由甲苯硝化得到的各种产物的含量可知,甲苯硝化反应的特点是
③与浓硫酸催化甲苯硝化相比,NaHSO4催化甲苯硝化的优点有
您最近一年使用:0次
2019-01-30更新
|
1046次组卷
|
3卷引用:2010年普通高等学校招生统一考试理综试题化学部分(江苏卷)
真题
解题方法
3 . 实验室以二氧化铈( )废渣为原料制备
)废渣为原料制备 含量少的
含量少的 ,其部分实验过程如下:
,其部分实验过程如下:

(1)“酸浸”时 与
与 反应生成
反应生成 并放出
并放出 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
(2)pH约为7的 溶液与
溶液与 溶液反应可生成
溶液反应可生成 沉淀,该沉淀中
沉淀,该沉淀中 含量与加料方式有关。得到含
含量与加料方式有关。得到含 量较少的
量较少的 的加料方式为
的加料方式为_______ (填序号)。
A.将 溶液滴加到
溶液滴加到 溶液中 B.将
溶液中 B.将 溶液滴加到
溶液滴加到 溶液中
溶液中
(3)通过中和、萃取、反萃取、沉淀等过程,可制备 含量少的
含量少的 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
 (水层)+3HA(有机层)
(水层)+3HA(有机层)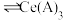 (有机层)+
(有机层)+ (水层)
(水层)
①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是_______ 。
②反萃取的目的是将有机层 转移到水层。使
转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有
尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有_______ (填两项)。
③与“反萃取”得到的水溶液比较,过滤 溶液的滤液中,物质的量减小的离子有
溶液的滤液中,物质的量减小的离子有_______ (填化学式)。
(4)实验中需要测定溶液中 的含量。已知水溶液中
的含量。已知水溶液中 可用准确浓度的
可用准确浓度的 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充完整实验方案:①准确量取
。请补充完整实验方案:①准确量取 溶液[
溶液[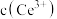 约为
约为 ],加氧化剂将
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到
完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到 容量瓶中后定容;②按规定操作分别将
容量瓶中后定容;②按规定操作分别将 和待测
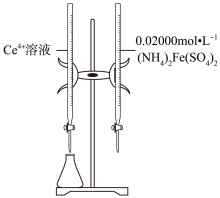
和待测 溶液装入如图所示的滴定管中:③
溶液装入如图所示的滴定管中:③_______ 。
 )废渣为原料制备
)废渣为原料制备 含量少的
含量少的 ,其部分实验过程如下:
,其部分实验过程如下:
(1)“酸浸”时
 与
与 反应生成
反应生成 并放出
并放出 ,该反应的离子方程式为
,该反应的离子方程式为(2)pH约为7的
 溶液与
溶液与 溶液反应可生成
溶液反应可生成 沉淀,该沉淀中
沉淀,该沉淀中 含量与加料方式有关。得到含
含量与加料方式有关。得到含 量较少的
量较少的 的加料方式为
的加料方式为A.将
 溶液滴加到
溶液滴加到 溶液中 B.将
溶液中 B.将 溶液滴加到
溶液滴加到 溶液中
溶液中(3)通过中和、萃取、反萃取、沉淀等过程,可制备
 含量少的
含量少的 。已知
。已知 能被有机萃取剂(简称HA)萃取,其萃取原理可表示为
能被有机萃取剂(简称HA)萃取,其萃取原理可表示为 (水层)+3HA(有机层)
(水层)+3HA(有机层)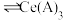 (有机层)+
(有机层)+ (水层)
(水层)①加氨水“中和”去除过量盐酸,使溶液接近中性。去除过量盐酸的目的是
②反萃取的目的是将有机层
 转移到水层。使
转移到水层。使 尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有
尽可能多地发生上述转移,应选择的实验条件或采取的实验操作有③与“反萃取”得到的水溶液比较,过滤
 溶液的滤液中,物质的量减小的离子有
溶液的滤液中,物质的量减小的离子有(4)实验中需要测定溶液中
 的含量。已知水溶液中
的含量。已知水溶液中 可用准确浓度的
可用准确浓度的 溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为
溶液滴定。以苯代邻氨基苯甲酸为指示剂,滴定终点时溶液由紫红色变为亮黄色,滴定反应为 。请补充完整实验方案:①准确量取
。请补充完整实验方案:①准确量取 溶液[
溶液[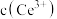 约为
约为 ],加氧化剂将
],加氧化剂将 完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到
完全氧化并去除多余氧化剂后,用稀硫酸酸化,将溶液完全转移到 容量瓶中后定容;②按规定操作分别将
容量瓶中后定容;②按规定操作分别将 和待测
和待测 溶液装入如图所示的滴定管中:③
溶液装入如图所示的滴定管中:③
您最近一年使用:0次
2022-07-21更新
|
8005次组卷
|
13卷引用:江苏省2022年普通高中学业水平选择性考试
江苏省2022年普通高中学业水平选择性考试(已下线)2022年江苏卷高考真题变式题14-17(已下线)江苏省2022年普通高中学业水平选择性考试变式题(实验探究题)(已下线)专题16 化学实验综合题-2022年高考真题模拟题分项汇编(已下线)专题17 化工流程综合题-备战2023年高考化学母题题源解密(广东卷)(已下线)易错点33 物质的制备-备战2023年高考化学考试易错题(已下线)热点情景汇编-专题十三 实验探究中的新思路(已下线)专题26 定量测定类综合性实验题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第30讲水的电离和溶液的酸碱性(已下线)题型四 以无机物制备为载体的综合实验-备战2024年高考化学答题技巧与模板构建
4 . 前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y的周期序数与族序数相等,基态时Z原子3p原子轨道上有5个电子,W与Z处于同个主族。下列说法正确的是
| A.原子半径:r(X)<r(Y)<r(Z)<r(W) |
| B.X的第一电离能比同周期相邻元素的大 |
| C.Y的最高价氧化物对应水化物的酸性比Z的强 |
| D.Z的简单气态氢化物的热稳定性比W的弱 |
您最近一年使用:0次
2022-01-04更新
|
7516次组卷
|
13卷引用:2021年新高考江苏化学高考真题
2021年新高考江苏化学高考真题(已下线)必刷卷01-2022年高考化学考前信息必刷卷(江苏专用)(已下线)押江苏卷第5题 物质结构与元素周期律 -备战2022年高考化学临考题号押题(江苏卷)江苏省南京市燕子矶中学2022-2023学年高二下学期3月月考化学试题江苏省连云港高级中学2022-2023学年高二下学期第二次学情检测化学试题04 2024年苏州震泽高二3月月考湖南省郴州市第一中学2022届高三下学期期中考试化学试题(已下线)专题33 物质结构与性质基础-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)题型74 核外电子排布与元素推断(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)2024届天域全国名校协作体学年高三下学期联考化学学科试题
真题
名校
5 . 医用氯化钙可用于生产补钙、抗过敏和消炎等药物。以工业碳酸钙(含有少量Na+、Al3+、Fe3+等杂质)生产医药级二水合氯化钙(CaCl2·2H2O的质量分数为97.0%~103.0%)的主要流程如下:
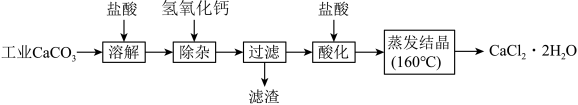
(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0~8.5,以除去溶液中的少量Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是________________ 。
(2)酸化操作是加入盐酸,调节溶液的pH为4.0,其目的有:①将溶液中的少量Ca(OH)2转化为CaCl2;②防止Ca2+在蒸发时水解;③_______________ 。
(3)测定样品中Cl-含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测液于锥形瓶中;c.用0.05000mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL。
①上述测定过程中需用溶液润洗的仪器有:____________________ 。
②计算上述样品中CaCl2·2H2O的质量分数为:____________________ 。
③若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有:__________ ;___________ 。

(1)除杂操作是加入氢氧化钙,调节溶液的pH为8.0~8.5,以除去溶液中的少量Al3+、Fe3+。检验Fe(OH)3是否沉淀完全的实验操作是
(2)酸化操作是加入盐酸,调节溶液的pH为4.0,其目的有:①将溶液中的少量Ca(OH)2转化为CaCl2;②防止Ca2+在蒸发时水解;③
(3)测定样品中Cl-含量的方法是:a.称取0.7500g样品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测液于锥形瓶中;c.用0.05000mol·L-1AgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为20.39mL。
①上述测定过程中需用溶液润洗的仪器有:
②计算上述样品中CaCl2·2H2O的质量分数为:
③若用上述方法测定的样品中CaCl2·2H2O的质量分数偏高(测定过程中产生的误差可忽略),其可能原因有:
您最近一年使用:0次
2019-01-30更新
|
1153次组卷
|
5卷引用:2009年普通高等学校招生统一考试化学试题(江苏卷)
2009年普通高等学校招生统一考试化学试题(江苏卷)2009高考真题汇编-化学实验常用仪器和基本操作(已下线)2011届湖北省天门市高三模拟考试(三)(理综)化学部分河北省黄骅中学2018-2019学年高二上学期第二次月考化学试题2020年安徽省全省教学质量检测统一考试(练习检测一)
真题
6 . 聚合硫酸铁[Fe2(OH)6-2n(SO4)n]m广泛用于水的净化。以FeSO4·7H2O为原料,经溶解、氧化、水解聚合等步骤,可制备聚合硫酸铁。
(1)将一定量的FeSO4·7H2O溶于稀硫酸,在约70 ℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。H2O2氧化Fe2+的离子方程式为________ ;水解聚合反应会导致溶液的pH________ 。
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000 g,置于250 mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10−2 mol·L−1 K2Cr2O7溶液滴定至终点(滴定过程中 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00 mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00 mL。
①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将________ (填“偏大”或“偏小”或“无影响”)。
②计算该样品中铁的质量分数(写出计算过程)_____ 。
(1)将一定量的FeSO4·7H2O溶于稀硫酸,在约70 ℃下边搅拌边缓慢加入一定量的H2O2溶液,继续反应一段时间,得到红棕色黏稠液体。H2O2氧化Fe2+的离子方程式为
(2)测定聚合硫酸铁样品中铁的质量分数:准确称取液态样品3.000 g,置于250 mL锥形瓶中,加入适量稀盐酸,加热,滴加稍过量的SnCl2溶液(Sn2+将Fe3+还原为Fe2+),充分反应后,除去过量的Sn2+。用5.000×10−2 mol·L−1 K2Cr2O7溶液滴定至终点(滴定过程中
 与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00 mL。
与Fe2+反应生成Cr3+和Fe3+),消耗K2Cr2O7溶液22.00 mL。①上述实验中若不除去过量的Sn2+,样品中铁的质量分数的测定结果将
②计算该样品中铁的质量分数(写出计算过程)
您最近一年使用:0次
2019-06-10更新
|
4312次组卷
|
6卷引用:2019年江苏省高考化学试题
2019年江苏省高考化学试题江苏省无锡江阴市2021届高三暑期作业开学检测化学试题(已下线)物质含量的测定2020届高考化学二轮复习大题精准训练——定量分析化学实验中物质含量的测定专题3.1 金属及其化合物(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升(已下线)专题02 阿伏加德罗常数及其化学计算 (练)-2023年高考化学二轮复习讲练测(新高考专用)
7 . 以水氯镁石(主要成分为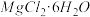 )为原料生产碱式碳酸镁的主要流程如下:
)为原料生产碱式碳酸镁的主要流程如下:
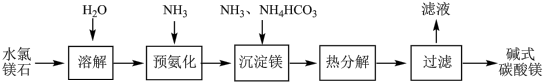
(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的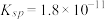 ,若溶液中
,若溶液中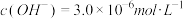 ,则溶液中
,则溶液中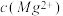 =
=________________ 。
(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为____________________ 。
(3)高温煅烧碱式碳酸镁得到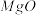 。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下
。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下 0.896L,通过计算确定碱式碳酸镁的化学式
0.896L,通过计算确定碱式碳酸镁的化学式________ 。
(4)若热水解不完全,所得碱式碳酸镁中将混有 ,则产品中镁的质量分数
,则产品中镁的质量分数________ (填 “升高”、“降低”或“不变”)。
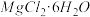 )为原料生产碱式碳酸镁的主要流程如下:
)为原料生产碱式碳酸镁的主要流程如下:
(l)预氨化过程中有Mg(OH)2沉淀生成,已知常温下Mg(OH)2的
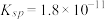 ,若溶液中
,若溶液中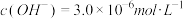 ,则溶液中
,则溶液中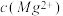 =
=(2)上述流程中的滤液浓缩结晶,所得主要固体物质的化学式为
(3)高温煅烧碱式碳酸镁得到
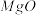 。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下
。取碱式碳酸镁4.66g,高温煅烧至恒重,得到固体2.00g和标准状况下 0.896L,通过计算确定碱式碳酸镁的化学式
0.896L,通过计算确定碱式碳酸镁的化学式(4)若热水解不完全,所得碱式碳酸镁中将混有
 ,则产品中镁的质量分数
,则产品中镁的质量分数
您最近一年使用:0次
2019-01-30更新
|
782次组卷
|
3卷引用:2010年普通高等学校招生统一考试理综试题化学部分(江苏卷)
真题
名校
8 . 短周期元素X、Y、Z、W 的原子序数依次增大,且原子最外层电子数之和为13。X 的原子半径比Y 的小,X 与W 同主族,Z 是地壳中含量最高的元素。下列说法正确的是( )
| A.原子半径的大小顺序: r(Y)>r(Z)>r(W) |
| B.元素Z、W 的简单离子的电子层结构不同 |
| C.元素Y 的简单气态氢化物的热稳定性比Z 的强 |
| D.只含X、Y、Z 三种元素的化合物,可能是离子化合物,也可能是共价化合物 |
您最近一年使用:0次
2019-01-30更新
|
2214次组卷
|
11卷引用:2013年全国普通高等学校招生统一考试化学(江苏卷)
2013年全国普通高等学校招生统一考试化学(江苏卷)(已下线)江苏省海安高级中学2019届高三12月月考化学试题江苏省南京、镇江市部分名校2021-2022学年高二5月学情调查考试化学试题河南省三门峡市2018届高三上学期期末考试化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期开学阶段性考试(8月)化学试题吉林省蛟河高级中学2018-2019学年高一下学期第一次月考化学试题2018-2019学年河南省洛阳市下学期第一次月考高一化学试题辽宁省瓦房店市实验高级中学2018-2019学年高一下学期月考化学试题河北省唐山市海港高级中学2019-2020学年高一下学期期中考试化学试题湖南省娄底市2019-2020学年高二下学期期末考试化学试题江西省上饶市横峰中学2020-2021学年高一下学期第一次月考(统招班)化学试题
真题
名校
9 . 磷是地壳中含量较为丰富的非金属元素,主要以难溶于水的磷酸盐如Ca3(PO4)2等形式存在。它的单质和化合物在工农业生产中有着重要的应用。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)=6CaO(s)+P4(s)+10CO(g) ∆H1=+3359.26kJ·mol-1
CaO(s)+SiO2(s)=CaSiO3(s) ∆H2 =-89.61kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)=6CaSiO3(s)+P4(s)+10CO(g) ∆H3
则∆H3 =_______ kJ·mol-1。
(2)白磷中毒后可用CuSO4溶液解毒,解毒原理可用下列化学方程式表示:11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4;60molCuSO4能氧化白磷的物质的量是_______ 。
(3)磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH 的关系如图所示。
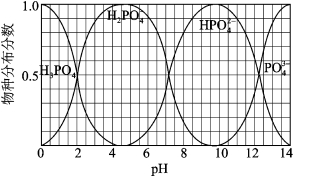
①为获得尽可能纯的NaH2PO4,pH应控制在_______ ;pH=8时,溶液中主要含磷物种浓度大小关系为_______ 。
②Na2HPO4溶液显碱性,若向溶液中加入足量的CaCl2溶液,溶液则显酸性,其原因是_______ (用离子方程式表示)。
(4)磷的化合物三氯氧磷(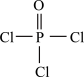 )与季戊四醇(
)与季戊四醇( )以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X 的核磁共振氢谱如图所示。
)以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X 的核磁共振氢谱如图所示。

①酸性气体是_______ (填化学式)。
②X的结构简式为_______ 。
(1)白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)=6CaO(s)+P4(s)+10CO(g) ∆H1=+3359.26kJ·mol-1
CaO(s)+SiO2(s)=CaSiO3(s) ∆H2 =-89.61kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)=6CaSiO3(s)+P4(s)+10CO(g) ∆H3
则∆H3 =
(2)白磷中毒后可用CuSO4溶液解毒,解毒原理可用下列化学方程式表示:11P4+60CuSO4+96H2O=20Cu3P+24H3PO4+60H2SO4;60molCuSO4能氧化白磷的物质的量是
(3)磷的重要化合物NaH2PO4、Na2HPO4和Na3PO4可通过H3PO4与NaOH溶液反应获得,含磷各物种的分布分数(平衡时某物种的浓度占各物种浓度之和的分数)与pH 的关系如图所示。

①为获得尽可能纯的NaH2PO4,pH应控制在
②Na2HPO4溶液显碱性,若向溶液中加入足量的CaCl2溶液,溶液则显酸性,其原因是
(4)磷的化合物三氯氧磷(
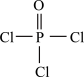 )与季戊四醇(
)与季戊四醇( )以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X 的核磁共振氢谱如图所示。
)以物质的量之比2:1 反应时,可获得一种新型阻燃剂中间体X,并释放出一种酸性气体。季戊四醇与X 的核磁共振氢谱如图所示。
①酸性气体是
②X的结构简式为
您最近一年使用:0次
2019-01-30更新
|
1515次组卷
|
3卷引用:2013年全国普通高等学校招生统一考试化学(江苏卷)
2013年全国普通高等学校招生统一考试化学(江苏卷)【全国百强校】江苏省启东中学2018-2019学年高一(创新班)下学期3月月考化学试题(已下线)2014届高考化学二轮复习必做训练 化学能与热能练习卷
真题
名校
10 . 烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为:
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200·9kJ·mol-1
NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1
SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241·6kJ·mol-1
(1)反应3NO(g)+O3(g)=3NO2(g)的△H=_______ mol·L-1。
(2)室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见下图。
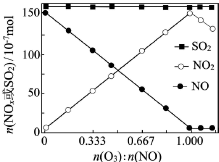
①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是__________ 。
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是_________ 。
(3)当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为 8)中SO32-将NO2转化为NO2-,其离子方程式为:___________ 。
(4)CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中c(SO32-)=________ [用c(SO42-)、Ksp(CaSO3)和Ksp(CaSO4)表示];CaSO3水悬浮液中加入Na2SO4溶液能提高NO2的吸收速率,其主要原因是_________ 。
NO(g)+O3(g)=NO2(g)+O2(g) △H=-200·9kJ·mol-1
NO(g)+1/2O2(g)=NO2(g) △H=-58.2kJ·mol-1
SO2(g)+O3(g)=SO3(g)+O2(g) △H=-241·6kJ·mol-1
(1)反应3NO(g)+O3(g)=3NO2(g)的△H=
(2)室温下,固定进入反应器的NO、SO2的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)、n(NO2)和n(SO2)随反应前n(O3):n(NO)的变化见下图。

①当n(O3):n(NO)>1时,反应后NO2的物质的量减少,其原因是
②增加n(O3),O3氧化SO2的反应几乎不受影响,其可能原因是
(3)当用CaSO3水悬浮液吸收经O3预处理的烟气时,清液(pH约为 8)中SO32-将NO2转化为NO2-,其离子方程式为:
(4)CaSO3水悬浮液中加入Na2SO4溶液,达到平衡后溶液中c(SO32-)=
您最近一年使用:0次
2019-01-30更新
|
1325次组卷
|
5卷引用:2015年全国普通高等学校招生统一考试理科综合能力测试化学(江苏卷)
2015年全国普通高等学校招生统一考试理科综合能力测试化学(江苏卷)2015-2016学年湖南师大附属中学高二上二次阶段测化学卷(已下线)2019高考备考二轮复习精品资料-专题8 化学反应中与能量变化(教学案)湖南省常德市第二中学2021届高三上学期开学考试化学试题内蒙古阿拉善盟第一中学2020-2021学年高二上学期第一次段考化学试题



