解题方法
1 . 下列三个方程式中,有关物质的还原性强弱顺序是I2+SO2+2H2O=H2SO4+2HI;2FeCl2+Cl2=2FeCl3;2FeCl3+2HI=2FeCl2+2HCl+I2
| A.I->Fe2+>Cl->SO2 | B.Cl->Fe2+>SO2> I- |
| C.Fe2+>I->Cl->SO2 | D.SO2>I->Fe2+>Cl- |
您最近一年使用:0次
2024-04-08更新
|
31次组卷
|
2卷引用:天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高一上学期第二次阶段检测(期中)化学试题
名校
2 . 分类法在化学学科的发展中有非常重要的作用,关于物质分类的符合题意是
| 选项 | 混合物 | 纯净物 | 电解质 | 酸性氧化物 |
| A | 盐酸 | NaOH |  溶液 溶液 |  |
| B | 空气 |  胶体 胶体 |  | CO |
| C | 氯水 |  晶体 晶体 | NaCl | 干冰 |
| D | 漂白粉 |  | 石墨 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-05更新
|
97次组卷
|
2卷引用:天津市九十六中学2023-2024学年高一上学期期中考试化学试卷
3 . 写出下列反应的离子反应方程式。
(1)氧化铜与硫酸反应:_______ ;
(2)铁与稀盐酸反应:_______ ;
(3)氯气与NaOH溶液反应:_______ ;
(4)过氧化钠与水反应:_______ ;
(5)氢氧化钡溶液与稀硫酸反应:_______ ;
(6)制备氢氧化铁胶体:_______ ;
(7)碳酸氢钠溶液与稀盐酸反应:_______ 。
(1)氧化铜与硫酸反应:
(2)铁与稀盐酸反应:
(3)氯气与NaOH溶液反应:
(4)过氧化钠与水反应:
(5)氢氧化钡溶液与稀硫酸反应:
(6)制备氢氧化铁胶体:
(7)碳酸氢钠溶液与稀盐酸反应:
您最近一年使用:0次
4 . 工业废水任意排放,会造成环境污染。“协同去污,变废为宝”,为处理工业废水提供了新思路。电镀厂产生大量含 、
、 的电镀废液,皮革厂产生大量含
的电镀废液,皮革厂产生大量含 的废液。两厂联合处理废水,回收Cu并生产铁红和媒染剂
的废液。两厂联合处理废水,回收Cu并生产铁红和媒染剂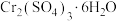 ,工艺流程如图:
,工艺流程如图:
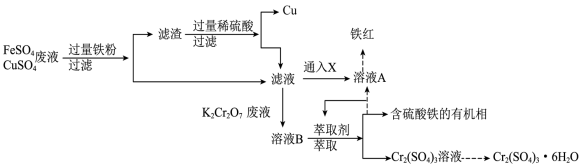
(1) 中Cr元素的化合价为
中Cr元素的化合价为__________ 。
(2)该工艺中多次用到过滤,过滤时需要的玻璃仪器除烧杯外还有__________ ,__________ 。
(3)滤液可以通入或加入X经一步转化为溶液A,X可以是下列选项中的哪些物质__________
A. B.
B. C.
C. D.
D. E.
E.
证明滤液中只含有 而不含
而不含 的实验方法是
的实验方法是__________ 。
(4)滤液与含 的废液反应的离子方程式为
的废液反应的离子方程式为__________ 。
(5)从 溶液制取
溶液制取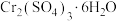 晶体的实验操作方法为
晶体的实验操作方法为__________ 、__________ 、过滤、洗涤、干燥。
(6)已知 化学性质与
化学性质与 类似,选择合适的化学试剂,先将流程中的
类似,选择合适的化学试剂,先将流程中的 溶液转化为氢氧化铬,再转化成可用于陶瓷和搪瓷的着色剂
溶液转化为氢氧化铬,再转化成可用于陶瓷和搪瓷的着色剂 。转化过程中发生的主要的方程式为:
。转化过程中发生的主要的方程式为:
离子方程式①__________ 化学方程式②__________ 。
 、
、 的电镀废液,皮革厂产生大量含
的电镀废液,皮革厂产生大量含 的废液。两厂联合处理废水,回收Cu并生产铁红和媒染剂
的废液。两厂联合处理废水,回收Cu并生产铁红和媒染剂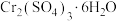 ,工艺流程如图:
,工艺流程如图:
(1)
 中Cr元素的化合价为
中Cr元素的化合价为(2)该工艺中多次用到过滤,过滤时需要的玻璃仪器除烧杯外还有
(3)滤液可以通入或加入X经一步转化为溶液A,X可以是下列选项中的哪些物质
A.
 B.
B. C.
C. D.
D. E.
E.
证明滤液中只含有
 而不含
而不含 的实验方法是
的实验方法是(4)滤液与含
 的废液反应的离子方程式为
的废液反应的离子方程式为(5)从
 溶液制取
溶液制取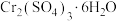 晶体的实验操作方法为
晶体的实验操作方法为(6)已知
 化学性质与
化学性质与 类似,选择合适的化学试剂,先将流程中的
类似,选择合适的化学试剂,先将流程中的 溶液转化为氢氧化铬,再转化成可用于陶瓷和搪瓷的着色剂
溶液转化为氢氧化铬,再转化成可用于陶瓷和搪瓷的着色剂 。转化过程中发生的主要的方程式为:
。转化过程中发生的主要的方程式为:离子方程式①
您最近一年使用:0次
5 . 向稀硝酸酸化的某溶液滴加AgNO3溶液,有白色沉淀生成,则该溶液一定含有
| A.Na+ | B.Cl- | C.Al3+ | D.CO |
您最近一年使用:0次
名校
解题方法
6 . 一定条件下,石墨转化为金刚石要吸收能量。在该条件下,下列结论正确的是
| A.金刚石比石墨稳定 |
| B.等质量的金刚石和石墨完全燃烧释放的热量相同 |
| C.金刚石转化为石墨是吸热反应 |
| D.1molC(金刚石)比1molC(石墨)的总能量高 |
您最近一年使用:0次
2024-04-02更新
|
467次组卷
|
20卷引用:天津市第二十五中学2023-2024学年高一下学期期中质量检测化学试卷
天津市第二十五中学2023-2024学年高一下学期期中质量检测化学试卷长春市榆树高级中学2020-2021学年高一下学期期中考试化学试题辽宁省大连市第一中学2020-2021学年高一下学期期中(合格性)考试化学试题(已下线)选择性必修1 期中检测(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)浙江省温州市平阳县万全综合高级中学2021-2022学年高二上学期期中考试化学试题(已下线)北京市第四中学2021-2022学年高一下学期期中考试化学试题湖南省长沙市长郡中学2022-2023学年高一下学期期中考试化学试题 北京市第五十五中学2022-2023学年高一下学期5月期中考试化学试题四川省甘孜藏族自治州某重点中学2023-2024学年高一下学期4月期中考试化学试题(已下线)专题04 化学反应与热能【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)(已下线)第一节 化学反应与能量的变化(第1课时 焓变 反应热)(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版选修4)人教2019版必修第二册第六章第一节 化学反应与能量变化课后习题黑龙江省大庆市大庆中学2021-2022学年高一下学期第一次月考化学试题黑龙江省饶河县高级中学2021-2022学年高一下学期学业水平(合格考)化学试题吉林省长春市第二实验中学2022-2023学年高一下学期4月月考化学试题贵州省黔西南州2022-2023学年高一下学期期末教学质量检测化学试题(已下线)热点04 化学能与热能新疆阿克苏市实验中学2022-2023学年高一下学期第三次月考化学试题四川省绵阳南山中学2023-2024学年高一下学期3月月考试题 化学试题山西省太原师范学院附属中学2023-2024学年高一下学期第二次月考化学试题
7 . 2020年世界环境日的宣传主题为“关爱自然,刻不容缓”。防治大气污染、水体污染等是世界各国保护环境的最重要课题。将CH4催化重整为可用的化学品,对改善环境意义重大。
(1)某科研团队利用Ni-CaO-Fe3O4三元催化剂在850℃下“超干重整”CH4和CO2。
已知:反应I:CH4(g)+CO2(g) 2CO(g)+2H2(g)ΔH=+247kJ/mol
2CO(g)+2H2(g)ΔH=+247kJ/mol
反应Ⅱ:CO(g)+H2O(g) CO2(g)+H2(g)ΔH=-41kJ/mol
CO2(g)+H2(g)ΔH=-41kJ/mol
则反应Ⅲ:CH4(g)+3CO2(g) 4CO(g)+2H2O(g)ΔH=
4CO(g)+2H2O(g)ΔH=_____ 。
(2)在容积为1L的刚性容器中进行“合成气催化重整”,反应的化学方程式为:CH4(g)+CO2(g) 2CO(g)+2H2(g),当投料n(CH4):n(CO2)=1.0时,CO2的平衡转化率(ɑ)与温度(T),初始压强(p)的关系如图所示,压强p1
2CO(g)+2H2(g),当投料n(CH4):n(CO2)=1.0时,CO2的平衡转化率(ɑ)与温度(T),初始压强(p)的关系如图所示,压强p1_____ (填”>“=”或“<”下同)p2;当温度为T3、压强为p1时,a点时的v正_____ v逆;在温度为T6,初始压强为p2时反应,该反应的K=_____ 。

(1)某科研团队利用Ni-CaO-Fe3O4三元催化剂在850℃下“超干重整”CH4和CO2。
已知:反应I:CH4(g)+CO2(g)
 2CO(g)+2H2(g)ΔH=+247kJ/mol
2CO(g)+2H2(g)ΔH=+247kJ/mol反应Ⅱ:CO(g)+H2O(g)
 CO2(g)+H2(g)ΔH=-41kJ/mol
CO2(g)+H2(g)ΔH=-41kJ/mol则反应Ⅲ:CH4(g)+3CO2(g)
 4CO(g)+2H2O(g)ΔH=
4CO(g)+2H2O(g)ΔH=(2)在容积为1L的刚性容器中进行“合成气催化重整”,反应的化学方程式为:CH4(g)+CO2(g)
 2CO(g)+2H2(g),当投料n(CH4):n(CO2)=1.0时,CO2的平衡转化率(ɑ)与温度(T),初始压强(p)的关系如图所示,压强p1
2CO(g)+2H2(g),当投料n(CH4):n(CO2)=1.0时,CO2的平衡转化率(ɑ)与温度(T),初始压强(p)的关系如图所示,压强p1
您最近一年使用:0次
8 . 探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=+40.9kJ·mol-1
(1)不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

其中纵坐标表示CO2平衡转化率的是图_____ (填“甲”或“乙”);压强p1、p2、p3由大到小的顺序为_____ ;图乙中T1温度时,三条曲线几乎交于一点的原因是_____ 。
(2)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_____(填标号)。
(3)反应ⅠCO2(g)+3H2(g)=CH3OH(g)+H2O(g)。最近采用真空封管法制备的磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:
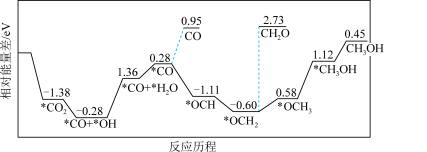
容易得到的副产物有CO和CH2O,其中相对较少的副产物为_____ ;上述合成甲醇的反应速率较慢,要使反应速率加快,主要降低下列变化中_____ (填字母)的能量变化。(双选)
A.*OCH3→*CH3OH B.*CO→*COH C.*OCH2→*OCH3 D.*CO+*OH→*CO+*H2O
Ⅰ.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49.5kJ·mol-1
Ⅱ.CO(g)+2H2(g)⇌CH3OH(g) ΔH2=-90.4kJ·mol-1
Ⅲ.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3=+40.9kJ·mol-1
(1)不同压强下,按照n(CO2)∶n(H2)=1∶3投料,实验测定CO2的平衡转化率和CH3OH的平衡产率随温度的变化关系如图所示。

其中纵坐标表示CO2平衡转化率的是图
(2)为同时提高CO2的平衡转化率和CH3OH的平衡产率,应选择的反应条件为_____(填标号)。
| A.低温、高压 | B.高温、低压 | C.低温、低压 | D.高温、高压 |
(3)反应ⅠCO2(g)+3H2(g)=CH3OH(g)+H2O(g)。最近采用真空封管法制备的磷化硼纳米颗粒,在发展非金属催化剂实现CO2电催化还原制备甲醇方向取得重要进展,该反应历程如图所示:

容易得到的副产物有CO和CH2O,其中相对较少的副产物为
A.*OCH3→*CH3OH B.*CO→*COH C.*OCH2→*OCH3 D.*CO+*OH→*CO+*H2O
您最近一年使用:0次
9 . 已知: ,电离度可表示电解质的相对强弱,电离度
,电离度可表示电解质的相对强弱,电离度 (已电离的电解质/原有电解质)×100%。已知25℃时醋酸的电离度是ɑ,
(已电离的电解质/原有电解质)×100%。已知25℃时醋酸的电离度是ɑ,
(1)电离平衡常数 的表达式是
的表达式是_____ ,
(2)物质的量浓度为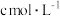 的醋酸的电离平衡常数
的醋酸的电离平衡常数 与电离度α的关系为
与电离度α的关系为
_____ (用含 的计算式表示)。
的计算式表示)。
 ,电离度可表示电解质的相对强弱,电离度
,电离度可表示电解质的相对强弱,电离度 (已电离的电解质/原有电解质)×100%。已知25℃时醋酸的电离度是ɑ,
(已电离的电解质/原有电解质)×100%。已知25℃时醋酸的电离度是ɑ,(1)电离平衡常数
 的表达式是
的表达式是(2)物质的量浓度为
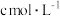 的醋酸的电离平衡常数
的醋酸的电离平衡常数 与电离度α的关系为
与电离度α的关系为
 的计算式表示)。
的计算式表示)。
您最近一年使用:0次
10 . 习近平总书记十分重视生态环境保护,多次对生态文明建设作出重要指示。试回答下列与环境有关的问题:
(1)在汽车排气系统中安装三元催化转化器,可发生下列反应:2NO(g)+2CO(g)⇌2CO2(g)+N2(g)。在某恒容密闭容器中通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如图所示:

该反应的正反应的ΔH_____ 0(填“>”或“<”)反应。
(2)汽车尾气是雾霾形成的原因之一、研究氮氧化物的处理方法可有效减少雾霾的形成,可采用氧化还原法脱硝:4NO(g)+4NH3(g)+O2(g) 4N2(g)+6H2O(g) ΔH<0
4N2(g)+6H2O(g) ΔH<0
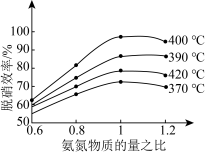
根据下图判断提高脱硝效率的最佳条件是_____ ;氨氮比一定时,在400℃时,脱硝效率最大,其可能的原因是_____ 。
(1)在汽车排气系统中安装三元催化转化器,可发生下列反应:2NO(g)+2CO(g)⇌2CO2(g)+N2(g)。在某恒容密闭容器中通入等物质的量的CO和NO,在不同温度(T)下发生上述反应时,c(CO)随时间(t)的变化曲线如图所示:

该反应的正反应的ΔH
(2)汽车尾气是雾霾形成的原因之一、研究氮氧化物的处理方法可有效减少雾霾的形成,可采用氧化还原法脱硝:4NO(g)+4NH3(g)+O2(g)
 4N2(g)+6H2O(g) ΔH<0
4N2(g)+6H2O(g) ΔH<0根据下图判断提高脱硝效率的最佳条件是

您最近一年使用:0次



