名校
解题方法
1 . 读下图信息,下列说法错误的是
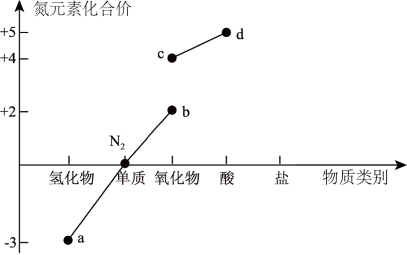
| A.a可经催化氧化生成b |
| B.b、c均为大气污染气体,在空气中可稳定存在 |
| C.Cu与d的浓溶液常温下反应可生成c |
| D.d的浓溶液保存在棕色试剂瓶中并放置在阴凉处 |
您最近一年使用:0次
2024-05-09更新
|
5次组卷
|
6卷引用:福建省福州第三中学2022-2023学年高一下学期期中考试化学试题
名校
2 . 下列物质在给定条件下能一步实现的是
A.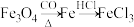 |
B.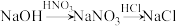 |
C.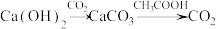 |
D.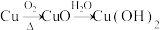 |
您最近一年使用:0次
名校
3 . 反应
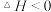 ,在恒容条件下进行。改变反应条件,在Ⅰ、Ⅱ、Ⅲ阶段中各物质浓度随时间变化的曲线如图所示:
,在恒容条件下进行。改变反应条件,在Ⅰ、Ⅱ、Ⅲ阶段中各物质浓度随时间变化的曲线如图所示:_____ 。
(2)A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小的排列顺序为_____ 。
(3)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是_____ ,其值是_____ %(保留2位有效数字)
(4)由第一次平衡到第二次平衡,平衡向_____ (填“左”或“右”)移动,采取的措施是_____ 。
(5)其他条件不变,只改变温度,则第Ⅱ阶段反应温度(T2)_____ 第Ⅲ阶段反应温度(T3)(填“<”或“>”或“=”),理由_____ 。

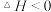 ,在恒容条件下进行。改变反应条件,在Ⅰ、Ⅱ、Ⅲ阶段中各物质浓度随时间变化的曲线如图所示:
,在恒容条件下进行。改变反应条件,在Ⅰ、Ⅱ、Ⅲ阶段中各物质浓度随时间变化的曲线如图所示:
(2)A的平均反应速率vⅠ(A)、vⅡ(A)、vⅢ(A)从大到小的排列顺序为
(3)B的平衡转化率αⅠ(B)、αⅡ(B)、αⅢ(B)中最小的是
(4)由第一次平衡到第二次平衡,平衡向
(5)其他条件不变,只改变温度,则第Ⅱ阶段反应温度(T2)
您最近一年使用:0次
名校
解题方法
4 . 以CO2和H2为原料制造更高价值的化学产品是用来缓解温室效应的研究方向。
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:
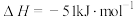
反应Ⅱ:
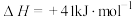
①已知几种化学键的键能如下表所示,则a=_____ kJ·mol-1.
②若反应Ⅱ逆反应活化能 ,则该反应的正反应的活化能
,则该反应的正反应的活化能
_____ kJ·mol-1.
(2)向2L容器中充入1molCO2和2molH2,若只发生反应I,测得反应在不同压强下平衡混合物中甲醇体积分数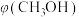 随温度变化如图1所示,逆反应速率与容器中
随温度变化如图1所示,逆反应速率与容器中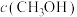 关系如图2所示:
关系如图2所示:
①图1中P1_____ P2(填“>”、“<”或“=”);
②图2中x点平衡体系时升温,反应重新达平衡状态时新平衡点可能是_____ (填字母序号)。 、
、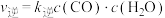 ,k正、k逆分别表示正逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lgk正随温度T变化关系的直线是
,k正、k逆分别表示正逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lgk正随温度T变化关系的直线是_____ ,表示lgk逆随温度T变化关系的直线是_____ 。
(4)已知一定温度下按照起始比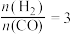 ,在一密闭容器中进行反应:
,在一密闭容器中进行反应: ,保持总压为2.1MPa不变,达到平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数
,保持总压为2.1MPa不变,达到平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数
_____ MPa-2(保留2位有效数字)(各气体分压=平衡体系中各气体的体积分数×总压)。
(5)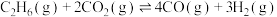
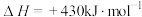 ,在四种不同容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是_____(填字母)。
,在四种不同容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是_____(填字母)。
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:

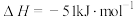
反应Ⅱ:

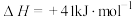
①已知几种化学键的键能如下表所示,则a=
| 化学键 | C—H | C—O | H—O | H—H | C≡O |
| 键能/kJ·mol-1 | 406 | 351 | 465 | 436 | a |
 ,则该反应的正反应的活化能
,则该反应的正反应的活化能
(2)向2L容器中充入1molCO2和2molH2,若只发生反应I,测得反应在不同压强下平衡混合物中甲醇体积分数
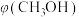 随温度变化如图1所示,逆反应速率与容器中
随温度变化如图1所示,逆反应速率与容器中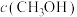 关系如图2所示:
关系如图2所示:①图1中P1
②图2中x点平衡体系时升温,反应重新达平衡状态时新平衡点可能是

 、
、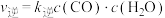 ,k正、k逆分别表示正逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lgk正随温度T变化关系的直线是
,k正、k逆分别表示正逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lgk正随温度T变化关系的直线是(4)已知一定温度下按照起始比
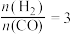 ,在一密闭容器中进行反应:
,在一密闭容器中进行反应: ,保持总压为2.1MPa不变,达到平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数
,保持总压为2.1MPa不变,达到平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数
(5)
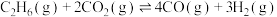
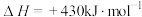 ,在四种不同容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是_____(填字母)。
,在四种不同容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是_____(填字母)。| A.恒温恒容容器 | B.恒容绝热容器 |
| C.恒压绝热容器 | D.恒温恒压容器 |
您最近一年使用:0次
名校
5 . 下列有关实验探究方案设计合理的是
| 选项 | 实验方案 | 实验目的 |
| A | 向等体积等浓度的H2O2溶液中分别加入5滴等浓度的CuSO4和FeCl3溶液,观察气体产生的速率 | 比较Cu2+和Fe3+的催化效果 |
| B | 先将注射器充满NO2气体,然后将活塞往里推,压缩体积,观察注射器内气体颜色先变深后变浅 | 验证压强对平衡的影响 |
| C | 在锥形瓶内各盛有2g锌粒(颗粒大小基本相同),然后通过分液漏斗分别加入40mL1mol·L-1和40mL18mol·L-1的硫酸,比较两者收集10mL氢气所用的时间
| 探究硫酸浓度对反应速率的影响 |
| D | 在 平衡体系中加入KCl晶体,观察并比较实验现象 平衡体系中加入KCl晶体,观察并比较实验现象 | 探究离子浓度对平衡移动的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
6 . 铬及其化合物在催化、金属防腐等方面具有重要应用。催化剂Cr2O3可由(NH4)2Cr2O7加热分解制备,反应同时生成无污染气体。
(1)完成化学方程式:_____ 。
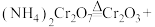 _____+_____。
_____+_____。
(2)Cr2O3催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为_____ (列式表示)。_____ (用“→”表示含氮物质间的转化);其中一个有颜色变化的反应的化学方程式为_____ 。
(1)完成化学方程式:
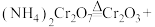 _____+_____。
_____+_____。(2)Cr2O3催化丙烷脱氢过程中,部分反应历程如图,
 过程的焓变为
过程的焓变为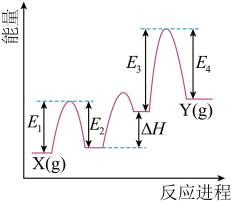
您最近一年使用:0次
名校
7 . 在一定温度下,向2L恒容密闭容器中加入1molHI,发生反应:
 ,H2的物质的量随时间变化如表,下列说法正确的是
,H2的物质的量随时间变化如表,下列说法正确的是

 ,H2的物质的量随时间变化如表,下列说法正确的是
,H2的物质的量随时间变化如表,下列说法正确的是| t/min | 1 | 2 | 3 |
| n(H2)/mol | 0.06 | 0.1 | 0.1 |
| A.反应前1min平均速率v(HI)=0.06mol⋅L-1⋅min-1 |
| B.该温度下,平衡时HI的转化率为10% |
| C.该温度下的平衡常数为K1,温度升高10℃后平衡常数为K2,则K1>K2 |
| D.达平衡后其他条件不变,压缩容器体积,平衡不移动,c(HI)不变 |
您最近一年使用:0次
名校
解题方法
8 . 灰锡结构松散,不能用于制造器皿。现把白锡制造的器皿在0℃、100kPa环境下存放,它会不会变成灰锡而不能继续使用呢?(已知在0℃、100kPa条件下白锡转化为灰锡的反应的焓变和熵变分别为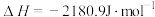 ,
, ,当
,当 时能自发反应)
时能自发反应)
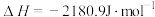 ,
, ,当
,当 时能自发反应)
时能自发反应)| A.会变 | B.不会变 | C.不能确定 | D.升高温度才会变 |
您最近一年使用:0次
名校
9 . 恒温下,反应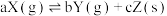 达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
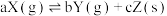 达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是
达到平衡状态,把容器容积缩小到原来的一半,且达到新的平衡状态时,X的物质的量浓度从0.1mol·L-1增大到0.19mol·L-1。下列判断中正确的是| A.a>b | B.a<b+c | C.a=b+c | D.a<b |
您最近一年使用:0次
2024-04-21更新
|
73次组卷
|
2卷引用:福建师范大学附属中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
10 . 在 反应中,表示该反应速率最快的是
反应中,表示该反应速率最快的是
 反应中,表示该反应速率最快的是
反应中,表示该反应速率最快的是A. | B.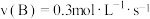 |
C. | D. |
您最近一年使用:0次
2024-04-21更新
|
414次组卷
|
2卷引用:福建师范大学附属中学2023-2024学年高二上学期期中考试化学试题




