解题方法
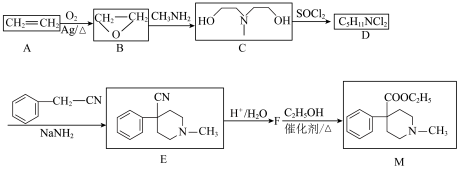
1 . 有机物M( )是一种合成镇痛药的主要成分。某小组设计了如下图所示的合成路线:
)是一种合成镇痛药的主要成分。某小组设计了如下图所示的合成路线:
已知:①RCN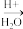 R一COOH
R一COOH
②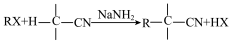
(1)B的化学名称为___________ ,B中官能团的名称为___________ 。
(2)D的结构简式为___________ ,C→D该反应的反应类型为___________ ,-CN中碳原子的杂化方式为___________ 。
(3)F→M的化学反应方程式为___________ 。
(4)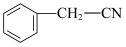 有多种同分异构体。其同分异构体中同时含有苯环和碳碳三键的结构有
有多种同分异构体。其同分异构体中同时含有苯环和碳碳三键的结构有___________ 种,请写出其中核磁共振氢谱有四组峰,峰面积之比为1∶2∶2∶2的所有同分异构体的结构简式:___________ 。
(5)请参照上述合成路线,设计以 、CH3-CN和CH3CH2NH2为原料制备
、CH3-CN和CH3CH2NH2为原料制备 的合成路线(无机试剂任选):
的合成路线(无机试剂任选):___________ 。
 )是一种合成镇痛药的主要成分。某小组设计了如下图所示的合成路线:
)是一种合成镇痛药的主要成分。某小组设计了如下图所示的合成路线:
已知:①RCN
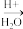 R一COOH
R一COOH②
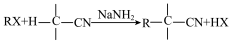
(1)B的化学名称为
(2)D的结构简式为
(3)F→M的化学反应方程式为
(4)
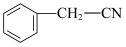 有多种同分异构体。其同分异构体中同时含有苯环和碳碳三键的结构有
有多种同分异构体。其同分异构体中同时含有苯环和碳碳三键的结构有(5)请参照上述合成路线,设计以
 、CH3-CN和CH3CH2NH2为原料制备
、CH3-CN和CH3CH2NH2为原料制备 的合成路线(无机试剂任选):
的合成路线(无机试剂任选):
您最近一年使用:0次
2 . 钛和钛的化合物在航天、化工、建筑、日常生活中都有着广泛的用途。请回答下列问题:
(1)钛在周期表中的位置是___________ 。
(2)钛的一种常见化合物是[Ti(H2O)6]Cl3,1mol该物质中含有σ键的数目为___________ NA,配体H2O的VSEPR模型是___________ 。
(3)常温下,TiCl4是易溶于CCl4.易挥发的无色液体。TiCl4挥发过程中破坏的作用力类型是___________ 。
(4)已知:TiCl4(g)+O2(g)⇌TiO2(s)+2Cl2(g) ΔH1=-175.4kJ·mol-1 I
2C(s)+O2(g)⇌2CO(g) ΔH2=-220.9kJ·mol-1 Ⅱ
①TiCl4(g)与CO(g)反应生成TiO2(s)、C(s)和氯气的热化学方程式为___________ 。升高温度对该反应的影响为___________ 。
②t℃时,向10L恒容密闭容器中充入1molTiCl4和2molO2发生反应I.5min时达到平衡,测得TiO2的物质的量为0.2mol。0~5min内,用Cl2表示的反应速率v(Cl2)=___________ ,TiCl4的平衡转化率为___________ 。
(5)氮化钛(TiN)晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体结构与NaCl相同,则该晶体中阳离子的配位数为___________ 。已知该晶体的晶胞参数为423.5pm,其晶体密度为___________ g/cm3(写出表达式即可)。
(1)钛在周期表中的位置是
(2)钛的一种常见化合物是[Ti(H2O)6]Cl3,1mol该物质中含有σ键的数目为
(3)常温下,TiCl4是易溶于CCl4.易挥发的无色液体。TiCl4挥发过程中破坏的作用力类型是
(4)已知:TiCl4(g)+O2(g)⇌TiO2(s)+2Cl2(g) ΔH1=-175.4kJ·mol-1 I
2C(s)+O2(g)⇌2CO(g) ΔH2=-220.9kJ·mol-1 Ⅱ
①TiCl4(g)与CO(g)反应生成TiO2(s)、C(s)和氯气的热化学方程式为
②t℃时,向10L恒容密闭容器中充入1molTiCl4和2molO2发生反应I.5min时达到平衡,测得TiO2的物质的量为0.2mol。0~5min内,用Cl2表示的反应速率v(Cl2)=
(5)氮化钛(TiN)晶体呈金黄色,化学稳定性好,可应用于超导材料。已知氮化钛晶体结构与NaCl相同,则该晶体中阳离子的配位数为
您最近一年使用:0次
3 . 3-苯基乳酸是一些重要的化学合成物的前体,并广泛应用于医药、化工、生物合成等领域,可作为日常食品的防腐剂。实验室通过苯丙氨酸的重氮化及水解反应制取3-苯基乳酸,方法如下:
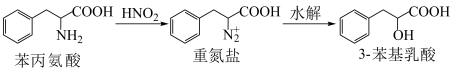
已知:HNO2(M=47)为弱酸,不稳定,遇热即分解,水溶液无色;苯丙氨酸(M=165)为白色固体,溶于水,熔点283℃;3−苯基乳酸(M=166)为白色晶体,微溶于水,易溶于有机溶剂,熔点121~126℃。
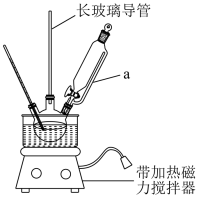
实验步骤:
①三颈烧瓶中加入6.0g苯丙氨酸,再加入70mL稀硫酸,冷却至5℃,边搅拌边滴加60mLNaNO2溶液(0.1g·mL-1),维持温度搅拌50min,然后改成35℃热水浴再搅拌10min。
②往烧瓶中加入25mL乙酸乙酯,搅拌后将混合液中的水分离,进一步提纯得到粗产品5.0g。
③取粗产品0.5g于锥形瓶中,加入1mL95%的乙醇,溶解后再加入25mL蒸馏水、2滴酚酞试剂,用0.1mol·L-1NaOH标准溶液滴定至终点,重复3次实验,平均消耗V(NaOH)=28.10mL。
(1)仪器a的名称为___________ ,配制60mL0.1g·mL-1NaNO2溶液需要的玻璃仪器有___________ 、胶头滴管、玻璃棒、烧杯。
(2)加入稀硫酸的作用是___________ ,生成重氮盐之前涉及反应的化学方程式为___________ 。
(3)步骤①中先在5℃下搅拌50min,采用较低温度较长时间反应的原因是___________ 。
(4)步骤②中乙酸乙酯的作用是___________ ,后续提纯粗产品的方法是___________ 。
(5)判断滴定终点的现象是___________ 粗产品的纯度是___________ (保留3位有效数字)。

已知:HNO2(M=47)为弱酸,不稳定,遇热即分解,水溶液无色;苯丙氨酸(M=165)为白色固体,溶于水,熔点283℃;3−苯基乳酸(M=166)为白色晶体,微溶于水,易溶于有机溶剂,熔点121~126℃。

实验步骤:
①三颈烧瓶中加入6.0g苯丙氨酸,再加入70mL稀硫酸,冷却至5℃,边搅拌边滴加60mLNaNO2溶液(0.1g·mL-1),维持温度搅拌50min,然后改成35℃热水浴再搅拌10min。
②往烧瓶中加入25mL乙酸乙酯,搅拌后将混合液中的水分离,进一步提纯得到粗产品5.0g。
③取粗产品0.5g于锥形瓶中,加入1mL95%的乙醇,溶解后再加入25mL蒸馏水、2滴酚酞试剂,用0.1mol·L-1NaOH标准溶液滴定至终点,重复3次实验,平均消耗V(NaOH)=28.10mL。
(1)仪器a的名称为
(2)加入稀硫酸的作用是
(3)步骤①中先在5℃下搅拌50min,采用较低温度较长时间反应的原因是
(4)步骤②中乙酸乙酯的作用是
(5)判断滴定终点的现象是
您最近一年使用:0次
4 . 高品质MnO2可用于生产锂离子电池正极材料锰酸锂。以软锰矿与黄铁矿为主要原料,采用“两矿一步浸出法”制备高品质MnO2的工艺流程如下图所示:
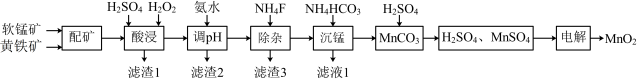
已知:①软锰矿与黄铁矿的主要成分分别为MnO2、FeS2,还含少量Fe、Ca、Mg、Al、Si等元素的氧化物;
②该工艺条件下,相关金属离子完全形成氢氧化物沉淀的pH如下:
回答下列问题:
(1)基态Fe2+的价电子轨道表示式为___________ 。
(2)“酸浸”操作中需先后分批加入H2SO4、H2O2。已知滤渣1的主要成分为S、SiO2、CaSO4等。加入H2SO4后发生反应生成单质S的离子方程式为___________ 。加入H2SO4后反应的生成物会附着在矿粉颗粒表面,使上述反应受阻,此时加入H2O2,利用其迅速分解产生的大量气泡可破除该不利影响。导致H2O2迅速分解的因素是___________ 。
(3)“调pH”时调节溶液pH范围为4.7~6.0,此时“滤渣2”的主要成分为________ (填化学式)。
(4)“除杂”时,溶液体系中的Ca2+和Mg2+形成氟化物沉淀。若沉淀后上层清液中c(F-)=0.05mol·L-1,则
___________ [已知Ksp(MgF2)=5.0×10-11,Ksp(CaF2)=2.5×10-9]。
(5)“沉锰”步骤发生主要反应的离子方程式为___________ 。
(6)利用惰性电极电解H2SO4-MnSO4-H2O体系可获得MnO2,阳极的电极反应式为___________ 。电解过程的机理(部分)如图甲所示,硫酸浓度与电流效率的关系如图乙所示。硫酸浓度超过3.0mol/L时,电流效率降低的原因是___________ 。


已知:①软锰矿与黄铁矿的主要成分分别为MnO2、FeS2,还含少量Fe、Ca、Mg、Al、Si等元素的氧化物;
②该工艺条件下,相关金属离子完全形成氢氧化物沉淀的pH如下:
| 金属离子 | Fe2+ | Fe3+ | Mn2+ | Mg2+ | Al3+ |
| 开始沉淀pH | 6.9 | 1.9 | 6.6 | 9.1 | 3.4 |
| 沉淀完全(c=1.0×10-5mol·L-1)的pH | 8.3 | 3.2 | 10.1 | 10.9 | 4.7 |
(1)基态Fe2+的价电子轨道表示式为
(2)“酸浸”操作中需先后分批加入H2SO4、H2O2。已知滤渣1的主要成分为S、SiO2、CaSO4等。加入H2SO4后发生反应生成单质S的离子方程式为
(3)“调pH”时调节溶液pH范围为4.7~6.0,此时“滤渣2”的主要成分为
(4)“除杂”时,溶液体系中的Ca2+和Mg2+形成氟化物沉淀。若沉淀后上层清液中c(F-)=0.05mol·L-1,则

(5)“沉锰”步骤发生主要反应的离子方程式为
(6)利用惰性电极电解H2SO4-MnSO4-H2O体系可获得MnO2,阳极的电极反应式为

您最近一年使用:0次
2023-05-21更新
|
413次组卷
|
3卷引用:山西省阳泉市2023届高三下学期第三次模拟测试理综化学试题
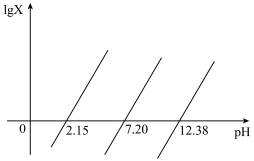
5 . H3PO4是一种三元酸。室温下,向0.1mol·L-1的H3PO4溶液中滴加NaOH溶液调节pH值。混合溶液中lgX[表示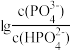 、
、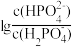 、
、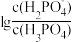 )]随溶液pH值的变化如图所示。下列说法不正确的是
)]随溶液pH值的变化如图所示。下列说法不正确的是
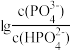 、
、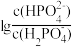 、
、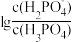 )]随溶液pH值的变化如图所示。下列说法不正确的是
)]随溶液pH值的变化如图所示。下列说法不正确的是
| A.室温下Na2HPO4溶液显碱性 |
| B.H3PO4二级电离常数Ka2的数量级为10-8 |
C.随着pH增大,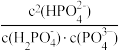 比值不断减小 比值不断减小 |
D.pH=2.15时,c(Na+)+c(H+)=c( )+2c( )+2c( )+3c( )+3c( )+c(OH-) )+c(OH-) |
您最近一年使用:0次
6 . 对下列实验操作和现象的解释或结论正确的是
| 实验操作 | 现象 | 解释或结论 | |
| A | 向盛有10mL0.01mol·L-1AgNO3溶液的试管中滴加1mL0.01mol·L-1NaCl溶液,再向其中滴加1mL0.01mol·L-1KI溶液 | 先产生白色沉淀,后产生黄色沉淀 | 常温下Ksp(AgCl)>Ksp(AgI) |
| B | 向浓盐酸中加入少量碳酸钠溶液,将产生的气体通入苯酚钠溶液 | 苯酚钠溶液中出现白色浑浊 | 可以证明酸性:盐酸>碳酸>苯酚 |
| C | 在酸性KMnO4溶液中通入SO2 | 溶液褪色 | SO2具有漂白性 |
| D | 压缩装有NO2和N2O4混合气体(已达平衡)的容器 | 气体颜色先变深后稍变浅 | 平衡向生成N2O4的方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
7 . 下图是我国科研工作者研究MgO(s)与CH4(g)作用最终生成Mg(s)与CH3OH (g)的物质相对能量-反应进程曲线。下列叙述错误的是
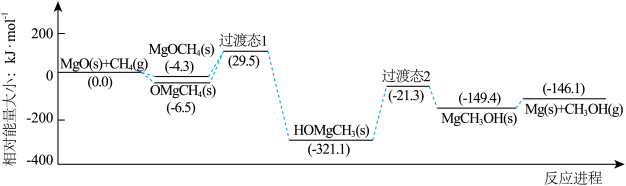
| A.中间体OMgCH4(s)比MgOCH4(s)更稳定 |
| B.该反应进程中的最大能垒(活化能)为350.6 kJ·mol-1 |
| C.生成HOMgCH3(s)的过程中有极性键的断裂和形成 |
| D.总反应的热化学方程式为MgO(s)+CH4(g)=Mg(s)+CH3OH (g) ΔH=-146.1kJ·mol-1 |
您最近一年使用:0次
2023-04-12更新
|
792次组卷
|
11卷引用:山西省阳泉市2023届高三下学期第三次模拟测试理综化学试题
山西省阳泉市2023届高三下学期第三次模拟测试理综化学试题安徽省合肥市2023届高三第一次教学质量检测 化学试题(已下线)化学-2023年高考押题预测卷02(天津卷)(含考试版、全解全析、参考答案、答题卡)(已下线)专题07 化学反应中的能量变化(已下线)素养卷02 循环转化过渡态理论图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)回归教材重难点08 聚焦热、速率、平衡-【查漏补缺】2023年高考化学三轮冲刺过关(新高考专用)湖南省衡阳市第一中学2023届高三下学期5月月考化学试题辽宁省铁岭市昌图县第一高级中学2022-2023学年高一下学期期末考试化学试题安徽省合肥市第一中学2023-2024学年高二上学期10月素质拓展(二)化学试题甘肃省兰州第一中学2023-2024学年高三上学期第三次月考化学试题浙江省杭州市富阳区场口中学2023-2024学年高二下学期3月月考化学试题
名校
解题方法
8 . 利用3-苯基丙酸催化脱氢制备异肉桂酸的反应如下所示,下列叙述错误的是
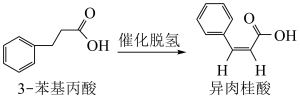

| A.上述制备过程属于氧化反应 |
B.3-苯基丙酸的分子式为 |
| C.异肉桂酸分子中最多有9个碳原子共面 |
D. 异肉桂酸最多与 异肉桂酸最多与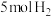 发生加成反应 发生加成反应 |
您最近一年使用:0次
2023-02-12更新
|
1114次组卷
|
5卷引用:山西省阳泉市2023届高三下学期第三次模拟测试理综化学试题
山西省阳泉市2023届高三下学期第三次模拟测试理综化学试题安徽省合肥市2023届高三第一次教学质量检测 化学试题(已下线)先机卷 04 -【热题狂飙】2023年高考化学样卷(全国卷专用)(已下线)专题09 有机化学基础湖南省衡阳市第一中学2023届高三下学期5月月考化学试题
9 . 紫薯含 、
、 等多种矿物元素,富含维生素C(具有较强还原性)等维生素,特别是含有大量花青素(花青素与石蕊类似,是一种天然指示剂)。下列叙述正确的是
等多种矿物元素,富含维生素C(具有较强还原性)等维生素,特别是含有大量花青素(花青素与石蕊类似,是一种天然指示剂)。下列叙述正确的是
 、
、 等多种矿物元素,富含维生素C(具有较强还原性)等维生素,特别是含有大量花青素(花青素与石蕊类似,是一种天然指示剂)。下列叙述正确的是
等多种矿物元素,富含维生素C(具有较强还原性)等维生素,特别是含有大量花青素(花青素与石蕊类似,是一种天然指示剂)。下列叙述正确的是| A.紫薯熬粥颜色很深,滴加几滴老陈醋,搅拌一下,粥就变成了红色 |
B. 是一种对人有益的过渡元素,适量的 是一种对人有益的过渡元素,适量的 有利于提高人体免疫力 有利于提高人体免疫力 |
| C.将紫薯煮熟,趁热滴加碘水,紫薯会变蓝 |
| D.紫薯所含淀粉和纤维素属于同分异构体 |
您最近一年使用:0次
2023-01-04更新
|
579次组卷
|
2卷引用:山西省阳泉市2023届高三下学期第三次模拟测试理综化学试题
名校
10 . 短周期元素X、Y、Z、W是同周期主族元素,W元素形成的某种单质具有强氧化性,可用于杀菌消毒。四种元素与锂组成的盐是一种新型的锂离子电池的电解质,结构如图所示,下列说法正确的是
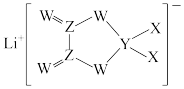
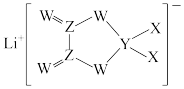
| A.同周期中第一电离能比W元素小的有5种 |
| B.该物质中含有1mol配位键 |
| C.基态X原子核外电子的空间运动状态有5种 |
| D.Y元素的最高价氧化物的水化物中Y元素的杂化方式为sp3杂化 |
您最近一年使用:0次
2022-03-29更新
|
372次组卷
|
3卷引用:山西省阳泉市2023届高三下学期第三次模拟测试理综化学试题



