解题方法
1 . 化合物G是一种药物合成中间体,其合成路线如下:
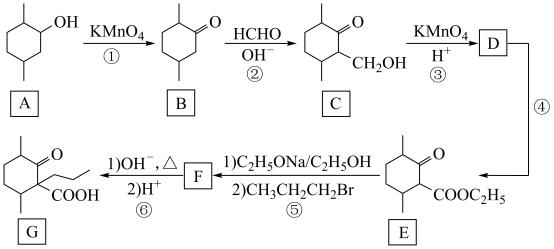
回答下列问题:
(1)A的名称是___________ ;C中的官能团名称是___________ 。
(2)②的反应类型是___________ ;写出D的结构简式,用星号(*)标出D中的手性碳原子___________ 。(碳原子上连有4个不同的原子或基团时,该碳称为手性碳)
(3)具有六元环结构、且环上只有1个取代基,并能与NaOH溶液发生反应的C的同分异构体有___________ 种;写出能发生银镜反应的同分异构体的结构简式___________ 。(不考虑立体异构)
(4)写出F到G的反应方程式___________ 、___________ 。
(5)参照化合物G合成线路,设计由甲苯和乙酰乙酸乙酯(CH3COCH2COOC2H5)制备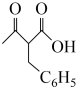 的合成路线
的合成路线___________ (无机试剂任选)。

回答下列问题:
(1)A的名称是
(2)②的反应类型是
(3)具有六元环结构、且环上只有1个取代基,并能与NaOH溶液发生反应的C的同分异构体有
(4)写出F到G的反应方程式
(5)参照化合物G合成线路,设计由甲苯和乙酰乙酸乙酯(CH3COCH2COOC2H5)制备
 的合成路线
的合成路线
您最近一年使用:0次
名校
2 . 氯化亚砜(SOCl2)是一种液态化合物,沸点为79℃,在农药、制药行业中用途广泛。SOCl2遇水剧烈反应,液面上产生白雾,并带有刺激性气味的气体产生。
(1)用三氧化硫、硫黄(S)和液氯为原料可以在一定条件合成二氯亚砜,反应物原子全部被利用,则三者的物质的量比为___________ 。
(2)①蒸干MgCl2溶液不能得到无水MgCl2,用SOCl2与MgCl2·6H2O混合加热。可得到无水MgCl2,写出反应的化学方程式___________ 。
②SOCl2与FeCl3·6H2O混合加热不宜制取无水FeCl3,是因为___________ 。
(3)制药厂可用阿司匹林和氯化亚砜合成乙酰水杨酰氯( ),实验室模拟制备乙酰水杨酰氯的装置与操作步骤如图:
),实验室模拟制备乙酰水杨酰氯的装置与操作步骤如图:

步骤1:取36.0g阿司匹林( )置于三颈烧瓶中,加入2~3滴DMF;
)置于三颈烧瓶中,加入2~3滴DMF;
步骤2:向三颈烧瓶中滴加氯化亚砜(SOCl2);
步骤3:70℃条件下充分反应后,除去过量的SOCl2,经一系列操作即可得到乙酰水杨酰氯。
已知:反应原理为 +SOCl2
+SOCl2
 +SO2↑+HCl↑;
+SO2↑+HCl↑;
有关物质的沸点如表:
回答下列问题:
①仪器M的名称为___________ ;干燥管中的无水CaCl2若更换为___________ 试剂,则可省去尾气吸收的NaOH溶液及其装置;若省去N,,三颈烧瓶中会产生___________ 现象。
②反应温度适宜选取70℃的原因是___________ ;除去过量SOCl2宜采用___________ 方法;反应最终得到12.9g纯净的 ,则该实验过程中
,则该实验过程中 的产率为
的产率为___________ %(保留3位有效数字)。
(1)用三氧化硫、硫黄(S)和液氯为原料可以在一定条件合成二氯亚砜,反应物原子全部被利用,则三者的物质的量比为
(2)①蒸干MgCl2溶液不能得到无水MgCl2,用SOCl2与MgCl2·6H2O混合加热。可得到无水MgCl2,写出反应的化学方程式
②SOCl2与FeCl3·6H2O混合加热不宜制取无水FeCl3,是因为
(3)制药厂可用阿司匹林和氯化亚砜合成乙酰水杨酰氯(
 ),实验室模拟制备乙酰水杨酰氯的装置与操作步骤如图:
),实验室模拟制备乙酰水杨酰氯的装置与操作步骤如图:
步骤1:取36.0g阿司匹林(
 )置于三颈烧瓶中,加入2~3滴DMF;
)置于三颈烧瓶中,加入2~3滴DMF;步骤2:向三颈烧瓶中滴加氯化亚砜(SOCl2);
步骤3:70℃条件下充分反应后,除去过量的SOCl2,经一系列操作即可得到乙酰水杨酰氯。
已知:反应原理为
 +SOCl2
+SOCl2
 +SO2↑+HCl↑;
+SO2↑+HCl↑;有关物质的沸点如表:
| 物质 | SOCl2 | 阿司匹林 | 乙酰水杨酰氯 |
| 沸点/℃ | 79 | 321 | 107~110 |
①仪器M的名称为
②反应温度适宜选取70℃的原因是
 ,则该实验过程中
,则该实验过程中 的产率为
的产率为
您最近一年使用:0次
2022-01-27更新
|
492次组卷
|
5卷引用:甘肃省金昌市2021-2022学年高三上学期第一次联考理科综合化学试题
名校
解题方法
3 . 金属回收与利用有利于环境保护,镉可用于制造体积小和电容量大的电池。铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质,湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如下:
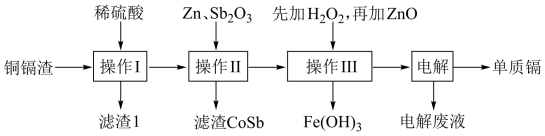
下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度均为0.1mol·L-1)
(1)滤渣Ⅰ可用硫酸酸化的双氧水浸取经结晶制取胆矾,试写出浸取过程离子方程式___________ 。
(2)操作Ⅱ“除钴”时,向含Co2+的浸液中加入Zn和Sb2O3,恰好产生CoSb合金,写出该反应的化学方程式:___________ 。
(3)操作Ⅲ加入ZnO控制反应液的pH范围为___________ ;若加入的H2O2不足,加入ZnO后所得的电解液中会含有Fe元素。请设计实验方案加以检验:___________ 。
(4)“电解”过程中以石墨为电极得到粗镉,电解阳极反应式为___________ ;电解废液最好在___________ 加入循环利用。(选择“操作I”、“操作Ⅱ”、“操作Ⅲ”、“电解”工序名称填入横线上)
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的阳极反应式为___________ ;如果用生石灰处理含Cd2+(2.88×10-4mol/L)的电解废液。常温下,当pH=10时,镉的去除率为___________ 。(用百分数表达,小数点后两位有效数字。已知常温下,Ksp[Cd(OH)2]=7.2×10-15)

下表列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度均为0.1mol·L-1)
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cd(OH)2 |
| 开始沉淀的pH | 1.7 | 6.3 | 7.5 |
| 沉淀完全的pH | 2.8 | 8.4 | 9.3 |
(2)操作Ⅱ“除钴”时,向含Co2+的浸液中加入Zn和Sb2O3,恰好产生CoSb合金,写出该反应的化学方程式:
(3)操作Ⅲ加入ZnO控制反应液的pH范围为
(4)“电解”过程中以石墨为电极得到粗镉,电解阳极反应式为
(5)回收所得的Cd可用于制造镍镉碱性二次电池,电池工作时,正极NiO(OH)转化为Ni(OH)2,则充电时电池的阳极反应式为
您最近一年使用:0次
2022-01-27更新
|
697次组卷
|
6卷引用:甘肃省金昌市2021-2022学年高三上学期第一次联考理科综合化学试题
甘肃省金昌市2021-2022学年高三上学期第一次联考理科综合化学试题(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)安徽省滁州市定远县育才学校2021-2022学年高三下学期开学考试理科综合化学试题湖南省常德市鼎城一中2022-2023学年高三第五次月考化学试题(已下线)T27-工业流程题
4 . 气候变化是人类面临的全球性问题,碳中和的含义是减少含碳温室气体的排放,采用合适的技术固碳,最终达到平衡。世界各国以全球协约的方式减排温室气体,中国承诺2030年前,二氧化碳的排放不再增长,达到峰值之后逐步降低。
(1)我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。下列措施对实现“碳中和”不 具有直接贡献的是
(2)二氧化碳加氢制备甲醇既可实现二氧化碳的资源化利用,又可有效缓解温室效应问题。
已知:(I)CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+42.3kJ/mol
(II)CH3OH(g)=CO(g)+2H2(g) ΔH2
(Ⅲ)CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH3=-49.4 kJ/mol
①ΔH2=___________ ;上述3个反应一定不能自发进行有___________ (填反应序号)。
②在260℃、5MPa恒容条件下发生反应(Ⅲ),原料气体积组成为V(CO2)∶V(H2)∶V(N2)=1∶3∶1,平衡时CO2的转化率为50%,则H2的压强为___________ ,反应(Ⅲ)的平衡常数:Kp=___________ (MPa)-2(计算结果精确至小数点后两位,用平衡分压代替平衡浓度计算,分压=总压x物质的量分数)。
(3)温室气体的利用是当前环境和能源领域的研究热点,Ni-CeO2催化CO2加H2形成CH4的反应历程如图1所示(吸附在催化剂表面的物种用*标注),含碳产物中CH4的物质的量百分数(Y)及CO2的转化率随温度的变化如图2所示。

①下列对CO2甲烷化反应体系的说法不合理的有___________ 。
A.存在副反应CO2+ H2 CO+ H2O
CO+ H2O
B.存在反应CO2+4H2 CH4 + 2H2O
CH4 + 2H2O
C.含碳副产物的产率均高于CH4
D.温度高于260℃后,升高温度,甲烷产率几乎不变
②CO2甲烷化的过程中,保持CO2与H2的体积比为1:5,反应气的总流量控制在36 mL·min-1,260 ℃时测得CO2转化率为40%,则H2反应速率为___________ mL·min-1。
(1)我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。下列措施对实现“碳中和”
| A.采取节能低碳生活方式 | B.推行生活垃圾分类 |
| C.植树造林增加绿色植被 | D.燃煤锅炉改烧天然气 |
已知:(I)CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+42.3kJ/mol
(II)CH3OH(g)=CO(g)+2H2(g) ΔH2
(Ⅲ)CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH3=-49.4 kJ/mol
①ΔH2=
②在260℃、5MPa恒容条件下发生反应(Ⅲ),原料气体积组成为V(CO2)∶V(H2)∶V(N2)=1∶3∶1,平衡时CO2的转化率为50%,则H2的压强为
(3)温室气体的利用是当前环境和能源领域的研究热点,Ni-CeO2催化CO2加H2形成CH4的反应历程如图1所示(吸附在催化剂表面的物种用*标注),含碳产物中CH4的物质的量百分数(Y)及CO2的转化率随温度的变化如图2所示。

①下列对CO2甲烷化反应体系的说法不合理的有
A.存在副反应CO2+ H2
 CO+ H2O
CO+ H2OB.存在反应CO2+4H2
 CH4 + 2H2O
CH4 + 2H2OC.含碳副产物的产率均高于CH4
D.温度高于260℃后,升高温度,甲烷产率几乎不变
②CO2甲烷化的过程中,保持CO2与H2的体积比为1:5,反应气的总流量控制在36 mL·min-1,260 ℃时测得CO2转化率为40%,则H2反应速率为
您最近一年使用:0次
2022-01-27更新
|
286次组卷
|
2卷引用:甘肃省金昌市2021-2022学年高三上学期第一次联考理科综合化学试题
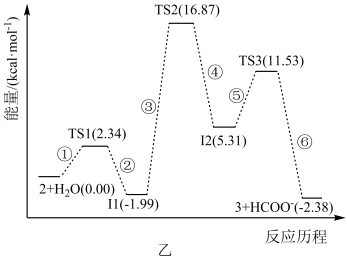
5 . 科学家已经成功地利用二氧化碳催化氢化获得甲酸,利用化合物1催化氢化二氧化碳的反应过程如图甲所示,其中化合物2与水反应变成化合物3,化合物3与 的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法错误的是
的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法错误的是
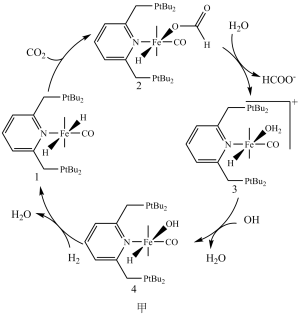
 的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法错误的是
的反应历程如图乙所示,其中TS表示过渡态,Ⅰ表示中间体。下列说法错误的是

A.从平衡移动的角度看,降低温度可促进化合物2与水反应变成化合物3与 |
| B.使用更高效的催化剂可以降低反应所需的活化能,最终提高二氧化碳的转化率 |
| C.该历程中最大能垒(活化能)E(正)=18.86Kcal/mol |
| D.化合物1到化合物2的过程中存在碳氧键的断裂和碳氢键的形成 |
您最近一年使用:0次
名校
6 . 常温下,向某浓度的二元弱酸H2A溶液中逐滴加入NaOH溶液,pC与溶液pH的变化关系如图所示(pC=-lgx,x表示溶液中溶质微粒的物质的量浓度)。下列说法正确的是


| A.pH由2增大到3的过程中,水的电离程度先减小后增大 |
| B.溶液中存在点d满足3[c(H2A)+c(HA-)+c(A2-)] = 2c(Na+),该点位于b、c之间 |
| C.pH=3时,溶液中c(HA-)= c(A2-) > c(H2A) |
| D.常温下,溶液中c(H2A)·c(A2-)与c2(HA-)的比值为104.5 |
您最近一年使用:0次
2022-01-27更新
|
645次组卷
|
6卷引用:甘肃省金昌市2021-2022学年高三上学期第一次联考理科综合化学试题
甘肃省金昌市2021-2022学年高三上学期第一次联考理科综合化学试题(已下线)【直击双一流】03-备战2022年高考化学名校进阶模拟卷(通用版)(已下线)专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)湖南省邵阳市第一中学2023届高三第七次月考化学试题湖南省衡阳八中2022-2023学年高三第四次月考化学试题江西省南昌市第一中学2023-2024学年高二上学期11月期中考试化学试题
7 . 图中是利用垃圾假单胞菌株分解有机物的电化学原理图。下列说法正确的是


| A.电子流向:B电极→用电器→电极A,该过程将化学能转化为电能 |
| B.A电极上发生氧化反应,电极反应式为:X-4e- =Y+4H+ |
| C.若有机物为麦芽糖,处理0.25mol有机物,12molH+透过质子交换膜移动到右室 |
| D.若B电极上消耗标准状况下氧气56mL,则电极A上生成1.64gY |
您最近一年使用:0次
2022-01-27更新
|
924次组卷
|
6卷引用:甘肃省金昌市2021-2022学年高三上学期第一次联考理科综合化学试题
名校
解题方法
8 . 某化合物的结构为 ,其中X、Y、W、Z四种短周期元素原子半径依次增大,X和Z同主族,W和Z同周期,Y和Z的简单离子具有相同的电子层结构。下列叙述正确的是
,其中X、Y、W、Z四种短周期元素原子半径依次增大,X和Z同主族,W和Z同周期,Y和Z的简单离子具有相同的电子层结构。下列叙述正确的是
 ,其中X、Y、W、Z四种短周期元素原子半径依次增大,X和Z同主族,W和Z同周期,Y和Z的简单离子具有相同的电子层结构。下列叙述正确的是
,其中X、Y、W、Z四种短周期元素原子半径依次增大,X和Z同主族,W和Z同周期,Y和Z的简单离子具有相同的电子层结构。下列叙述正确的是| A.简单离子半径:W>Z>Y |
B.工业上可通过电解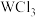 制取单质W 制取单质W |
| C.该化合物的水溶液显酸性 |
D. 与 与 形成的化合物可与 形成的化合物可与 与 与 形成的化合物发生反应 形成的化合物发生反应 |
您最近一年使用:0次
2022-01-27更新
|
1042次组卷
|
5卷引用:甘肃省金昌市2021-2022学年高三上学期第一次联考理科综合化学试题
甘肃省金昌市2021-2022学年高三上学期第一次联考理科综合化学试题(已下线)【直击双一流】05-备战2022年高考化学名校进阶模拟卷(通用版)(已下线)专项08 物质结构 元素周期律-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)湖南省常德市鼎城一中2022-2023学年高三第五次月考化学试题河南省新乡市第一中学2022-2023学年高一下学期3月月考化学试题
9 . 设 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是A.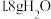 中含有的中子数为 中含有的中子数为 |
B.标准状况下,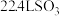 中含有的分子数大于 中含有的分子数大于 |
C.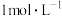  溶液中含有的阴阳离子总数约为3 溶液中含有的阴阳离子总数约为3 |
D.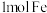 与足量 与足量 反应,转移的电子数为2 反应,转移的电子数为2 |
您最近一年使用:0次
解题方法
10 . 化学与生活、科技及环境密切相关。下列说法错误的是
| A.二氧化氯泡腾片遇水产生的二氧化氯能用于杀菌消毒 |
| B.高铁“和谐号”车厢连接关键部位所使用的增强聚四氟乙烯板属于有机高分子材料 |
| C.“木棉花落絮飞初,歌舞岗前夜雨余”中“絮”的主要成分和淀粉互为同分异构体 |
| D.蜡蛾幼虫会啃食聚乙烯塑料袋将其转化为乙二醇,这项研究有助于减少白色污染 |
您最近一年使用:0次



