1 . 晶体结构的缺陷美与对称美同样受关注。某富锂超离子导体的晶胞是立方体(图1),进行镁离子取代及卤素共掺杂后,可获得高性能固体电解质材料(图2)。下列说法错误的是
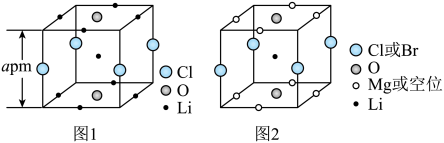
A.图1晶体密度为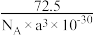 g∙cm-3 g∙cm-3 | B.图1中O原子的配位数为6 |
C.图2表示的化学式为 | D. 取代产生的空位有利于 取代产生的空位有利于 传导 传导 |
您最近一年使用:0次
2023-06-13更新
|
11117次组卷
|
22卷引用:2023年高考辽宁卷化学真题
2023年高考辽宁卷化学真题(已下线)测试辽宁化学 请勿下载(已下线)T14-晶体结构(已下线)2023年高考化学真题完全解读(辽宁卷)(已下线)专题06 物质结构与性质(已下线)专题06 物质结构与性质(已下线)专题06 物质结构与性质(已下线)第22讲晶体结构与性质(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)(已下线)考点43 晶体结构与性质(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第7讲 配合物与超分子(已下线)题型05 晶胞分析-2024年高考化学答题技巧与模板构建安徽省淮北市2023-2024学年高三上学期1月调研化学试题(已下线)微题型02 晶体结构及相关计算-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河北省石家庄市第十七中学2023-2024高二上学期期末考试化学试题福建泉州科技中学2022-2023学年高二下学期期末考化学试题 浙江省绍兴市诸暨市2023-2024学年高二上学期期末检测化学试题湖北省襄阳市第一中学2023-2024学年高二下学期3月月考化学试题湖北省鄂东新领先协作体2023-2024学年高二下学期3月联考化学试题安徽省合肥市第七中学2023-2024学年高二下学期第一次段考化学试卷 辽宁省沈阳市东北育才学校科学高中部2024届高三下学期最后一模化学试题
2 . 中华文化源远流长,化学与文化传承密不可分。下列说法错误的是
| A.青铜器“四羊方尊”的主要材质为合金 |
| B.长沙走马楼出土的竹木简牍主要成分是纤维素 |
| C.蔡伦采用碱液蒸煮制浆法造纸,该过程不涉及化学变化 |
| D.铜官窑彩瓷是以黏土为主要原料,经高温烧结而成 |
您最近一年使用:0次
2023-06-16更新
|
11014次组卷
|
15卷引用:2023年高考湖南卷化学真题
2023年高考湖南卷化学真题(已下线)专题01 化学与STSE(已下线)专题01 化学与STSE(已下线)专题01 化学与STSE(已下线)2023年湖南卷高考真题变式题(选择题1-5)(已下线)考点12 硅及其无机非金属材料(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题01 化学与STSE 物质的组成、性质和用途-2023年高考化学真题题源解密(新高考专用)(已下线)专题01 化学与STSE 物质的组成、性质和用途-2023年高考化学真题题源解密(全国通用)甘肃省武威市凉州区2024届高三上学期第一次诊断考试化学试题湖南省长沙市周南中学2023-2024学年高二上学期入学考试化学试题重庆市第七中学校2023-2024学年高三上学期11月月考化学试卷(已下线)题型01 物质的组成与分类 传统文化 化学用语-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)湖南省长沙麓山国际实验学校2023-2024学年高二下学期4月份学情检测化学试卷宁夏回族自治区银川一中2024届高三下学期考前热身训练化学试卷2(已下线)第01讲 物质的分类及转化(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
3 . 某工厂采用如下工艺制备 ,已知焙烧后
,已知焙烧后 元素以
元素以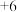 价形式存在,下列说法错误的是
价形式存在,下列说法错误的是
 ,已知焙烧后
,已知焙烧后 元素以
元素以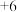 价形式存在,下列说法错误的是
价形式存在,下列说法错误的是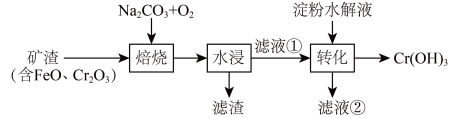
A.“焙烧”中产生 | B.滤渣的主要成分为 |
C.滤液①中 元素的主要存在形式为 元素的主要存在形式为 | D.淀粉水解液中的葡萄糖起还原作用 |
您最近一年使用:0次
2023-06-13更新
|
11185次组卷
|
23卷引用:2023年高考辽宁卷化学真题
2023年高考辽宁卷化学真题(已下线)测试辽宁化学 请勿下载(已下线)T10-物质反应及转化(已下线)2023年高考化学真题完全解读(辽宁卷)(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)专题10 物质的反应及转化(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)陕西省汉中中学2024届高三上学期8月质量检测化学试题陕西省渭南市2023-2024学年高三上学期期中检测化学试题(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)河北省迁安市2023-2024学年高三上学期期中考试化学试题(已下线)第3讲 物质制备实验的设计与评价黑龙江省龙西北名校联合体2023-2024学年高三上学期期中考试化学试题(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)陕西省西安市长安区第一中学2023-2024学年高三上学期第二次教学质量检测化学试题河北省保定市蠡县中学2023-2024学年高二上学期化学月考试题黑龙江省齐齐哈尔市龙西北高中名校联盟2023-2024学年高三上学期10月联考化学试题福建泉州科技中学2022-2023学年高二下学期期末考化学试题(已下线)第四章 生物大分子(B卷)(已下线)FHgkyldyjhx03福建省厦门第一中学2023-2024学年高三下学期5月第2次月考化学试卷2024年辽宁省锦州市渤海大学附属高级中学模拟化学试题
真题
名校
4 . 根据实验目的,下列实验及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 比较 和 和 的水解常数 的水解常数 | 分别测浓度均为 的 的 和 和 溶液的 溶液的 ,后者大于前者 ,后者大于前者 |  |
| B | 检验铁锈中是否含有二价铁 | 将铁锈溶于浓盐酸,滴入 溶液,紫色褪去 溶液,紫色褪去 | 铁锈中含有二价铁 |
| C | 探究氢离子浓度对 、 、 相互转化的影响 相互转化的影响 | 向 溶液中缓慢滴加硫酸,黄色变为橙红色 溶液中缓慢滴加硫酸,黄色变为橙红色 | 增大氢离子浓度,转化平衡向生成 的方向移动 的方向移动 |
| D | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,产生无色气体 | 乙醇中含有水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-06-08更新
|
23327次组卷
|
32卷引用:2022年高考全国甲卷化学真题
2022年高考全国甲卷化学真题(已下线)专题11化学实验基础-2022年高考真题+模拟题汇编(全国卷)(已下线)专题12化学实验方案的设计与评价-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题12化学实验方案的设计与评价-五年(2018~2022)高考真题汇编(全国卷)(已下线)2022年全国甲卷高考真题变式题(选择题)(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)微专题43 常见物质的分离、提纯和鉴别-备战2023年高考化学考点微专题(全国版)(已下线)易错点34 化学实验方案的设计与评价-备战2023年高考化学考试易错题河南省濮阳市南乐县第一高级中学2022-2023学年高三上学期9月月考化学试题福建省2022-2023学年高三上学期化学1月质检考前模拟试题(已下线)专题11 化学实验基础(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)专题24 实验分析设计型选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题18 物质检验、鉴别简单实验方案的设计及评价(已下线)题型169 “实验目的—实验现象—实验操作”中涉及的实验基本操作(已下线)专题05 突破化学实验基础(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)北京师范大学附属实验中学2022-2023学年高三下学期零模化学试题(已下线)素养卷09 微型原理验证方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题14 化学实验方案的设计与评价湖南省衡阳市第八中学2022-2023学年高二下学期5月月考化学试题(已下线)专题14 化学实验方案的设计与评价(已下线)专题14 化学实验方案的设计与评价(已下线)第09练 微型实验设计与评价 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题11 化学实验(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)江西省宜春市宜丰中学2022-2023学年高三上学期1月期末考试化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)题型07 化学实验基础(选择题)-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)四川省眉山市彭山区第一中学2023-2024学年高三上学期11月月考理综试题湖南省长沙市周南中学2023-2024学年高二下学期第一次月考化学试题山东省济宁市第一中学2023-2024学年高二下学期开学考试化学试题宁夏回族自治区银川一中2024届高三下学期考前热身训练化学试卷1
真题
解题方法
5 .  是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下:
(1)Co位于元素周期表第_______ 周期,第_______ 族。
(2)烧渣是LiCl、 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因_______ 。
(3)鉴别洗净的“滤饼3”和固体 常用方法的名称是
常用方法的名称是_______ 。
(4)已知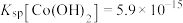 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为_______  。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为_______ 。
(5)导致 比
比 易水解的因素有
易水解的因素有_______ (填标号)。
a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
 是生产多晶硅的副产物。利用
是生产多晶硅的副产物。利用 对废弃的锂电池正极材料
对废弃的锂电池正极材料 进行氯化处理以回收Li、Co等金属,工艺路线如下:
进行氯化处理以回收Li、Co等金属,工艺路线如下: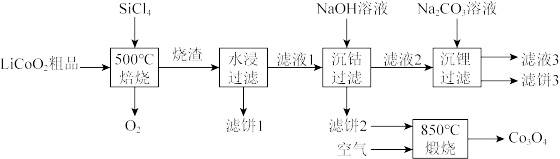
(1)Co位于元素周期表第
(2)烧渣是LiCl、
 和
和 的混合物,“500℃焙烧”后剩余的
的混合物,“500℃焙烧”后剩余的 应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因
应先除去,否则水浸时会产生大量烟雾,用化学方程式表示其原因(3)鉴别洗净的“滤饼3”和固体
 常用方法的名称是
常用方法的名称是(4)已知
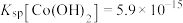 ,若“沉钴过滤”的pH控制为10.0,则溶液中
,若“沉钴过滤”的pH控制为10.0,则溶液中 浓度为
浓度为 。“850℃煅烧”时的化学方程式为
。“850℃煅烧”时的化学方程式为(5)导致
 比
比 易水解的因素有
易水解的因素有a.Si-Cl键极性更大 b.Si的原子半径更大
c.Si-Cl键键能更大 d.Si有更多的价层轨道
您最近一年使用:0次
2023-06-14更新
|
10956次组卷
|
13卷引用:2023年高考湖北卷化学真题
2023年高考湖北卷化学真题(已下线)专题18 工艺流程题(已下线)T16-工业流程题(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)第19练 化学工艺流程题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第32讲难溶电解质的溶解平衡(已下线)题型06 化工微流程-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)专题06 沉淀溶解平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)(已下线)题型四 无机化工流程题解题策略-备战2024年高考化学答题技巧与模板构建
真题
名校
6 . 日光灯中用到的某种荧光粉的主要成分为3W3(ZX4)2·WY2。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
| A.电负性:X>Y>Z>W |
| B.原子半径:X<Y<Z<W |
| C.Y和W的单质都能与水反应生成气体 |
| D.Z元素最高价氧化物对应的水化物具有强氧化性 |
您最近一年使用:0次
2023-06-16更新
|
11440次组卷
|
25卷引用:2023年高考湖南卷化学真题
2023年高考湖南卷化学真题(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)2023年湖南卷高考真题变式题(选择题6-10)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第19讲元素周期律与元素周期表安徽省亳州市第二完全中学2022-2023学年高二下学期期末考试化学(A卷)试题(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)湖北省武汉市第六中学2023-2024学年高三上学期第一次月考化学试题江西省宜春市宜丰中学2023-2024学年高三上学期开学考试化学试题天津市耀华中学2023-2024学年高三上学期第一次月考化学试题(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)福建省厦门第一中学2024届高三上学期10 月月考化学试题河北省迁安市2023-2024学年高三上学期期中考试化学试题福州市福州高级中学2023-2024学年高三上学期10月月考化学试题福建省厦门第一中学2024届高三上学期第一次月考化学试题重庆市第七中学校2023-2024学年高三上学期11月月考化学试卷北京市第二十中学2023-2024学年高三上学期10月月考化学试题(已下线)题型01 元素位-构-性推断-2024年高考化学答题技巧与模板构建(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)福建省福州高级中学2023-2024学年高三上学期第一阶段考试化学试卷山东省东营市第一中学2023-2024学年高二下学期开学收心考试化学试题(已下线)FHgkyldyjhx12
真题
解题方法
7 . 氨是最重要的化学品之一,我国目前氨的生产能力位居世界首位。回答下列问题:
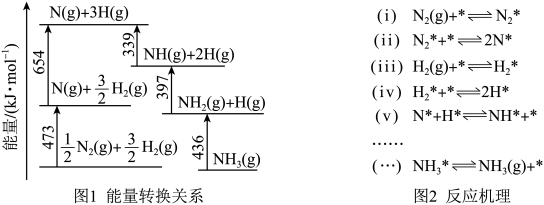
(1)根据图1数据计算反应 的
的
_______  。
。
(2)研究表明,合成氨反应在 催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,
催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,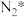 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
)。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为_______ (填步骤前的标号),理由是_______ 。
(3)合成氨催化剂前驱体(主要成分为 )使用前经
)使用前经 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数 ,密度为
,密度为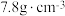 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为_______ (列出计算式,阿伏加德罗常数的值为 )。
)。
(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为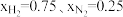 ,另一种为
,另一种为 。(物质i的摩尔分数:
。(物质i的摩尔分数: )
)

①图中压强由小到大的顺序为_______ ,判断的依据是_______ 。
②进料组成中含有惰性气体 的图是
的图是_______ 。
③图3中,当 、
、 时,氮气的转化率
时,氮气的转化率
_______ 。该温度时,反应 的平衡常数
的平衡常数
_______  (化为最简式)。
(化为最简式)。
(1)根据图1数据计算反应
 的
的
 。
。
(2)研究表明,合成氨反应在
 催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,
催化剂上可能通过图2机理进行(*表示催化剂表面吸附位,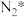 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
)。判断上述反应机理中,速率控制步骤(即速率最慢步骤)为(3)合成氨催化剂前驱体(主要成分为
 )使用前经
)使用前经 还原,生成
还原,生成 包裹的
包裹的 。已知
。已知 属于立方晶系,晶胞参数
属于立方晶系,晶胞参数 ,密度为
,密度为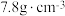 ,则
,则 晶胞中含有
晶胞中含有 的原子数为
的原子数为 )。
)。(4)在不同压强下,以两种不同组成进料,反应达平衡时氨的摩尔分数与温度的计算结果如下图所示。其中一种进料组成为
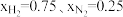 ,另一种为
,另一种为 。(物质i的摩尔分数:
。(物质i的摩尔分数: )
)
①图中压强由小到大的顺序为
②进料组成中含有惰性气体
 的图是
的图是③图3中,当
 、
、 时,氮气的转化率
时,氮气的转化率
 的平衡常数
的平衡常数
 (化为最简式)。
(化为最简式)。
您最近一年使用:0次
8 . 离子化合物 和
和 与水的反应分别为①
与水的反应分别为①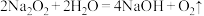 ;②
;② 。下列说法正确的是
。下列说法正确的是
 和
和 与水的反应分别为①
与水的反应分别为①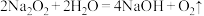 ;②
;② 。下列说法正确的是
。下列说法正确的是A.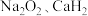 中均有非极性共价键 中均有非极性共价键 |
| B.①中水发生氧化反应,②中水发生还原反应 |
C. 中阴、阳离子个数比为 中阴、阳离子个数比为 , , 中阴、阳离子个数比为 中阴、阳离子个数比为 |
D.当反应①和②中转移的电子数相同时,产生的 和 和 的物质的量相同 的物质的量相同 |
您最近一年使用:0次
2023-06-28更新
|
10731次组卷
|
40卷引用:2023年高考北京卷化学真题
2023年高考北京卷化学真题(已下线)2023年北京卷高考真题变式题(选择题11-14)(已下线)第4讲 钠及其重要化合物(已下线)第8讲 物质的量与气体摩尔体积(已下线)专题04 氧化还原反应-2023年高考化学真题题源解密(全国通用)(已下线)专题03 化学计量-2023年高考化学真题题源解密(全国通用)(已下线)专题05 氧化还原反应及其计算-2023年高考化学真题题源解密(新高考专用)(已下线)专题03 阿伏加德罗常数与化学计算 -2023年高考化学真题题源解密(新高考专用)黑龙江省哈尔滨师范大学附属中学2022-2023学年高三下学期开学考试化学试题黑龙江省哈尔滨师范大学附属中学2024届高三上学期开学考试化学试题(已下线)广东省东莞市光正实验学校2023-2024学年高三上学期第二次月孝化学试题湖南省株洲市炎陵县2023-2024学年高二上学期入学考试化学试题江西省丰城中学2023-2024学年高二创新班上学期开学考试化学试题江苏省常州市联盟学校2023-2024学年高三上学期10月学情调研化学试题北京市第一七一中学2023-2024学年高三上学期10月考化学试题(已下线)实验03 探究氧化钠和过氧化钠的性质-【同步实验课】2023-2024学年高一化学教材实验大盘点(人教版2019必修第一册)山西省大同市第一中学校2023-2024学年高三上学期10月月考化学试题河北省石家庄市第二十四中学2023-2024高三上学期第一次月考化学试题四川省攀枝花市第七高级中学校2023-2024学年高三上学期9月第二次诊断性考试理综化学试题河北省石家庄市河北正定中学2024届高三上学期第二次月考化学试题天津市第二南开学校2023-2024学年高三上学期期中质量调查化学试题北京师范大学第二附属中学2023-2024学年高二上学期12月月考化学试题 北京师范大学第二附属中学2023-2024学年高三上学期期中考试化学试题(已下线)北京市第四中学2023-2024学年高三上学期期中考试化学试题(已下线)题型04 氧化还原反应-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)河南省信阳高级中学2023-2024学年高三上学期11月一模考试化学试题陕西省西安市长安区第一中学2023-2024学年高三上学期第二次教学质量检测化学试题山东省德州市第一中学2023-2024学年高三上学期1月月考化学试题天津市武清区城关中学2023-2024学年高三上学期第二次阶段性练习化学试题(已下线)北京市第四中学2023-2024学年高三上学期 期中化学试卷北京师范大学附属中学2023-2024学年高一上学期期末考试化学试卷北京市密云二中2023-2024学年高二上学期10月月考化学试卷 安徽省宿州市泗县第一中学2023-2024学年高一下学期开学考试化学试题黑龙江省哈尔滨师范大学附属中学2023-2024学年高一下学期开学摸底考试化学试卷福建省福建师范大学附属中学2023-2024学年高三上学期开学考化学试题四川省达州外国语学校2023-2024学年高二下学期3月月考化学试题北京市北京师范大学第二附属中学2023-2024学年高一下学期期中考试化学试题北京大学附属中学2023-2024学年高一下学期期中考试化学(行知+未名)试卷(已下线)第04讲 氧化还原反应的基本概念和规律(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
9 . 硫酸工业在国民经济中占有重要地位。
(1)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO4·5H2O)取精华法”。借助现代仪器分析,该制备过程中CuSO4·5H2O分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有SO2、_______ 和_______ (填化学式)。
NO2+SO2+H2O=NO+H2SO4
2NO+O2=2NO2
(ⅰ)上述过程中NO2的作用为_______ 。
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是_______ (答出两点即可)。
(3)接触法制硫酸的关键反应为SO2的催化氧化:
SO2(g)+ O2(g)
O2(g) SO3(g) ΔH=-98.9kJ·mol-1
SO3(g) ΔH=-98.9kJ·mol-1
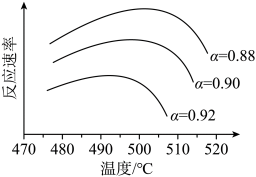
(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如下图所示,下列说法正确的是_______ 。
b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同 下的最大速率,选择最佳生产温度
下的最大速率,选择最佳生产温度
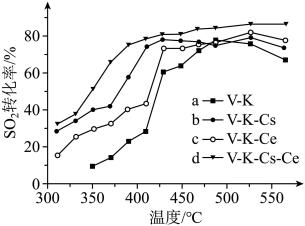
(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所示,催化性能最佳的是_______ (填标号)。_______ (用平衡分压代替平衡浓度计算)。
(1)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO4·5H2O)取精华法”。借助现代仪器分析,该制备过程中CuSO4·5H2O分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。700℃左右有两个吸热峰,则此时分解生成的氧化物有SO2、

NO2+SO2+H2O=NO+H2SO4
2NO+O2=2NO2
(ⅰ)上述过程中NO2的作用为
(ⅱ)为了适应化工生产的需求,铅室法最终被接触法所代替,其主要原因是
(3)接触法制硫酸的关键反应为SO2的催化氧化:
SO2(g)+
 O2(g)
O2(g) SO3(g) ΔH=-98.9kJ·mol-1
SO3(g) ΔH=-98.9kJ·mol-1(ⅰ)为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如下图所示,下列说法正确的是
b.α=0.88的曲线代表平衡转化率
c.α越大,反应速率最大值对应温度越低
d.可根据不同
 下的最大速率,选择最佳生产温度
下的最大速率,选择最佳生产温度(ⅱ)为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所示,催化性能最佳的是
您最近一年使用:0次
2023-06-13更新
|
10969次组卷
|
15卷引用:2023年高考辽宁卷化学真题
2023年高考辽宁卷化学真题(已下线)测试辽宁化学 请勿下载(已下线)T18-原理综合题(已下线)2023年高考化学真题完全解读(辽宁卷)(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)第20练 化学反应原理综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)第27讲化学平衡和化学平衡常数(已下线)题型12 化学平衡图表分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)2024届山东省潍坊市昌乐二中高三模拟预测化学试题山东省烟台市龙口市2023-2024学年高二上学期10月统考化学试题福建泉州科技中学2022-2023学年高二下学期期末考化学试题黑龙江省哈尔滨市双城区兆麟中学2023-2024学年高二下学期开学验收考试化学黑龙江省哈尔滨市双城区兆麟中学2023-2024学年高二下学期开学化学试题
10 . 探究卤族元素单质及其化合物的性质,下列方案设计、现象和结论都正确的是
实验方案 | 现象 | 结论 | |
A | 往碘的 溶液中加入等体积浓 溶液中加入等体积浓 溶液,振荡 溶液,振荡 | 分层,下层由紫红色变为浅粉红色,上层呈棕黄色 | 碘在浓 溶液中的溶解能力大于在 溶液中的溶解能力大于在 中的溶解能力 中的溶解能力 |
B | 用玻璃棒蘸取次氯酸钠溶液点在 试纸上 试纸上 | 试纸变白 | 次氯酸钠溶液呈中性 |
C | 向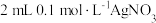 溶液中先滴加4滴 溶液中先滴加4滴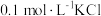 溶液,再滴加4滴 溶液,再滴加4滴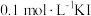 溶液 溶液 | 先产生白色沉淀,再产生黄色沉淀 |  转化为 转化为 , , 溶解度小于 溶解度小于 溶解度 溶解度 |
D | 取两份新制氯水,分别滴加 溶液和淀粉 溶液和淀粉 溶液 溶液 | 前者有白色沉淀,后者溶液变蓝色 | 氯气与水的反应存在限度 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-21更新
|
10419次组卷
|
21卷引用:2023年高考浙江卷化学真题(6月)
2023年高考浙江卷化学真题(6月)(已下线)2023年高考浙江卷化学真题(6月)变式题(选择题11-16)(已下线)专题14 化学实验方案的设计与评价(已下线)专题14 化学实验方案的设计与评价(已下线)考点09 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点巩固卷12 化学实验基础(一)(3大考点67题)-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)2019年高考江苏卷化学试题变式题(不定项选择题)(已下线)第17讲实验方案的设计与评价(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)(已下线)广东省东莞市光正实验学校2023-2024学年高三上学期第二次月孝化学试题(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 化学实验方案设计与探究 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)河南省濮阳市油田第二高级中学2023-2024学年高三10月份阶段性考试化学试题四川省内江市第六中学2023-2024学年高三上学期入学考试化学试题四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题(已下线)题型03 离子方程式正误判断 离子共存、检验和推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)选择题6-10题型15 沉淀溶解平衡及图像分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)2024届河北省实验中学高三年级上学期第一次月考化学试题四川省达州外国语学校2023-2024学年高二下学期3月月考化学试题浙江省余姚中学2023-2024学年高二下学期期中考试化学试题



