名校
1 . 反应CaC2+2H2O=Ca(OH)2+C2H2↑,可用于制取乙炔。下列说法正确的是
| A.H2O的空间结构为三角锥形 |
B.CaC2的电子式:Ca2+ |
C.C2H2的空间填充模型: |
D.基态碳原子的价层电子轨道表示式: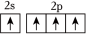 |
您最近一年使用:0次
2 . 赤铜矿(主要成分为 ,含少量
,含少量 、
、 )含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备
)含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备 晶体的流程为:
晶体的流程为:
(1) 晶体结构如下图所示。晶体中存在的作用力包括离子键、
晶体结构如下图所示。晶体中存在的作用力包括离子键、_______ 。_______ 。 发生反应的离子方程式为
发生反应的离子方程式为_______ 。检验氧化完全的试剂为_______ (填化学式)。
(4)沉铁。离子浓度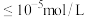 时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则
时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则 的
的 为
为_______ 。
(5)试从产率、试剂选择角度评价该制备流程并提出修改建议_______ 。
 ,含少量
,含少量 、
、 )含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备
)含铜量高达88.8%,是重要的冶金材料,某化学兴趣小组利用其制备 晶体的流程为:
晶体的流程为:

(1)
 晶体结构如下图所示。晶体中存在的作用力包括离子键、
晶体结构如下图所示。晶体中存在的作用力包括离子键、

 发生反应的离子方程式为
发生反应的离子方程式为(4)沉铁。离子浓度
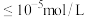 时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则
时,可认为该离子被沉淀完全。若室温下溶液pH应调节至略大于3.7,则 的
的 为
为(5)试从产率、试剂选择角度评价该制备流程并提出修改建议
您最近一年使用:0次
名校
3 . 设NA为阿伏加德罗常数的值。下列说法正确的是
| A.1molFe与水蒸气在高温下充分反应,转移的电子数为3NA |
| B.常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4NA |
| C.1mol[Cu(H2O)4]2+中σ键的数目为8NA |
| D.1L 1mol/L的NaClO溶液中含有ClO-的数目为NA |
您最近一年使用:0次
名校
4 . 下列反应的离子方程式书写正确的是
A.向 溶液中滴加少量氯水: 溶液中滴加少量氯水: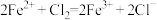 |
B.不用玻璃瓶盛装氢氟酸的原因: |
C.将稀硫酸加入硫代硫酸钠溶液中: |
D.Fe与稀硝酸反应,当 时, 时,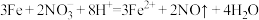 |
您最近一年使用:0次
解题方法
5 . 下列有关离子方程式错误 的是
A.向AgCl沉淀中加入过量氨水使AgCl溶解: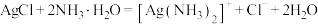 |
B.用 溶液处理锅炉水垢中的 溶液处理锅炉水垢中的 : : |
C.已知: 为二元弱碱,与足量浓 为二元弱碱,与足量浓 反应: 反应: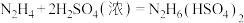 |
D.苯酚钠溶液中通入少量 气体: 气体: |
您最近一年使用:0次
名校
解题方法
6 . 下列离子方程式书写错误的是
A. 用于治疗胃酸(主要为盐酸)过多症: 用于治疗胃酸(主要为盐酸)过多症: |
B.将少量金属钠加入硫酸铜溶液中: |
C.铝粉和NaOH用作管道疏通剂: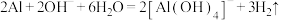 |
D.用湿润的淀粉-KI试纸检验 : : |
您最近一年使用:0次
名校
解题方法
7 . 下列离子在指定溶液中一定能大量共存的是
A.无色透明的溶液中: 、 、 、 、 、 、 |
B.含有大量 的溶液中: 的溶液中: 、 、 、 、 、 、 |
C.使酚酞变红的溶液中: 、 、 、 、 、 、 |
D. 的溶液中: 的溶液中: 、 、 、 、 、 、 |
您最近一年使用:0次
名校
8 . 下列化学用语的表达正确的是
A.H2S的电子式为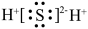 |
B.BaSO4的电离方程式为BaSO4⇌Ba2++ |
| C.中子数为10的氧的同位素为18O |
D.基态O原子核外电子轨道表示式: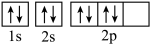 |
您最近一年使用:0次
昨日更新
|
110次组卷
|
2卷引用:广东省梅州市梅江区梅州中学2024届高三下学期5月模拟考试化学试题
名校
9 . 设 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.标准状况下,11.2 L  与11.2 L 与11.2 L  在光照下充分反应后,气体分子数为 在光照下充分反应后,气体分子数为 |
B.46 g乙醇中含有的 键的数目为 键的数目为 |
C.1 mol⋅L 的NaClO溶液中含有的 的NaClO溶液中含有的 数目小于 数目小于 |
D.1 mol 完全转化为 完全转化为 转移电子数为 转移电子数为 |
您最近一年使用:0次

 、
、 有还原性
有还原性 参与的反应一定为氧化还原反应
参与的反应一定为氧化还原反应

