2011·江西吉安·一模
1 . 下面是某学习小组对乙二酸的某些性质进行研究性学习的过程:
【研究课题】探究乙二酸的某些性质
【查阅资料】乙二酸(HOOC-COOH)俗称草酸,其主要物理常数如下:
又知草酸在100℃时开始升华,157℃时大量升华,并开始分解。草酸钙不溶于水。根据上述材料提供的信息,回答下列问题:
【提出猜想】
[猜想一]根据草酸晶体的组成对其分解产物进行猜想,设计方案:
(1)该小组同学猜想其产物为CO、CO2和H2O,并设计了探究实验,实验装置如下(草酸晶体分解装置略)。

A中水槽装冰水混合物、B中装氧化铜、C中装无水硫酸铜,D中装澄清石灰水、E中装碱石灰(已知草酸蒸气也可使澄清石灰水变浑浊,草酸蒸气在低温下可冷凝为固体)。请回答下列问题:
①装置的连接顺序为:A→__________ ;
②检验产物中CO的实验现象是__________ ;
③整套装置是否存在不合理之处,__________ (填是或否),若有该如何解决__________ ;
(猜想二)乙二酸具有弱酸性,设计方案:
(2)该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是__________ (填字母)
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH
C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
(猜想三)乙二酸具有还原性,设计方案:
(3)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性,写出该反应的离子方程式:__________ ;
(4)利用上述原理可定量测定某草酸晶体样品(含有H2C2O4•2H2O及其它一些杂质)中H2C2O4•2H2O的含量。方法是:称取该样品0.12g,加适量水完全溶解,然后用0.020mol•L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示(单位:mL),则该草酸晶体样品中H2C2O4•2H2O的质量分数为__________ ;(已知相对原子质量:Mr(H2C2O4•2H2O)=126)。

【研究课题】探究乙二酸的某些性质
【查阅资料】乙二酸(HOOC-COOH)俗称草酸,其主要物理常数如下:
| 名称 | 乙二酸 | 乙二酸晶体 |
| 分子式 | H2C2O4 | H2C2O4·2H2O |
| 颜色状态 | 无色固体 | 无色晶体 |
| 溶解度(g) | 8.6(20℃) | — |
| 熔点(℃) | 189.5 | 101.5 |
| 密度(g·cm-3) | 1.900 | 1.650 |
【提出猜想】
[猜想一]根据草酸晶体的组成对其分解产物进行猜想,设计方案:
(1)该小组同学猜想其产物为CO、CO2和H2O,并设计了探究实验,实验装置如下(草酸晶体分解装置略)。

A中水槽装冰水混合物、B中装氧化铜、C中装无水硫酸铜,D中装澄清石灰水、E中装碱石灰(已知草酸蒸气也可使澄清石灰水变浑浊,草酸蒸气在低温下可冷凝为固体)。请回答下列问题:
①装置的连接顺序为:A→
②检验产物中CO的实验现象是
③整套装置是否存在不合理之处,
(猜想二)乙二酸具有弱酸性,设计方案:
(2)该小组同学为验证草酸具有弱酸性设计了下列实验,其中能达到实验目的是
A.将草酸晶体溶于含酚酞的NaOH溶液中,溶液褪色
B.测定相同浓度的草酸和硫酸溶液的pH
C.测定草酸钠(Na2C2O4)溶液的pH
D.将草酸溶液加入Na2CO3溶液中,有CO2放出
(猜想三)乙二酸具有还原性,设计方案:
(3)该小组同学向用硫酸酸化的KMnO4溶液中滴入过量的草酸溶液,发现酸性KMnO4溶液褪色,从而判断草酸具有较强的还原性,写出该反应的离子方程式:
(4)利用上述原理可定量测定某草酸晶体样品(含有H2C2O4•2H2O及其它一些杂质)中H2C2O4•2H2O的含量。方法是:称取该样品0.12g,加适量水完全溶解,然后用0.020mol•L-1的酸性KMnO4溶液滴定至终点(杂质不参与反应),滴定前后滴定管中的液面读数如图所示(单位:mL),则该草酸晶体样品中H2C2O4•2H2O的质量分数为

您最近一年使用:0次
10-11高三上·江西宜春·阶段练习
解题方法
2 . “稳定性二氧化氯溶液”是淡黄色透明液体,广泛应用于食品卫生等领域的杀菌消毒。ClO2沸点11℃,是一种黄绿色的气体,易溶于水。ClO2稳定性较差,“稳定性二氧化氯溶液”是以碳酸钠为稳定剂,有效成分为NaClO2。
某合作学习小组的同学拟证实其中的有效成分并测定二氧化氯的含量(用样品和酸反应产生二氧化氯的质量与样品质量的比值来衡量)。请回答下列问题:
(1)为证实“稳定性二氧化氯溶液”中含有钠离子,其正确的操作步骤是:_______________ 。
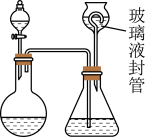
(2)为测定“稳定性二氧化氯溶液”中二氧化氯的含量,现进行以下操作:①取mg(2g左右)试样,置于烧瓶中,向分液漏斗中加入10mL盐酸溶液;②在锥形瓶中加入4g碘化钾,用100mL水溶解后,再加3mL硫酸溶液;③在玻璃液封管中加入水;④将分液漏斗中的盐酸溶液放入烧瓶中,关闭旋塞。缓慢加热烧瓶,使产生的二氧化氯气体全部通过导管在锥形瓶中被吸收;⑤将玻璃液封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定至蓝色消失(I2+2S2O32-=2I- +S4O62-),共用去VmL硫代硫酸钠溶液。
(Ⅰ)NaClO2与盐酸反应生成ClO2(还原产物为Cl-),该反应的化学方程式为:__________ ;ClO2通入锥形瓶与酸性碘化钾溶液反应,二氧化氯被还原为氯离子,该反应的离子方程式为:__________ 。
(Ⅱ)装置中玻璃液封管的作用是:_________ ;如何确定烧瓶中的二氧化氯全部被锥形瓶中的液体吸收________________ 。
(Ⅲ)“稳定性二氧化氯溶液”中,ClO2的质量分数为_____________ (用m、c、V表示)。

某合作学习小组的同学拟证实其中的有效成分并测定二氧化氯的含量(用样品和酸反应产生二氧化氯的质量与样品质量的比值来衡量)。请回答下列问题:
(1)为证实“稳定性二氧化氯溶液”中含有钠离子,其正确的操作步骤是:
(2)为测定“稳定性二氧化氯溶液”中二氧化氯的含量,现进行以下操作:①取mg(2g左右)试样,置于烧瓶中,向分液漏斗中加入10mL盐酸溶液;②在锥形瓶中加入4g碘化钾,用100mL水溶解后,再加3mL硫酸溶液;③在玻璃液封管中加入水;④将分液漏斗中的盐酸溶液放入烧瓶中,关闭旋塞。缓慢加热烧瓶,使产生的二氧化氯气体全部通过导管在锥形瓶中被吸收;⑤将玻璃液封管中的水封液倒入锥形瓶中,加入几滴淀粉溶液,用cmol/L硫代硫酸钠标准溶液滴定至蓝色消失(I2+2S2O32-=2I- +S4O62-),共用去VmL硫代硫酸钠溶液。
(Ⅰ)NaClO2与盐酸反应生成ClO2(还原产物为Cl-),该反应的化学方程式为:
(Ⅱ)装置中玻璃液封管的作用是:
(Ⅲ)“稳定性二氧化氯溶液”中,ClO2的质量分数为
您最近一年使用:0次
解题方法
3 . 某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质。
I.他们先把铜粉放在空气中灼烧,再与稀HNO3反应制取硝酸铜。
(1)如果直接用铜屑与稀HNO3反应来制取硝酸铜,可能导致的两个不利因素是______ 。
(2)实验中铜粉应该放在_____ (选填“蒸发皿”、“坩埚”或“烧杯”)中灼烧。欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤按顺序分别是___ 、____ 、过滤。
II.为了探究Cu(NO3)2的热稳定性,探究小组按下图中的装置进行实验。(图中铁架台、铁夹和加热设备均略去)
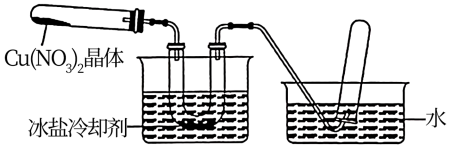
往左试管中放入研细的无水Cu(NO3)2晶体并加热,观察到左试管中有红棕色气体生成,最终残留黑色粉末;用U形管除去红棕色气体,在右试管中收集到无色气体。
(1)红棕色气体是____ 。
(2)当导管口不再有气泡冒出时,停止反应,这时在操作上应注意________ 。
(3)探究小组判断Cu(NO3)2的分解属于氧化还原反应,产物除了红棕色气体和黑色固体外,进一步分析、推断,分解产物中一定还含有_____ 。
III.为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请在下面表格中补充写出实验操作步骤、预期现象与结论___ 、___ 、___ 。
I.他们先把铜粉放在空气中灼烧,再与稀HNO3反应制取硝酸铜。
(1)如果直接用铜屑与稀HNO3反应来制取硝酸铜,可能导致的两个不利因素是
(2)实验中铜粉应该放在
II.为了探究Cu(NO3)2的热稳定性,探究小组按下图中的装置进行实验。(图中铁架台、铁夹和加热设备均略去)

往左试管中放入研细的无水Cu(NO3)2晶体并加热,观察到左试管中有红棕色气体生成,最终残留黑色粉末;用U形管除去红棕色气体,在右试管中收集到无色气体。
(1)红棕色气体是
(2)当导管口不再有气泡冒出时,停止反应,这时在操作上应注意
(3)探究小组判断Cu(NO3)2的分解属于氧化还原反应,产物除了红棕色气体和黑色固体外,进一步分析、推断,分解产物中一定还含有
III.为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请在下面表格中补充写出实验操作步骤、预期现象与结论
| 实验操作步骤 | 预期现象与结论 |
| 步骤1:观察样品 | 溶液呈蓝绿色, (填“能”或“不能”)确定 产物中铁元素的化合价 |
| 步骤2:取少量溶液,滴加酸性KMnO4溶液 | |
| 步骤3: | 若溶液变为红色,说明产物中含+3价的铁 元素;若溶液颜色无明显变化,则说明产物 中不含+3价的铁元素 |
您最近一年使用:0次



