1 . 甲乙两同学对保存已久的Na2SO3试剂进行实验探究。
取适量Na2SO3样品于洁净烧杯中,加入适量蒸馏水,充分搅拌全部溶解。
(1)测上述溶液的pH值,其pH值>7,原因是(用离子方程式表示)_________
(2)取少量上述溶液于试管中,加入硝酸钡溶液生成白色沉淀,再加入盐酸,白色沉淀不溶解,甲认为已变质,乙认为他的结论不科学,理由是______
(3)假设试剂由Na2SO3和Na2SO4组成,设计实验方案,进行成分检验,他们决定继续探究,请在答题卡上写出实验步骤、预期现象和结论。
限选 试剂及仪器:稀盐酸、稀硝酸、氯化钡溶液,品红溶液,酸性高锰酸溶液,NaOH溶液、澄清石灰水、pH计、烧杯、试管、带塞导气管、滴管
(4)经实验检验后,确实已变质,现准确测定其中Na2SO3的含量。实验如下:
①配制250ml约0.2mol•L-1Na2SO3溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水溶解,将溶液转入________ ,洗涤,定容,摇匀。
②滴定:准确量取25.00ml Na2SO3所配制溶液于锥形瓶中,将0.05mol•L-1酸性高锰酸钾装入50ml____ (填酸式或碱式)滴定管,滴定至终点,记录数据。重复滴定2次。平均消耗KMnO4VmL。
③计算Na2SO3的质量分数=______ (只列出计算式,不要求 算出结果)
取适量Na2SO3样品于洁净烧杯中,加入适量蒸馏水,充分搅拌全部溶解。
(1)测上述溶液的pH值,其pH值>7,原因是(用离子方程式表示)
(2)取少量上述溶液于试管中,加入硝酸钡溶液生成白色沉淀,再加入盐酸,白色沉淀不溶解,甲认为已变质,乙认为他的结论不科学,理由是
(3)假设试剂由Na2SO3和Na2SO4组成,设计实验方案,进行成分检验,他们决定继续探究,请在答题卡上写出实验步骤、预期现象和结论。
| 实验步骤 | 预期现象和结论 |
| 1.取适量试剂于洁净烧杯中,加入足量蒸馏水,充分搅拌,静置。 | |
| 2.取适量步骤1所得溶液于试管中,加入少量的 | 若溶液褪色,说明其有 若溶液不褪色,说明其中没有 |
| 3.再取适量步骤1所得溶液于另一试管中,先加入足量的稀盐酸,再滴 加 | 如果有白色沉淀生成,则说明其中有 |
①配制250ml约0.2mol•L-1Na2SO3溶液:准确称取w克试样,置于烧杯中,加适量蒸馏水溶解,将溶液转入
②滴定:准确量取25.00ml Na2SO3所配制溶液于锥形瓶中,将0.05mol•L-1酸性高锰酸钾装入50ml
③计算Na2SO3的质量分数=
您最近一年使用:0次
2016-12-09更新
|
166次组卷
|
3卷引用:2015-2016学年甘肃省会宁一中高二上期末考试化学试卷
2 . 下列根据实验操作和实验现象所得出的结论,正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱和Na2SO4溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| B | 在CuSO4溶液中加入KI溶液,再加入苯,振荡后静置 | 有白色沉淀生成,苯层呈紫红色 | 白色沉淀可能为CuI |
| C | 将气体X通入品红溶液中 | 红色褪去 | X一定是SO2 |
| D | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液 | 溶液变为血红色 | Fe(NO3)2样品已氧化变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-12-09更新
|
122次组卷
|
2卷引用:2016届甘肃西北师大附中高三下第五次诊断理科化学试卷
3 . 用莫尔盐[(NH4)2Fe(SO4)2·6H2O]为浅绿色晶体,隔绝空气时遇强热可完全分解为一种固体产物和多种气体产物(已知产物中无O2,其中确定的成分之一为N2)。在定量分析中莫尔盐常用作标定高锰酸钾、重铬酸钾等溶液的标准物质。回答下列问题:
(1)莫尔盐在空气中比硫酸亚铁稳定,但长期露置于空气中也会变质,可用来检验莫尔盐是否变质的试剂是_________ 。
(2)莫尔盐标定高锰酸钾溶液时,准确移取KMnO4溶液的仪器名称是_________ ,滴定过程中反应的离子方程式为________________________ 。
(3)某课题组组装如图所示的装置,通过实验检验莫尔盐晶体遇强热时的分解产物。实验中可观察到A中绿色粉末逐渐变成红色粉末,据此推测分解产物中有_________ (填化学式),同时装置C中酚酞溶液变红,酚酞溶液的作用是__________________ 。该装置可能存在的缺点是____________________________________ 。
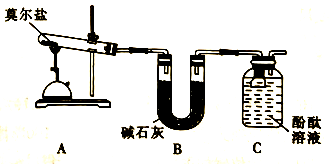 ,
,
(4)为分别检验产物中SO3(g)和SO2(g)的存在,应选用的试剂为_________ 和_________ 。加入试剂后经检验产物中不存在SO3(g),据此写出莫尔盐遇强热分解的化学方程式:_____________________________________________ 。
(1)莫尔盐在空气中比硫酸亚铁稳定,但长期露置于空气中也会变质,可用来检验莫尔盐是否变质的试剂是
(2)莫尔盐标定高锰酸钾溶液时,准确移取KMnO4溶液的仪器名称是
(3)某课题组组装如图所示的装置,通过实验检验莫尔盐晶体遇强热时的分解产物。实验中可观察到A中绿色粉末逐渐变成红色粉末,据此推测分解产物中有
 ,
,(4)为分别检验产物中SO3(g)和SO2(g)的存在,应选用的试剂为
您最近一年使用:0次
解题方法
4 . 在有机化学中,硫酰氯(SO2Cl2)常用作氯化剂和氯磺化剂,在染料、药品、除草剂和农用杀虫剂的生产过程中有重要作用。现在拟用干燥的Cl2和SO2在活性炭催化下制取硫酰氯。反应的化学方程式为:SO2(g)+ Cl2(g) =SO2Cl2(l) ΔH =−97.3 kJ·mol−1,实验装置如图所示(部分夹持装置未画出)。
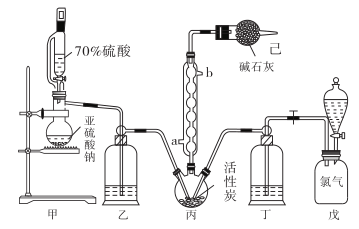
已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置丙中作为反应容器的仪器的名称为_______ ,装置丙中球形冷凝管的作用是________ ;如何控制两种反应物体积相等:____________________________________ 。
(2)装置戊上方分液漏斗中最好选用下列试剂:_________________ (选填字母)
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L-1盐酸
(3)若缺少装置己,硫酰氯(SO2Cl2)会和空气中的水反应而变质,其化学方程式是______________________________ 。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H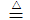 SO2Cl2 + H2SO4,分离两种产物的方法是
SO2Cl2 + H2SO4,分离两种产物的方法是_____________ (选填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期储存的硫酰氯会发黄,可能的原因是_________________________________ (用化学方程式和必要的文字加以解释)。
(6)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g纯净的硫酰氯,则硫酰氯的产率为___________ 。
(7)请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):___________________________ 。

已知:硫酰氯通常条件下为无色液体,熔点−54.1℃,沸点69.1℃。在潮湿空气中“发烟”;100°C以上开始分解,生成二氧化硫和氯气,长期放置也会发生分解。
回答下列问题:
(1)装置丙中作为反应容器的仪器的名称为
(2)装置戊上方分液漏斗中最好选用下列试剂:
A.蒸馏水 B.饱和食盐水 C.浓氢氧化钠溶液 D.6.0 mol·L-1盐酸
(3)若缺少装置己,硫酰氯(SO2Cl2)会和空气中的水反应而变质,其化学方程式是
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯:2ClSO3H
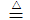 SO2Cl2 + H2SO4,分离两种产物的方法是
SO2Cl2 + H2SO4,分离两种产物的方法是A.重结晶 B.过滤 C.蒸馏 D.萃取
(5)长期储存的硫酰氯会发黄,可能的原因是
(6)若反应中消耗的氯气体积为896 mL(标准状况下),最后经过分离提纯得到4.05 g纯净的硫酰氯,则硫酰氯的产率为
(7)请设计实验方案检验产品中有硫酸(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):
您最近一年使用:0次
2018-06-06更新
|
427次组卷
|
3卷引用:甘肃省玉门市2021-2022学年高三上学期 “研课标读教材”期中学业质量监测化学试题
名校
解题方法
5 . 硫氰化钾(KSCN)可用于药物合成、作制冷剂等。 和
和 在催化剂作用下先合成
在催化剂作用下先合成 ,再制备
,再制备 ,利用如下装置制备
,利用如下装置制备 粗品。
粗品。
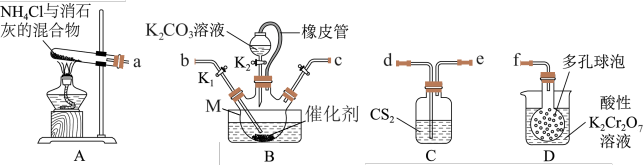
已知: 沸点为46.2℃,具有极强的挥发性。
沸点为46.2℃,具有极强的挥发性。
回答下列问题。
(1)连接装置,实验仪器接口顺序为a→___________ ,仪器M名称为___________ 。
(2)制备 时进行操作:
时进行操作:
(ⅰ)……;
(ⅱ)关闭 ,打开
,打开 ,点燃A处酒精灯,加热;
,点燃A处酒精灯,加热;
(ⅲ)当C装置中 消失,熄灭酒精灯,反应一段时间。
消失,熄灭酒精灯,反应一段时间。
操作(ⅰ)为___________ 。M中产物为两种铵盐,发生反应的化学方程式为___________ 。
(3)移走B处水浴槽,加热M并保持恒温105℃一段时间,关闭 ,打开
,打开 ,保持恒温105℃,向M中缓慢加入
,保持恒温105℃,向M中缓慢加入 溶液,反应过程中会产生大量气体,气体的主要成分为
溶液,反应过程中会产生大量气体,气体的主要成分为___________ 。装置D的作用是___________ 。
(4)测定产物中 的含量:称取制备的
的含量:称取制备的 样品配成
样品配成 溶液,取
溶液,取 溶液于锥形瓶中,加入适量稀硝酸,加入3滴
溶液于锥形瓶中,加入适量稀硝酸,加入3滴 溶液作指示剂,用
溶液作指示剂,用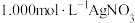 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液
标准溶液 。滴定终点的现象为
。滴定终点的现象为___________ ,晶体中 的质量分数为
的质量分数为___________ 。[已知: (白色)]。
(白色)]。
 和
和 在催化剂作用下先合成
在催化剂作用下先合成 ,再制备
,再制备 ,利用如下装置制备
,利用如下装置制备 粗品。
粗品。
已知:
 沸点为46.2℃,具有极强的挥发性。
沸点为46.2℃,具有极强的挥发性。回答下列问题。
(1)连接装置,实验仪器接口顺序为a→
(2)制备
 时进行操作:
时进行操作:(ⅰ)……;
(ⅱ)关闭
 ,打开
,打开 ,点燃A处酒精灯,加热;
,点燃A处酒精灯,加热;(ⅲ)当C装置中
 消失,熄灭酒精灯,反应一段时间。
消失,熄灭酒精灯,反应一段时间。操作(ⅰ)为
(3)移走B处水浴槽,加热M并保持恒温105℃一段时间,关闭
 ,打开
,打开 ,保持恒温105℃,向M中缓慢加入
,保持恒温105℃,向M中缓慢加入 溶液,反应过程中会产生大量气体,气体的主要成分为
溶液,反应过程中会产生大量气体,气体的主要成分为(4)测定产物中
 的含量:称取制备的
的含量:称取制备的 样品配成
样品配成 溶液,取
溶液,取 溶液于锥形瓶中,加入适量稀硝酸,加入3滴
溶液于锥形瓶中,加入适量稀硝酸,加入3滴 溶液作指示剂,用
溶液作指示剂,用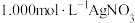 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液
标准溶液 。滴定终点的现象为
。滴定终点的现象为 的质量分数为
的质量分数为 (白色)]。
(白色)]。
您最近一年使用:0次
2024-03-18更新
|
151次组卷
|
3卷引用:甘肃省平凉市静宁县第一中学2023-2024学年高三下学期开学化学试题
名校
解题方法
6 . 无水FeCl3是芳香烃取代反应常用的催化剂,它具有易水解、易升华的性质。某同学用5.60g干燥铁粉制得13.00g无水FeCl3样品,实验装置如图所示。下列说法正确的是
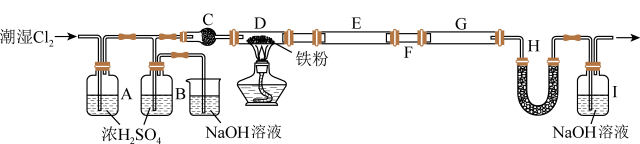

| A.该实验中FeCl3的产率为60% |
| B.装置C、H中的药品可以都为P2O5 |
| C.装置B用于干燥氯气,装置E和G用于收集产物 |
| D.可用K4[Fe(CN)6]溶液检验FeCl3产品中是否存在FeCl2 |
您最近一年使用:0次
2023-04-04更新
|
1834次组卷
|
10卷引用:甘肃省天水市第一中学 第三中学联考2023-2024学年高三上学期第三次月考 化学试题
甘肃省天水市第一中学 第三中学联考2023-2024学年高三上学期第三次月考 化学试题湖北省圆创2023届高三3月联合测评化学试题湖北省武汉市圆创联考2023届高三3月质检化学试题(已下线)化学-2023年高考押题预测卷03(云南,安徽,黑龙江,山西,吉林五省通用)(含考试版、全解全析、参考答案、答题卡)(已下线)题型35 微型成套装置实验流程(已下线)T13-化学实验基础湖北省名校联盟2023届高三3月联合测评化学试题(已下线)选择题11-15四川省成都市双流棠湖中学2023-2024学年高三上学期11月期中考试化学试题(已下线)热点19 化学微型实验
解题方法
7 . 磁性Fe3O4纳米粒子(粒径1-100nm)因其独特的物理、化学性质广泛用于生物医学和功能材料等领域而受到研究者的关注。实验室通过共沉淀法制备磁性Fe3O4纳米粒子的方法如下:
I.称取5.0gFeCl2·4H2O和2.7gFeCl3·6HO加入烧杯中,加入40mL蒸馏水,充分溶解。
Ⅱ.将I所得的混合液保持30℃恒温,向混合液中加入0.4mol·L-1的NaOH溶液并不断搅拌,溶液中逐渐出现黑色物质,直至溶液pH=11,再加入5mL乙醇,将混合液在50℃恒温的条件下晶化2h。
Ⅲ.从晶化后的混合液中分离出纳米粒子,用少量蒸馏水反复洗涤直至洗涤液的pH=7,再用乙醇洗涤后,在60℃真空中干燥2h得到磁性Fe3O4纳米粒子。
回答下列问题:
(1)将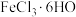 固体溶于蒸馏水时常会出现的现象为
固体溶于蒸馏水时常会出现的现象为___________ 。
(2)制备时NaOH溶液的浓度不宜过大,其原因为___________ ,实验Ⅱ过程中控制反应温度为50℃的操作方法为___________ 。
(3)生成磁性Fe3O4纳米粒子的离子方程式为___________ 。在制备过程中实际上加入的试剂中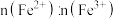 约为2.5:1,其原因为
约为2.5:1,其原因为___________ 。
(4)实验Ⅲ中除了通过测定洗涤液的pH=7外,实验室还可以判断纳米粒子已经洗涤干净的操作方法为___________ 。
(5)产物中混杂的 会降低纳米粒子的磁性,为了测定产品中
会降低纳米粒子的磁性,为了测定产品中 的含量,采取如下实验方法:准确称取
的含量,采取如下实验方法:准确称取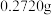 产品于锥形瓶中,用稀硝酸充分浸取,再加热使过量的硝酸全部逸出,冷却后加入足量
产品于锥形瓶中,用稀硝酸充分浸取,再加热使过量的硝酸全部逸出,冷却后加入足量 溶液充分混合反应后,用
溶液充分混合反应后,用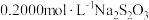 标准溶液滴定至溶液颜色明显变浅,加入几滴淀粉溶液,继续滴定至终点,消耗
标准溶液滴定至溶液颜色明显变浅,加入几滴淀粉溶液,继续滴定至终点,消耗 标准溶液的体积为
标准溶液的体积为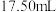 ,已知滴定过程中发生反应的离子方程式为
,已知滴定过程中发生反应的离子方程式为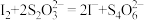 。
。
① 标准溶液应盛放在
标准溶液应盛放在____________ 填“酸式”或“碱式”)滴定管。
②若过量的硝酸没有全部逸出,则会导致测定结果___________ (填“偏高”“偏低”或“不变”)。
③所取样品中 的质量为
的质量为___________ g(结果保留4位小数)。
I.称取5.0gFeCl2·4H2O和2.7gFeCl3·6HO加入烧杯中,加入40mL蒸馏水,充分溶解。
Ⅱ.将I所得的混合液保持30℃恒温,向混合液中加入0.4mol·L-1的NaOH溶液并不断搅拌,溶液中逐渐出现黑色物质,直至溶液pH=11,再加入5mL乙醇,将混合液在50℃恒温的条件下晶化2h。
Ⅲ.从晶化后的混合液中分离出纳米粒子,用少量蒸馏水反复洗涤直至洗涤液的pH=7,再用乙醇洗涤后,在60℃真空中干燥2h得到磁性Fe3O4纳米粒子。
回答下列问题:
(1)将
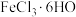 固体溶于蒸馏水时常会出现的现象为
固体溶于蒸馏水时常会出现的现象为(2)制备时NaOH溶液的浓度不宜过大,其原因为
(3)生成磁性Fe3O4纳米粒子的离子方程式为
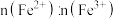 约为2.5:1,其原因为
约为2.5:1,其原因为(4)实验Ⅲ中除了通过测定洗涤液的pH=7外,实验室还可以判断纳米粒子已经洗涤干净的操作方法为
(5)产物中混杂的
 会降低纳米粒子的磁性,为了测定产品中
会降低纳米粒子的磁性,为了测定产品中 的含量,采取如下实验方法:准确称取
的含量,采取如下实验方法:准确称取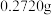 产品于锥形瓶中,用稀硝酸充分浸取,再加热使过量的硝酸全部逸出,冷却后加入足量
产品于锥形瓶中,用稀硝酸充分浸取,再加热使过量的硝酸全部逸出,冷却后加入足量 溶液充分混合反应后,用
溶液充分混合反应后,用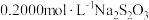 标准溶液滴定至溶液颜色明显变浅,加入几滴淀粉溶液,继续滴定至终点,消耗
标准溶液滴定至溶液颜色明显变浅,加入几滴淀粉溶液,继续滴定至终点,消耗 标准溶液的体积为
标准溶液的体积为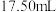 ,已知滴定过程中发生反应的离子方程式为
,已知滴定过程中发生反应的离子方程式为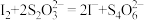 。
。①
 标准溶液应盛放在
标准溶液应盛放在②若过量的硝酸没有全部逸出,则会导致测定结果
③所取样品中
 的质量为
的质量为
您最近一年使用:0次
名校
解题方法
8 . 已知: 是重要的硫-氮二元化合物,室温下为橙黄色的固体,178~187℃熔化并分解,可用氨气与
是重要的硫-氮二元化合物,室温下为橙黄色的固体,178~187℃熔化并分解,可用氨气与 反应制得。某同学利用如图装置(加热装置已略)制取
反应制得。某同学利用如图装置(加热装置已略)制取 ,然后制取
,然后制取 。已知:
。已知: 为红棕色液体,有刺激性臭味,熔点:
为红棕色液体,有刺激性臭味,熔点: ,沸点:60℃,易水解。
,沸点:60℃,易水解。

反应步骤:
①反应时先向C中通入干燥的氯气,使硫粉与氯气在50℃下反应生成 。
。
②待C中的硫粉全部反应后,关闭B、C之间的止水夹,撤掉装置A、B。
③连接制氨的装置,通入氨,反应制得 。
。
回答下列问题。
(1)仪器C的名称为_______ ,a中三氧化铬(还原产物中铬为+3价)可与浓盐酸快速反应制得氯气,写出反应的离子方程式_______ 。
(2)B装置中应选择的试剂为_______ 。制取 过程中,b导管末端应连接下图中的
过程中,b导管末端应连接下图中的_______ (填序号)。
A.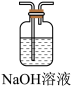 B.
B. C.
C.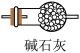 D.
D.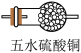
(3)向制得的 中通入
中通入 ,生成
,生成 的同时还生成一种常见固体单质和一种盐,写出反应的化学方程式
的同时还生成一种常见固体单质和一种盐,写出反应的化学方程式_______ 。所得产物分离后,检验所得盐中阳离子的具体操作步骤和现象_______ 。
(4) 在碱性条件下发生水解反应氮元素转化为氨,用硼酸吸收,滴定氨释放量可进一步测定
在碱性条件下发生水解反应氮元素转化为氨,用硼酸吸收,滴定氨释放量可进一步测定 的纯度。称取1.000g
的纯度。称取1.000g 样品,加入NaOH溶液,并加热,释放出的氨用足量100mL
样品,加入NaOH溶液,并加热,释放出的氨用足量100mL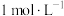 硼酸吸收[反应方程式为
硼酸吸收[反应方程式为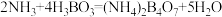 ,假定反应过程中溶液体积不变]。反应后的溶液以甲基红-亚甲蓝为指示剂,再用
,假定反应过程中溶液体积不变]。反应后的溶液以甲基红-亚甲蓝为指示剂,再用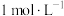 的盐酸[滴定反应方程式为
的盐酸[滴定反应方程式为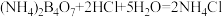
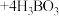 ]进行滴定,重复三次实验。实验数据记录如下表所示:
]进行滴定,重复三次实验。实验数据记录如下表所示:
则制得的 的纯度为
的纯度为_______ (保留4位有效数字)。
 是重要的硫-氮二元化合物,室温下为橙黄色的固体,178~187℃熔化并分解,可用氨气与
是重要的硫-氮二元化合物,室温下为橙黄色的固体,178~187℃熔化并分解,可用氨气与 反应制得。某同学利用如图装置(加热装置已略)制取
反应制得。某同学利用如图装置(加热装置已略)制取 ,然后制取
,然后制取 。已知:
。已知: 为红棕色液体,有刺激性臭味,熔点:
为红棕色液体,有刺激性臭味,熔点: ,沸点:60℃,易水解。
,沸点:60℃,易水解。
反应步骤:
①反应时先向C中通入干燥的氯气,使硫粉与氯气在50℃下反应生成
 。
。②待C中的硫粉全部反应后,关闭B、C之间的止水夹,撤掉装置A、B。
③连接制氨的装置,通入氨,反应制得
 。
。回答下列问题。
(1)仪器C的名称为
(2)B装置中应选择的试剂为
 过程中,b导管末端应连接下图中的
过程中,b导管末端应连接下图中的A.
 B.
B. C.
C. D.
D.
(3)向制得的
 中通入
中通入 ,生成
,生成 的同时还生成一种常见固体单质和一种盐,写出反应的化学方程式
的同时还生成一种常见固体单质和一种盐,写出反应的化学方程式(4)
 在碱性条件下发生水解反应氮元素转化为氨,用硼酸吸收,滴定氨释放量可进一步测定
在碱性条件下发生水解反应氮元素转化为氨,用硼酸吸收,滴定氨释放量可进一步测定 的纯度。称取1.000g
的纯度。称取1.000g 样品,加入NaOH溶液,并加热,释放出的氨用足量100mL
样品,加入NaOH溶液,并加热,释放出的氨用足量100mL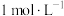 硼酸吸收[反应方程式为
硼酸吸收[反应方程式为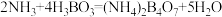 ,假定反应过程中溶液体积不变]。反应后的溶液以甲基红-亚甲蓝为指示剂,再用
,假定反应过程中溶液体积不变]。反应后的溶液以甲基红-亚甲蓝为指示剂,再用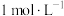 的盐酸[滴定反应方程式为
的盐酸[滴定反应方程式为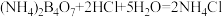
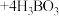 ]进行滴定,重复三次实验。实验数据记录如下表所示:
]进行滴定,重复三次实验。实验数据记录如下表所示:| 实验序号 | 初始读数 | 最终读数 |
| I | 0.10 | 20.14 |
| II | 0.50 | 24.75 |
| III | 1.00 | 20.96 |
 的纯度为
的纯度为
您最近一年使用:0次
名校
9 . 某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。
I.制备纯碱:先以NaCl、NH3、CO2和水等为原料,用下图所示装置制取NaHCO3,然后再将NaHCO3制备成Na2CO3。
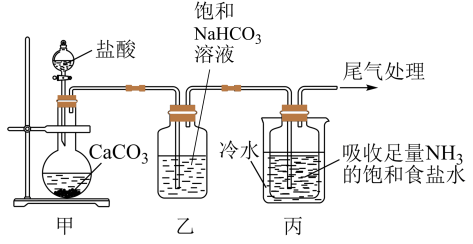
(1)装置乙的作用是_______ ,反应的化学方程式为_______ 。
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3。装置丙中可得两种产物,分别是NaHCO3和另一种盐,装置丙中反应的化学方程式为____ 。
(3)用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有过滤、洗涤、_______ ,最后一步发生反应的化学方程式为_______ 。
II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有NaHCO3,请选择下列装置设计实验,并完成下表:
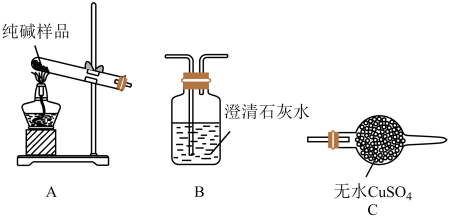
(5)测定该纯碱样品的纯度:称取m1g样品,置于小烧杯中,加水溶解,滴加足量CaCl2溶液。将反应混合物过滤、洗涤、干燥、称量,得到固体的质量为m2g。则该纯碱样品的纯度为_______ 。请另设计一个实验方案,测定纯碱样品的纯度(样品中只含有NaHCO3杂质)_______ 。
I.制备纯碱:先以NaCl、NH3、CO2和水等为原料,用下图所示装置制取NaHCO3,然后再将NaHCO3制备成Na2CO3。

(1)装置乙的作用是
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3。装置丙中可得两种产物,分别是NaHCO3和另一种盐,装置丙中反应的化学方程式为
(3)用装置丙中产生的NaHCO3制取Na2CO3时,需要进行的实验操作有过滤、洗涤、
II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有NaHCO3,请选择下列装置设计实验,并完成下表:

| 选择的装置(填编号) | 实验现象 | 实验结论 |
| 样品中含NaHCO3 |
您最近一年使用:0次
2022-08-21更新
|
474次组卷
|
2卷引用:甘肃省天水市2023-2024学年高一上学期10月份化学竞赛试卷
解题方法
10 . 草酸亚铁晶体( FeC2O4·2H2O,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
(1)采用如下装置(可重复选用)进行实验探究纯净草酸亚铁晶体受热分解的产物。
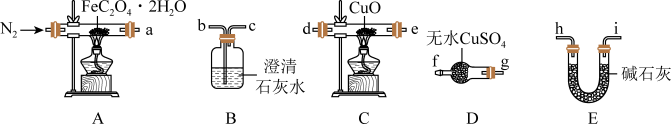
①装置D的名称为_______ 。
②按照气流从左到右的方向,上述装置的连接顺序为_______ → 尾气处理装置。(填仪器接口的字母编号)
③实验前先通入一段时间N2,其目的为_______ 。
④实验证明气体产物中含有CO,依据的实验现象为_______ 。
⑤充分反应后,A处硬质试管中残留黑色固体。查阅资料可知,黑色固体可能为Fe或FeO。小组成员设计实验证明了其成分只有FeO,其操作及现象为_______ 。
⑥A处硬质试管中发生反应的化学方程式为_______ 。
(2)测定草酸亚铁晶体样品的纯度。
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品并溶于稀H2SO4中,配成250 mL溶液 ;
步骤2:取上述溶液25.00 mL,用c mol/L KMnO4标准液滴定至终点,消耗标准液V1 mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4再用cmol/LKMnO4标准溶液滴定至终点,消耗标准液V2mL。
①步骤3中加入锌粉的目的是_______ 。
②草酸亚铁晶体样品的纯度为_______ (列出计算式即可,不必化简)。
(1)采用如下装置(可重复选用)进行实验探究纯净草酸亚铁晶体受热分解的产物。

①装置D的名称为
②按照气流从左到右的方向,上述装置的连接顺序为
③实验前先通入一段时间N2,其目的为
④实验证明气体产物中含有CO,依据的实验现象为
⑤充分反应后,A处硬质试管中残留黑色固体。查阅资料可知,黑色固体可能为Fe或FeO。小组成员设计实验证明了其成分只有FeO,其操作及现象为
⑥A处硬质试管中发生反应的化学方程式为
(2)测定草酸亚铁晶体样品的纯度。
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品并溶于稀H2SO4中,配成250 mL溶液 ;
步骤2:取上述溶液25.00 mL,用c mol/L KMnO4标准液滴定至终点,消耗标准液V1 mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4再用cmol/LKMnO4标准溶液滴定至终点,消耗标准液V2mL。
①步骤3中加入锌粉的目的是
②草酸亚铁晶体样品的纯度为
您最近一年使用:0次
2022-07-12更新
|
111次组卷
|
2卷引用:甘肃省庆阳市宁县2021-2022学年高二下学期期末考试化学试题



