名校
1 . 将一定量的Cl2通入体积为40mL、浓度为7.5mol/L的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),测得反应后溶液中有三种含氯元素的离子,其中ClO-物质的量为0.06mol和ClO3-物质的量0.03mol,下列说法不正确的是
| A.该反应的离子方程式为:5Cl2+10OH-=7Cl-+2ClO-+ClO3—+5H2O |
| B.该反应中,氧化剂与还原剂物质的量之比为5:3 |
| C.上述苛性钾溶液中含有0.3mol的KOH |
| D.反应后生成的ClO-和ClO3-两种离子在一定条件下均有氧化性 |
您最近一年使用:0次
2016-12-09更新
|
2583次组卷
|
5卷引用:2015-2016学年江苏省南通中学高一上学期期末化学试卷
名校
解题方法
2 . 向FeI2、FeBr2的混合溶液中通入适量的氯气,溶液中某些离子的物质的量变化如下图所示。下列有关说法中正确的是
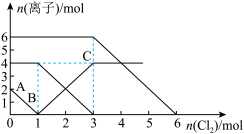

| A.离子的还原性顺序为:Fe2+>Br->I- |
| B.原混合溶液中FeBr2的物质的量为4mol |
| C.原溶液中:n(Fe2+)∶n(I-)∶n(Br-)=2∶1∶3 |
| D.当通入2 mol Cl2时,溶液中发生的离子反应可表示为:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
您最近一年使用:0次
2016-12-09更新
|
1854次组卷
|
7卷引用:江苏省盐城中学2023-2024学年高一上学期12月月考化学试题
名校
解题方法
3 . 将一定质量的铁、氧化铁、氧化铜的混合物粉末放入100 mL4.40 mol/L盐酸中,充分反应后产生896 mL H2(标准状况),残留固体1.28 g。过滤,滤液中无Cu2+。将滤液加水稀释到200 mL,测得其中c(H+)为0.400 mol/L。则原混合物中单质铁的质量是
| A.2.4g | B.3.36g | C.5.60g | D.10.08g |
您最近一年使用:0次
2016-12-09更新
|
2791次组卷
|
7卷引用:江苏省启东中学2016-2017学年高一(创新班)下学期期中考试化学试题
江苏省启东中学2016-2017学年高一(创新班)下学期期中考试化学试题江苏省连云港市锦屏高级中学2016-2017学年高二上学期期中考试化学试题2014-2015四川省遂宁市射洪中学高一下学期第一次月考化学试卷2016届吉林省长春市第十一高中高三上学期期中测试化学试卷2016届湖南长沙市长郡中学三上学期第四次月考化学试卷辽宁省实验中学2021-2022学年高一上学期12月月考化学试题(已下线)3.1.2 铁盐和亚铁盐-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)
名校
解题方法
4 . 高纯碳酸锰在电子工业中有重要的应用,湿法浸出软锰矿(主要成分为MnO2,含少量Fe、Al、Mg等杂质元素)制备高纯碳酸锰的实验过程如下:
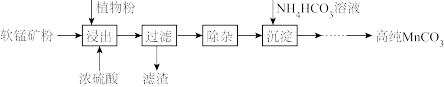
(1)浸出:浸出时温度控制在90℃~95℃之间,并且要连续搅拌3小时的目的是____ ,植物粉的作用是____ 。
(2)除杂:①向浸出液中加入一定量的碳酸锰矿,调节浸出液的pH为3.5~5.5;
②再加入一定量的软锰矿和双氧水,过滤;
③…
操作①中使用碳酸锰调pH的优势是____ ;操作②中加入双氧水不仅能将Fe2+氧化为Fe3+,而且能提高软锰矿的浸出率。写出双氧水提高软锰矿浸出率的离子方程式____ 。
(3)制备:在30 ℃~35 ℃下, 将碳酸氢铵溶液滴加到硫酸锰净化液中,控制反应液的最终pH在6.5~7.0,得到MnCO3沉淀。温度控制35 ℃以下的原因是____ ;该反应的化学方程式为____ ;生成的MnCO3沉淀需经充分洗涤,检验洗涤是否完全的方法是____ 。
(4)计算:室温下,Ksp(MnCO3)=1.8×10-11,Ksp(MgCO3)=2.6×10-5,已知离子浓度小于1.0×10-5mol·L-1时,表示该离子沉淀完全。若净化液中的c(Mg2+)=10-2mol/L,试计算说明Mg2+的存在是否会影响MnCO3的纯度。_____________________________________

(1)浸出:浸出时温度控制在90℃~95℃之间,并且要连续搅拌3小时的目的是
(2)除杂:①向浸出液中加入一定量的碳酸锰矿,调节浸出液的pH为3.5~5.5;
②再加入一定量的软锰矿和双氧水,过滤;
③…
操作①中使用碳酸锰调pH的优势是
(3)制备:在30 ℃~35 ℃下, 将碳酸氢铵溶液滴加到硫酸锰净化液中,控制反应液的最终pH在6.5~7.0,得到MnCO3沉淀。温度控制35 ℃以下的原因是
(4)计算:室温下,Ksp(MnCO3)=1.8×10-11,Ksp(MgCO3)=2.6×10-5,已知离子浓度小于1.0×10-5mol·L-1时,表示该离子沉淀完全。若净化液中的c(Mg2+)=10-2mol/L,试计算说明Mg2+的存在是否会影响MnCO3的纯度。
您最近一年使用:0次
2016-12-09更新
|
721次组卷
|
2卷引用:2015届江苏省扬州市高三上学期期末考试化学试卷
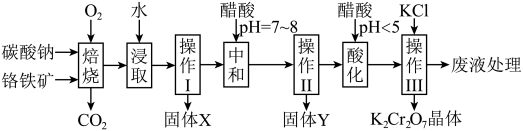
5 . 铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,以下是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的流程图: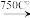 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;
②Na2CO3+Al2O3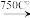 2NaAlO2 +CO2↑;
2NaAlO2 +CO2↑;
③Cr2O72-+H2O 2CrO42-+2H+
2CrO42-+2H+
根据题意回答下列问题:
(1)操作I的名称是_____ 。
(2)下表是相关物质的溶解度数据,操作III发生反应的化学方程式是:Na2Cr207 + 2KCl=K2Cr2O7 ↓+ 2NaCl,该反应在溶液中能发生的理由是_____
(3)操作III有多步组成,获得K2Cr2O7晶体的操作依次是:加入KC1固体、蒸发浓缩、_____ 、过滤、_____ 、干燥。
(4)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量_____ (填写试剂)、溶解、过滤、再通入足量_____ 气体.......灼烧、冷却、称量,得干燥固体m g。计算样品中氢氧化铝的质量分数为_____ (用含m、n的代数式表示)。
(5)称取重铬酸钾试样2.500g配成250mL溶液,取出25mL与碘量瓶中,加入10mL 2mol/L H2SO4和足量碘化钾,放于暗处5min。然后加入100mL水,加入3mL 淀粉指示剂,用0.1000mol/LNa2SO3标准溶液滴定若实验中共用去Na2S2O3标准溶液47.40mL,则所得产品中重铬酸钾的纯度为_____ 。(保留3位有效数字)
已知:①K2Cr2O7的摩尔质量为294g/mol
②Cr2O +6I-+14H+=2Cr3++3I2+7H2O;I2+2S2O
+6I-+14H+=2Cr3++3I2+7H2O;I2+2S2O =2I-+S4O
=2I-+S4O
 8Na2CrO4+2Fe2O3+8CO2↑;
8Na2CrO4+2Fe2O3+8CO2↑;②Na2CO3+Al2O3
 2NaAlO2 +CO2↑;
2NaAlO2 +CO2↑;③Cr2O72-+H2O
 2CrO42-+2H+
2CrO42-+2H+根据题意回答下列问题:
(1)操作I的名称是
(2)下表是相关物质的溶解度数据,操作III发生反应的化学方程式是:Na2Cr207 + 2KCl=K2Cr2O7 ↓+ 2NaCl,该反应在溶液中能发生的理由是
物质 | KCl | NaCl | K2Cr2O7 | Na2Cr2O7 | |
溶解度 (g/100g 水) | 0℃ | 28 | 35.7 | 4.7 | 163 |
40℃ | 40.1 | 36.4 | 26.3 | 215 | |
80℃ | 51.3 | 38 | 73 | 376 | |
(3)操作III有多步组成,获得K2Cr2O7晶体的操作依次是:加入KC1固体、蒸发浓缩、
(4)副产品Y主要含氢氧化铝,还含少量镁、铁的难溶化合物及可溶性杂质,精确分析Y中氢氧化铝含量的方法是称取n g样品,加入过量
(5)称取重铬酸钾试样2.500g配成250mL溶液,取出25mL与碘量瓶中,加入10mL 2mol/L H2SO4和足量碘化钾,放于暗处5min。然后加入100mL水,加入3mL 淀粉指示剂,用0.1000mol/LNa2SO3标准溶液滴定若实验中共用去Na2S2O3标准溶液47.40mL,则所得产品中重铬酸钾的纯度为
已知:①K2Cr2O7的摩尔质量为294g/mol
②Cr2O
 +6I-+14H+=2Cr3++3I2+7H2O;I2+2S2O
+6I-+14H+=2Cr3++3I2+7H2O;I2+2S2O =2I-+S4O
=2I-+S4O
您最近一年使用:0次
2016-12-09更新
|
803次组卷
|
3卷引用:2014-2015江苏省宿迁市高二下学期学业水平模拟化学试卷
2014-2015江苏省宿迁市高二下学期学业水平模拟化学试卷江苏省常州市联盟学校2022-2023学年高一下学期期末考试化学试题(已下线)综合期末压轴85+18题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
解题方法
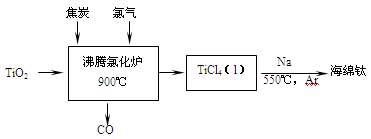
6 . 常温下钛的化学活性很小,在较高温度下可与多种物质反应。工业上由金红石(含TiO2大于96%)为原料生产钛的流程如下:
(1)TiCl4遇水强烈水解,写出其水解的化学方程式___________________ 。
(2)①若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是___________ 。
②Cl2含量检测仪工作原理如下图,则Cl2在Pt电极放电的电极反应式为_______ 。

③实验室也可用KClO3和浓盐酸制取Cl2,方程式为:KClO3+ 6HCl(浓) =" KCl" + 3Cl2↑+ 3H2O。
当生成6.72LCl2(标准状况下)时,转移的电子的物质的量为____ mol。
(3)一定条件下CO可以发生如下反应:4H2(g)+2CO(g) CH3OCH3(g)+H2O(g) △H。
CH3OCH3(g)+H2O(g) △H。
①该反应的平衡常数表达式为K=_____________ 。
②将合成气以n(H2)/n(CO)=2通入1 L的反应器中,CO的平衡转化率随温度、压强变化关系如图所示,下列判断正确的是___________ (填序号)。
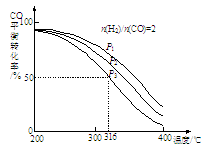
a.△H <0
b.P1<P2<P3
c.若在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO转化率小于50%
③采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(简称DME)。观察下图回答问题。
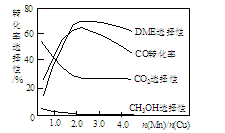
催化剂中n(Mn)/n(Cu)约为___________ 时最有利于二甲醚的合成。

(1)TiCl4遇水强烈水解,写出其水解的化学方程式
(2)①若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是
②Cl2含量检测仪工作原理如下图,则Cl2在Pt电极放电的电极反应式为

③实验室也可用KClO3和浓盐酸制取Cl2,方程式为:KClO3+ 6HCl(浓) =" KCl" + 3Cl2↑+ 3H2O。
当生成6.72LCl2(标准状况下)时,转移的电子的物质的量为
(3)一定条件下CO可以发生如下反应:4H2(g)+2CO(g)
 CH3OCH3(g)+H2O(g) △H。
CH3OCH3(g)+H2O(g) △H。①该反应的平衡常数表达式为K=
②将合成气以n(H2)/n(CO)=2通入1 L的反应器中,CO的平衡转化率随温度、压强变化关系如图所示,下列判断正确的是

a.△H <0
b.P1<P2<P3
c.若在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO转化率小于50%
③采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚(简称DME)。观察下图回答问题。

催化剂中n(Mn)/n(Cu)约为
您最近一年使用:0次
2015-03-20更新
|
1273次组卷
|
2卷引用:2015届江苏省泰州市姜堰区高三下学期期初联考化学试卷



