名校
1 . 完成下列问题。
(1)为了证明Ag+能将Fe2+氧化为Fe3+,某同学设计了如下图所示装置:
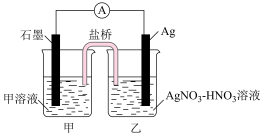
①其中甲溶液是_______ 。
②Ag电极为该电池的______ 极(填“阴或阳”或者“正或负”)
③该电池的总反应方程式为________ 。
(2)铵盐是一种重要的水体污染物。某课题组利用电解法,在含Cl-的水样中,探究将 转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:
转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:
①直接电氧化
在碱性条件下,阳极的电极反应式为______ 。
②间接电氧化
利用电解产生的Cl2,与H2O作用生成HClO进行脱氮。请写出HClO在酸性条件下氧化 的离子方程式
的离子方程式_____ 。25℃时,反应进行10min时,溶液的pH由6变为2时,其NH4+的平均反应速率为____ mol∙L−1∙min−1。
(1)为了证明Ag+能将Fe2+氧化为Fe3+,某同学设计了如下图所示装置:

①其中甲溶液是
②Ag电极为该电池的
③该电池的总反应方程式为
(2)铵盐是一种重要的水体污染物。某课题组利用电解法,在含Cl-的水样中,探究将
 转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:
转化为N2而脱氮的影响因素和反应机理。电解法脱氮的原理可能如下:①直接电氧化
在碱性条件下,阳极的电极反应式为
②间接电氧化
利用电解产生的Cl2,与H2O作用生成HClO进行脱氮。请写出HClO在酸性条件下氧化
 的离子方程式
的离子方程式
您最近一年使用:0次
2 . 某小组拟探究氯气的性质,设计如图实验(尾气处理装置略)。下列叙述错误的是
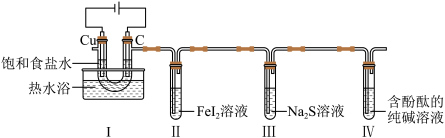
A.Ⅰ中逸出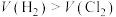 的原因是部分 的原因是部分 与碱、水反应及溶液中的 与碱、水反应及溶液中的 被氧化 被氧化 |
B.用 、KSCN溶液可确认Ⅱ中 、KSCN溶液可确认Ⅱ中 是否被氧化 是否被氧化 |
| C.Ⅲ中溶液变浑浊,则说明氯的非金属性比硫的强 |
D.Ⅳ中溶液由红色变为无色,说明 有漂白性 有漂白性 |
您最近一年使用:0次
解题方法
3 . 废旧金属的综合利用有利于节约资源、保护环境。工业上以赤铁矿(主要含 ,还含少量
,还含少量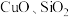 等杂质)为原料,制备
等杂质)为原料,制备 、回收
、回收 的工艺流程如下:
的工艺流程如下:
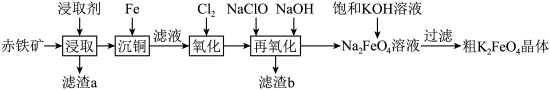
已知: 为难溶于盐酸、易溶于
为难溶于盐酸、易溶于 溶液的固体。
溶液的固体。
(1)“浸取”的方式为_________ (填“酸浸”“碱浸”或“水浸”)。
(2)“沉铜”过程中,发生还原反应的物质为_______ (填化学式)。
(3)“再氧化”中需要配制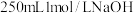 溶液。实验中除了量筒、烧杯、玻璃棒之外,还需要的玻璃仪器有
溶液。实验中除了量筒、烧杯、玻璃棒之外,还需要的玻璃仪器有______ ;“再氧化”制备 的离子方程式为:
的离子方程式为: ,
, 的名称为
的名称为______ ,X、Y代表的粒子符号依次为_______ 。
(4) 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 。从价态角度分析,
。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是________ 。
(5)“氧化”后,利用色度传感器测定其对光的透过率或者吸收率,颜色越深,吸收率越高。已知不同浓度 的标准液吸收率如下图。
的标准液吸收率如下图。
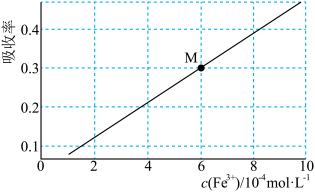
取 “氧化”后的溶液,稀释至
“氧化”后的溶液,稀释至 ,测得吸收率为上图中
,测得吸收率为上图中 点,则
点,则 该溶液中含铁元素的质量为
该溶液中含铁元素的质量为_____  ;已知色度传感器测定准确,实验制备的粗
;已知色度传感器测定准确,实验制备的粗 中铁元素质量偏低,其原因可能为
中铁元素质量偏低,其原因可能为___________ (任意回答一条原因)。
 ,还含少量
,还含少量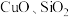 等杂质)为原料,制备
等杂质)为原料,制备 、回收
、回收 的工艺流程如下:
的工艺流程如下:
已知:
 为难溶于盐酸、易溶于
为难溶于盐酸、易溶于 溶液的固体。
溶液的固体。(1)“浸取”的方式为
(2)“沉铜”过程中,发生还原反应的物质为
(3)“再氧化”中需要配制
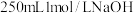 溶液。实验中除了量筒、烧杯、玻璃棒之外,还需要的玻璃仪器有
溶液。实验中除了量筒、烧杯、玻璃棒之外,还需要的玻璃仪器有 的离子方程式为:
的离子方程式为: ,
, 的名称为
的名称为(4)
 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 。从价态角度分析,
。从价态角度分析, 能处理氨氮废水的原因是
能处理氨氮废水的原因是(5)“氧化”后,利用色度传感器测定其对光的透过率或者吸收率,颜色越深,吸收率越高。已知不同浓度
 的标准液吸收率如下图。
的标准液吸收率如下图。
取
 “氧化”后的溶液,稀释至
“氧化”后的溶液,稀释至 ,测得吸收率为上图中
,测得吸收率为上图中 点,则
点,则 该溶液中含铁元素的质量为
该溶液中含铁元素的质量为 ;已知色度传感器测定准确,实验制备的粗
;已知色度传感器测定准确,实验制备的粗 中铁元素质量偏低,其原因可能为
中铁元素质量偏低,其原因可能为
您最近一年使用:0次
解题方法
4 . 回答下列问题。
I.酸雨是指 pH<5.6 的降水。
(1)下列气体中,与形成酸雨无关的是___________ 。
A.CO2 B.SO2 C.NOx
(2)从硫元素的化合价看,下列物质不具有氧化性的是___________。
Ⅱ.揭开浓硫酸的“神秘面纱”。
(3)在化工生产的过程中,一些试剂需要特殊的运输方式,比如具有强氧化性、强还原性、强腐蚀性等性质的试剂。通常情况下,下列物质可用铁制槽车装运的是___________。
I.酸雨是指 pH<5.6 的降水。
(1)下列气体中,与形成酸雨无关的是
A.CO2 B.SO2 C.NOx
(2)从硫元素的化合价看,下列物质不具有氧化性的是___________。
| A.Na2S | B.S | C.SO2 | D.H2SO4 |
Ⅱ.揭开浓硫酸的“神秘面纱”。
(3)在化工生产的过程中,一些试剂需要特殊的运输方式,比如具有强氧化性、强还原性、强腐蚀性等性质的试剂。通常情况下,下列物质可用铁制槽车装运的是___________。
| A.浓盐酸 | B.浓硫酸 | C.稀硫酸 | D.浓氢氧化钠溶液 |
您最近一年使用:0次
5 . 化合价和物质分类是认识物质的性质、实现物质之间转化的两个视角。回答下列问题。
(1)现有下列物质:
A. 溶液 B.
溶液 B. C.
C. 晶体 D.
晶体 D. E.
E. F.
F. 溶液 G.
溶液 G.
①上述物质中属于碱性氧化物的是___________ (填字母)。
② 与
与 反应的离子方程式为
反应的离子方程式为___________ 。
③ 溶于水的电离方程式为
溶于水的电离方程式为___________ 。
④氮氧化物是大气污染物,若要将NO转化为 ,从性质考虑,以上物质
,从性质考虑,以上物质 中可以选择与NO反应的是
中可以选择与NO反应的是___________ (填字母)。
(2)下图是部分含氯物质的“价-类”二维图。

①d表示的物质的化学式为___________ 。
②过程ⅰ、ⅱ、ⅲ的转化中属于氧化还原反应的有过程___________ (填编号)。
③表示b转化为f的离子方程式可以为___________ 。
(1)现有下列物质:
A.
 溶液 B.
溶液 B. C.
C. 晶体 D.
晶体 D. E.
E. F.
F. 溶液 G.
溶液 G.
①上述物质中属于碱性氧化物的是
②
 与
与 反应的离子方程式为
反应的离子方程式为③
 溶于水的电离方程式为
溶于水的电离方程式为④氮氧化物是大气污染物,若要将NO转化为
 ,从性质考虑,以上物质
,从性质考虑,以上物质 中可以选择与NO反应的是
中可以选择与NO反应的是(2)下图是部分含氯物质的“价-类”二维图。

①d表示的物质的化学式为
②过程ⅰ、ⅱ、ⅲ的转化中属于氧化还原反应的有过程
③表示b转化为f的离子方程式可以为
您最近一年使用:0次
名校
6 . 化学实验中的颜色变化,可将化学抽象之美具体为形象之美。下列叙述正确的是
A.将 通入水中所得溶液为黄绿色,说明 通入水中所得溶液为黄绿色,说明 与水不发生反应 与水不发生反应 |
B.向淀粉 溶液中通入 溶液中通入 ,溶液变成蓝色,说明 ,溶液变成蓝色,说明 的氧化性强于 的氧化性强于 |
C.向待测液中滴加 溶液,产生白色沉淀,说明待测液中含有 溶液,产生白色沉淀,说明待测液中含有 |
| D.用洁净的铂丝蘸取某溶液进行焰色试验,火焰呈黄色,说明该溶液一定为钠盐溶液 |
您最近一年使用:0次
名校
7 . 高温下,钠可以把 中的钛置换出来,反应的化学方程式为
中的钛置换出来,反应的化学方程式为 。下列说法错误的是
。下列说法错误的是
 中的钛置换出来,反应的化学方程式为
中的钛置换出来,反应的化学方程式为 。下列说法错误的是
。下列说法错误的是A.该反应中 表现了还原性 表现了还原性 |
B.该反应中还原性: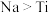 |
C.该反应中有 参与反应时,转移 参与反应时,转移 电子 电子 |
D.依该反应类推,将 投入 投入 稀溶液中,有红色物质生成 稀溶液中,有红色物质生成 |
您最近一年使用:0次
名校
解题方法
8 . 连二亚硫酸钠(Na2S2O4)俗称保险粉,广泛应用于纺织业和造纸业。利用碱性NaBH4溶液或Zn还原含硫化合物是制备Na2S2O4常用方法。
已知:①Na2S2O4在水溶液可以发生歧化反应(只有S元素化合价的升降),受热易分解。
②NaBH4是一种强还原剂,酸性或受热条件下易与水反应产生氢气,在碱性溶液中比较稳定。
③生成物的ΔG越大,表示在该条件下转化成该物质的可能性较大。溶液中部分含硫组分的ΔG如图所示。

Ⅰ.NaBH4碱性溶液还原法
(1)12%NaBH4碱性溶液配制:在烧杯中加入48g水,再向其中加入___________ (请完成溶液配制,所需试剂为40gNaOH固体及12gNaBH4固体)。
(2)溶有饱和SO2的NaHSO3溶液制备:利用如图所示装置来制备该溶液,判断制备完成的方法是___________ 。

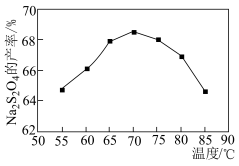
(3)将12%NaBH4碱性溶液与制备的NaHSO3溶液在无氧、水浴加热的条件下发生反应,相同时间内,Na2S2O4的产率随温度的变化如图所示,70℃后Na2S2O4的产率下降的原因是___________ 。Na2S2O4在水溶液中发生歧化反应的离子方程式为___________ 。
Ⅱ.锌粉还原法
已知:①Zn+2H2SO3 ZnS2O4(易溶于水)+2H2O;
ZnS2O4(易溶于水)+2H2O;
②二价锌在水溶液中的存在形式与pH的关系如图所示。
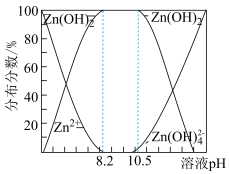
(4)请补充完整由锌粉制备Na2S2O4粗品的实验方案:向盛有水的烧杯中加入一定量的Zn粉,搅拌,___________ ,向滤液中加入氯化钠粉末至有大量晶体析出,过滤得到Na2S2O4粗品(实验中须使用的试剂:SO2、1mol·L-1NaOH溶液)。
已知:①Na2S2O4在水溶液可以发生歧化反应(只有S元素化合价的升降),受热易分解。
②NaBH4是一种强还原剂,酸性或受热条件下易与水反应产生氢气,在碱性溶液中比较稳定。
③生成物的ΔG越大,表示在该条件下转化成该物质的可能性较大。溶液中部分含硫组分的ΔG如图所示。

Ⅰ.NaBH4碱性溶液还原法
(1)12%NaBH4碱性溶液配制:在烧杯中加入48g水,再向其中加入
(2)溶有饱和SO2的NaHSO3溶液制备:利用如图所示装置来制备该溶液,判断制备完成的方法是

(3)将12%NaBH4碱性溶液与制备的NaHSO3溶液在无氧、水浴加热的条件下发生反应,相同时间内,Na2S2O4的产率随温度的变化如图所示,70℃后Na2S2O4的产率下降的原因是

Ⅱ.锌粉还原法
已知:①Zn+2H2SO3
 ZnS2O4(易溶于水)+2H2O;
ZnS2O4(易溶于水)+2H2O;②二价锌在水溶液中的存在形式与pH的关系如图所示。

(4)请补充完整由锌粉制备Na2S2O4粗品的实验方案:向盛有水的烧杯中加入一定量的Zn粉,搅拌,
您最近一年使用:0次
2024-02-22更新
|
343次组卷
|
2卷引用:江苏省南通市如东中学,如东一高等四校2023-2024学年高三上学期12月学情调研化学试题
解题方法
9 . 将 转化为有机物是实现“碳中和”的有效途径和研究热点。
转化为有机物是实现“碳中和”的有效途径和研究热点。
(1)通过电解法可将 转化为
转化为 的装置如图所示。
的装置如图所示。
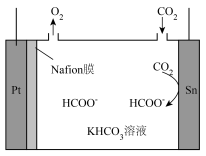
①写出阴极的电极反应式___________ 。
②已知:Nafion膜为一种阳离子交换膜,只允许阳离子及水分子通过,电池工作时在Pt电极覆盖一层Nafion膜的主要目的是___________ 。
(2)电解催化还原 用某复合金属作为电极时,复合金属吸附二氧化碳的位置不同,产物也不一样。复合金属优先与O原子结合,生成的产物主要为HCOOH.复合金属优先与C结合,生成的产物主要为
用某复合金属作为电极时,复合金属吸附二氧化碳的位置不同,产物也不一样。复合金属优先与O原子结合,生成的产物主要为HCOOH.复合金属优先与C结合,生成的产物主要为 或
或 。该复合金属催化还原
。该复合金属催化还原 可能的机理及各产物的物质的量分数如图所示,
可能的机理及各产物的物质的量分数如图所示,
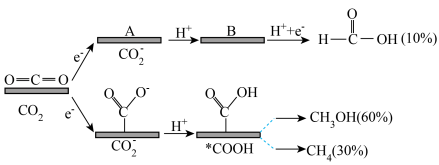
①画出图中中间体B的结构___________ 。
②若有 完全转化,反应过程中转移的电子数为
完全转化,反应过程中转移的电子数为___________ mol。
(3)铁水热法还原 转化为
转化为 的过程如下所示,
的过程如下所示,
制氢: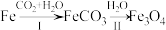
合成: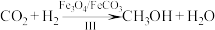
加热条件下,将一定量的Fe、 和
和 投入容器中进行反应,所得固体中各组分的质量分数及生成
投入容器中进行反应,所得固体中各组分的质量分数及生成 的体积随反应时间的变化如下表所示,
的体积随反应时间的变化如下表所示,
①书写步骤Ⅱ的化学反应方程式___________ 。
②从1小时后, 质量分数逐渐下降的主要原因是
质量分数逐渐下降的主要原因是___________ 。
 转化为有机物是实现“碳中和”的有效途径和研究热点。
转化为有机物是实现“碳中和”的有效途径和研究热点。(1)通过电解法可将
 转化为
转化为 的装置如图所示。
的装置如图所示。
①写出阴极的电极反应式
②已知:Nafion膜为一种阳离子交换膜,只允许阳离子及水分子通过,电池工作时在Pt电极覆盖一层Nafion膜的主要目的是
(2)电解催化还原
 用某复合金属作为电极时,复合金属吸附二氧化碳的位置不同,产物也不一样。复合金属优先与O原子结合,生成的产物主要为HCOOH.复合金属优先与C结合,生成的产物主要为
用某复合金属作为电极时,复合金属吸附二氧化碳的位置不同,产物也不一样。复合金属优先与O原子结合,生成的产物主要为HCOOH.复合金属优先与C结合,生成的产物主要为 或
或 。该复合金属催化还原
。该复合金属催化还原 可能的机理及各产物的物质的量分数如图所示,
可能的机理及各产物的物质的量分数如图所示,
①画出图中中间体B的结构
②若有
 完全转化,反应过程中转移的电子数为
完全转化,反应过程中转移的电子数为(3)铁水热法还原
 转化为
转化为 的过程如下所示,
的过程如下所示,制氢:
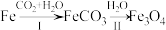
合成:
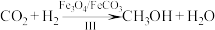
加热条件下,将一定量的Fe、
 和
和 投入容器中进行反应,所得固体中各组分的质量分数及生成
投入容器中进行反应,所得固体中各组分的质量分数及生成 的体积随反应时间的变化如下表所示,
的体积随反应时间的变化如下表所示,| 反应时间(小时) | Fe(%) |  (%) (%) |  (%) (%) |  (mL) (mL) |
| 1 | 47.3 | 19.1 | 33.6 | 260 |
| 2 | 46.9 | 20.1 | 33 | 370 |
| 3 | 45.5 | 25.5 | 30 | 400 |
| 4 | 36.8 | 37.6 | 25.6 | 480 |
②从1小时后,
 质量分数逐渐下降的主要原因是
质量分数逐渐下降的主要原因是
您最近一年使用:0次
10 . 钛(T)被称为“未来金属”,钛合金广泛应用于多个领域。
(1)工业上由钛铁矿(主要成分为 )在高温下经氯化得到
)在高温下经氯化得到 ,再制取金属钛的流程如图
,再制取金属钛的流程如图

① 元素在元素周期表的位置是
元素在元素周期表的位置是_______ 。
②基态 原子的简化电子排布式是
原子的简化电子排布式是_______ 。
③补全反应器中发生反应的化学方程式:_______ 。

④由合成器得到的粗产品是 、
、 、
、 的混合物,可采用真空蒸馏的方法分离得到
的混合物,可采用真空蒸馏的方法分离得到 。依据下表信息,加热的温度略高于
。依据下表信息,加热的温度略高于_______  即可。
即可。
(2)超高硬度生物材料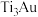 合金是理想的人工髋关节和膝关节材料,其晶体有
合金是理想的人工髋关节和膝关节材料,其晶体有 、
、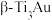 两种结构,如下图所示。
两种结构,如下图所示。

① 晶胞中,
晶胞中, 原子周围与它最近且距离相等的
原子周围与它最近且距离相等的 原子有
原子有_______ 个。
②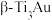 的晶胞边长为
的晶胞边长为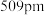 ,每个晶胞面上有两个
,每个晶胞面上有两个 原子。
原子。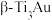 晶体的密度是
晶体的密度是_______  (列出计算式)。(已知:阿伏加德罗常数为
(列出计算式)。(已知:阿伏加德罗常数为 ,
,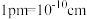 )
)
③与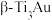 晶体相比,
晶体相比, 晶体有更长的
晶体有更长的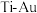 键键长。上述两种晶体中硬度较高的是
键键长。上述两种晶体中硬度较高的是_______ (填“ ”或“
”或“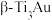 ”)。
”)。
(1)工业上由钛铁矿(主要成分为
 )在高温下经氯化得到
)在高温下经氯化得到 ,再制取金属钛的流程如图
,再制取金属钛的流程如图
①
 元素在元素周期表的位置是
元素在元素周期表的位置是②基态
 原子的简化电子排布式是
原子的简化电子排布式是③补全反应器中发生反应的化学方程式:

④由合成器得到的粗产品是
 、
、 、
、 的混合物,可采用真空蒸馏的方法分离得到
的混合物,可采用真空蒸馏的方法分离得到 。依据下表信息,加热的温度略高于
。依据下表信息,加热的温度略高于 即可。
即可。 |  |  |  | |
熔点/ |  | 648.8 | 714 | 1667 |
沸点/ | 136.4 | 1090 | 1412 | 3287 |
(2)超高硬度生物材料
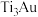 合金是理想的人工髋关节和膝关节材料,其晶体有
合金是理想的人工髋关节和膝关节材料,其晶体有 、
、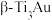 两种结构,如下图所示。
两种结构,如下图所示。
①
 晶胞中,
晶胞中, 原子周围与它最近且距离相等的
原子周围与它最近且距离相等的 原子有
原子有②
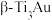 的晶胞边长为
的晶胞边长为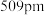 ,每个晶胞面上有两个
,每个晶胞面上有两个 原子。
原子。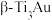 晶体的密度是
晶体的密度是 (列出计算式)。(已知:阿伏加德罗常数为
(列出计算式)。(已知:阿伏加德罗常数为 ,
,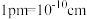 )
)③与
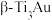 晶体相比,
晶体相比, 晶体有更长的
晶体有更长的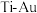 键键长。上述两种晶体中硬度较高的是
键键长。上述两种晶体中硬度较高的是 ”或“
”或“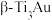 ”)。
”)。
您最近一年使用:0次



