1 . 已知反应:①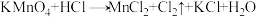 、②
、②
 、③
、③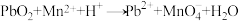 (方程式均未配平)。下列说法正确的是
(方程式均未配平)。下列说法正确的是
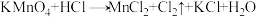 、②
、②
 、③
、③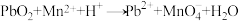 (方程式均未配平)。下列说法正确的是
(方程式均未配平)。下列说法正确的是A.反应③中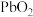 发生氧化反应 发生氧化反应 |
| B.反应①中氧化剂与还原剂的物质的量之比为1:8 |
C.氧化性: |
| D.反应①和②中生成相同质量的氯气时,消耗HCl的物质的量之比为5:4 |
您最近半年使用:0次
2022-10-10更新
|
338次组卷
|
3卷引用:皖豫名校联盟2022-2023学年高三毕业班第一次联考化学试题
解题方法
2 . 为验证木炭与浓硫酸反应生成的气体M含有CO2和SO2,可按下图进行实验。各装置中可供选择的试剂是:①澄清石灰水,②品红溶液,③酸性高锰酸钾溶液。判断各装置所盛试剂后,请回答:
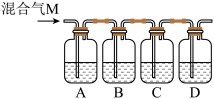
(1)A中所盛放的试剂是_______ (填写试剂序号)。
(2)B中的实验现象_______ ,B装置的作用是_______ 。
(3)C中所盛试剂是_______ (填写试剂序号),C装置的作用是_______ 。
(4)D中所盛试剂应是_______ (填写试剂序号),作用是_______ 。
(5)配平下列方程式
①_______
________Cu2S+_______HNO3=_______Cu(NO3)2+_______H2SO4+_______NO↑+_______H2O
②_______
_______MnO +_______H2O2+_______H+=_______Mn2++_______O2↑+_______H2O
+_______H2O2+_______H+=_______Mn2++_______O2↑+_______H2O
(6)油画所用的颜料含有某种白色铅化合物,置于空气中,天长日久就会生成黑色PbS,从而使油画色彩变暗,若用H2O2来擦拭,则可将PbS转化为白色的PbSO4而使油画恢复光彩。问:这一过程的化学方程式:_______ 。

(1)A中所盛放的试剂是
(2)B中的实验现象
(3)C中所盛试剂是
(4)D中所盛试剂应是
(5)配平下列方程式
①
________Cu2S+_______HNO3=_______Cu(NO3)2+_______H2SO4+_______NO↑+_______H2O
②
_______MnO
 +_______H2O2+_______H+=_______Mn2++_______O2↑+_______H2O
+_______H2O2+_______H+=_______Mn2++_______O2↑+_______H2O(6)油画所用的颜料含有某种白色铅化合物,置于空气中,天长日久就会生成黑色PbS,从而使油画色彩变暗,若用H2O2来擦拭,则可将PbS转化为白色的PbSO4而使油画恢复光彩。问:这一过程的化学方程式:
您最近半年使用:0次
3 . 回答下列问题:
(1)配平下列化学方程式(将系数填在横线上),并写出还原剂。___NH3+___O2=___N2+___H2O____ ,该反应中的还原剂是____ 。
(2)在反应2Na2O2+2H2O=4NaOH+O2↑中,还原剂是___ ,生成1molO2转移电子的物质的量为___ 。
(1)配平下列化学方程式(将系数填在横线上),并写出还原剂。___NH3+___O2=___N2+___H2O
(2)在反应2Na2O2+2H2O=4NaOH+O2↑中,还原剂是
您最近半年使用:0次
名校
解题方法
4 . 某同学在实验室欲配制物质的量浓度均为1.0mol·L-1的NaOH溶液、稀硫酸各450mL。提供的试剂是:NaOH固体、18.4mol·L-1的浓硫酸(密度为1.84g·cm-3)和蒸馏水。
(1)请你观察图示判断其中不正确的操作有_______ 。(填序号)
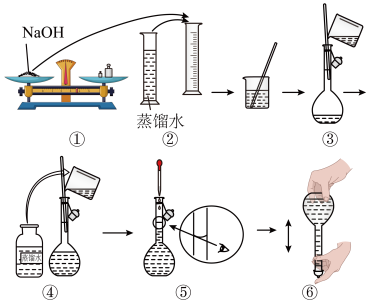
(2)应用托盘天平称量NaOH_______ g,应用量筒量取浓硫酸_______ mL。
(3)在配制上述溶液实验中,下列操作引起结果偏低的有_______ 。
A.该学生在量取浓硫酸时,仰视刻度线
B.溶解硫酸后没有冷却至室温就立即完成后面的配制操作
C.在烧杯中溶解搅拌时,溅出少量溶液
D.没有用蒸馏水洗涤烧杯2~3次,并将洗涤液移入容量瓶中
E.将量筒洗涤2~3次,并全部转移至容量瓶中
F.容量瓶中原来存有少量蒸馏水
G.胶头滴管加水定容时俯视刻度线
(4)若用0.01000mol·L-1K2Cr2O7(酸性)溶液滴定20.00mL未知浓度的含Fe2+的溶液,恰好完全反应时消10.00mLK2Cr2O7溶液,写出该反应的离子反应方程式_______ ,待测液中Fe2+的浓度是_______ g/L(保留4位有效数字)。
(1)请你观察图示判断其中不正确的操作有

(2)应用托盘天平称量NaOH
(3)在配制上述溶液实验中,下列操作引起结果偏低的有
A.该学生在量取浓硫酸时,仰视刻度线
B.溶解硫酸后没有冷却至室温就立即完成后面的配制操作
C.在烧杯中溶解搅拌时,溅出少量溶液
D.没有用蒸馏水洗涤烧杯2~3次,并将洗涤液移入容量瓶中
E.将量筒洗涤2~3次,并全部转移至容量瓶中
F.容量瓶中原来存有少量蒸馏水
G.胶头滴管加水定容时俯视刻度线
(4)若用0.01000mol·L-1K2Cr2O7(酸性)溶液滴定20.00mL未知浓度的含Fe2+的溶液,恰好完全反应时消10.00mLK2Cr2O7溶液,写出该反应的离子反应方程式
您最近半年使用:0次
2022-08-30更新
|
323次组卷
|
2卷引用:宁夏回族自治区银川一中2022-2023学年高三上学期第一次月考理科综合化学试题
2021高三·全国·专题练习
解题方法
5 . 水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+xOH-Fe3O4↓+S4O
+O2+xOH-Fe3O4↓+S4O +2H2O,反应的离子方程式中x=2。
+2H2O,反应的离子方程式中x=2。_______
 +O2+xOH-Fe3O4↓+S4O
+O2+xOH-Fe3O4↓+S4O +2H2O,反应的离子方程式中x=2。
+2H2O,反应的离子方程式中x=2。
您最近半年使用:0次
名校
解题方法
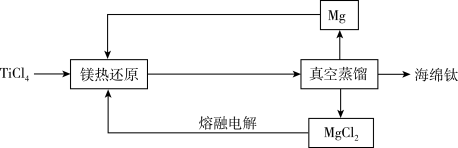
6 . Ti具备优良的抗腐蚀性,被称为未来金属,工业上可以采用铁热还原法高温制备,工艺流程如下;已知: ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是 
| A.Mg的循环使用可以提高原料利用率,降低成本 |
B.热还原的化学方程式为: |
| C.Ti和Mg高温下化学性质非常活泼,镁还原需在惰性气氛中进行 |
| D.整个工艺流程中,Cl元素化合价始终不变 |
您最近半年使用:0次
2022高三·全国·专题练习
7 . 在反应式:aFeCl2+bKNO3+cHCl=dFeCl3+eKCl+fX+gH2O中,若b=1,d=3,则X的分子式为N2。(______)
您最近半年使用:0次
名校
8 .  溶液是一种常见的强氧化剂,
溶液是一种常见的强氧化剂, 的酸性
的酸性 溶液恰好把
溶液恰好把 的草酸(H2C2O4)完全氧化,产物中铬元素的化合价为
的草酸(H2C2O4)完全氧化,产物中铬元素的化合价为
 溶液是一种常见的强氧化剂,
溶液是一种常见的强氧化剂, 的酸性
的酸性 溶液恰好把
溶液恰好把 的草酸(H2C2O4)完全氧化,产物中铬元素的化合价为
的草酸(H2C2O4)完全氧化,产物中铬元素的化合价为| A.+1 | B.+2 | C.+3 | D.+4 |
您最近半年使用:0次
2022-07-07更新
|
375次组卷
|
2卷引用:四川省成都市2021-2022学年高一下学期期末化考试学试题
9 . 化学是一门实用性很强的科学,请根据题意填空:
(1)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装_______ (填“浓硫酸”或“浓盐酸”)。
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是_______ (填“SiO2”或“Na2SiO3”)。
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式:2CO+2NO 2CO2 +
2CO2 +_______ 。
(1)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装
(2)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是
(3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式:2CO+2NO
 2CO2 +
2CO2 +
您最近半年使用:0次
名校
10 . Ⅰ.某地出现硫酸型酸雨,现采集了一份雨水样品,其pH随时间变化如下:
(1)用化学方程式表示雨水样品pH变化的原因_______ 。
(2)如将刚采集到的雨水样品与自来水混合(自来水含氯气),pH将_______ (选填“变大”、“变小”、“不变”)。发生反应的化学方程式为_______ 。
(3)为了防治酸雨,降低煤燃烧时产生的SO2,工业上将生石灰(CaO)与含硫煤混合使用制取石膏,请写出燃烧时,有关“固硫”的方程式:_______ 。
Ⅱ.如图是土壤中发生的氮循环示意图,回答下列问题:
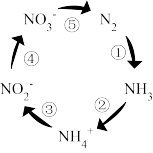
(4)固氮过程的序号是_______ 。人工固氮的反应方程式为_______ 。在细菌微生物的作用下可实现反硝化作用,实现转化的序号为_______ 。为了消除NOx对大气的污染,工业上通常利用NH3还原的方法实现无害化处理,配平NO2与NH3反应的化学方程式:_______ 。
(5)现有NO2和NO的混合气体3L,可用相同状况下3.5L的NH3恰好使其完全转化为N2,则混合气体中NO2和NO体积之比为_______ 。
| 测试时间/h | 0 | 2 | 4 | 6 |
| pH | 4.73 | 4.55 | 4.42 | 4.41 |
(1)用化学方程式表示雨水样品pH变化的原因
(2)如将刚采集到的雨水样品与自来水混合(自来水含氯气),pH将
(3)为了防治酸雨,降低煤燃烧时产生的SO2,工业上将生石灰(CaO)与含硫煤混合使用制取石膏,请写出燃烧时,有关“固硫”的方程式:
Ⅱ.如图是土壤中发生的氮循环示意图,回答下列问题:

(4)固氮过程的序号是
(5)现有NO2和NO的混合气体3L,可用相同状况下3.5L的NH3恰好使其完全转化为N2,则混合气体中NO2和NO体积之比为
您最近半年使用:0次



