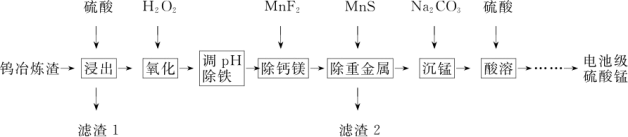
1 . 钨冶炼渣主要含锰、铁、钙、镁、硅的氧化物及少量重金属盐。工业上利用钨冶炼渣制备电池级硫酸锰(含MnSO4的质量分数98%以上)的工艺如图所示。
回答下列问题:
(1)为提高钨冶炼渣的浸出速率,可采用的方法有___________ (写出2种)。“滤渣 1”的主要成分是___________ 。
(2)写出“氧化”步骤的离子方程式___________ 。
(3)“调 pH除铁”步骤中的最优试剂是___________ 。
A.H2SO4 B.CO2 C.NaOH D.MnCO3
(4)为使Ca2+和 Mg2+完全沉淀,除去钙镁后的溶液中c(F-)应不低于___________ mol/L。[已知:Ksp(CaF2)=1.6×10-10,Ksp(MgF2)=9×10-11]。
(5)“沉锰”步骤的化学方程式为___________ 。

回答下列问题:
(1)为提高钨冶炼渣的浸出速率,可采用的方法有
(2)写出“氧化”步骤的离子方程式
(3)“调 pH除铁”步骤中的最优试剂是
A.H2SO4 B.CO2 C.NaOH D.MnCO3
(4)为使Ca2+和 Mg2+完全沉淀,除去钙镁后的溶液中c(F-)应不低于
(5)“沉锰”步骤的化学方程式为
您最近一年使用:0次
2021-01-14更新
|
283次组卷
|
4卷引用:辽宁省2020-2021学年高二上学期期末考试化学试题
解题方法
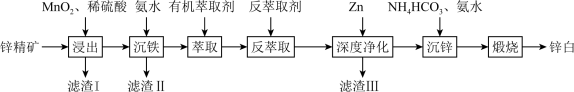
2 . 氧化锌又称锌白,作为添加剂在多种材料和产品中有广泛应用,一种以锌精矿(主要成分是ZnS,还有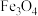 、CuO、
、CuO、 等杂质)为原料制备锌白的工艺流程如下:
等杂质)为原料制备锌白的工艺流程如下:
已知:25℃时相关物质的 如下表:
如下表:
回答下列问题:
(1)滤渣Ⅰ的主要成分除过量 外,还有S和
外,还有S和_______ (填化学式)。“浸出”时, 氧化ZnS的离子方程式为
氧化ZnS的离子方程式为_______ 。
(2)“沉铁”时,滴加氨水需要调节pH最低为_______ (通常认为残留在溶液中离子浓度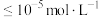 时,沉淀完全)。
时,沉淀完全)。
(3)“萃取,反萃取”时发生的反应是 。有机萃取剂能分离
。有机萃取剂能分离 和
和 ,为了提高反萃取效率,反萃取剂应该呈
,为了提高反萃取效率,反萃取剂应该呈_______ (填“酸”“碱”或“中”)性。
(4)“深度净化”中加Zn的目的是_______ 。
(5)“沉锌”时,恰好完全反应,过滤、洗涤得到碱式碳酸锌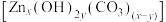 ,反应的离子方程式为
,反应的离子方程式为_______ 。检验沉淀洗涤干净的方法是_______ 。
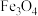 、CuO、
、CuO、 等杂质)为原料制备锌白的工艺流程如下:
等杂质)为原料制备锌白的工艺流程如下:
已知:25℃时相关物质的
 如下表:
如下表:| 物质 |  |  |  |  |  |
 | 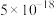 | 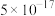 | 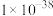 | 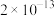 |  |
(1)滤渣Ⅰ的主要成分除过量
 外,还有S和
外,还有S和 氧化ZnS的离子方程式为
氧化ZnS的离子方程式为(2)“沉铁”时,滴加氨水需要调节pH最低为
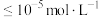 时,沉淀完全)。
时,沉淀完全)。(3)“萃取,反萃取”时发生的反应是
 。有机萃取剂能分离
。有机萃取剂能分离 和
和 ,为了提高反萃取效率,反萃取剂应该呈
,为了提高反萃取效率,反萃取剂应该呈(4)“深度净化”中加Zn的目的是
(5)“沉锌”时,恰好完全反应,过滤、洗涤得到碱式碳酸锌
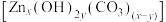 ,反应的离子方程式为
,反应的离子方程式为
您最近一年使用:0次
解题方法
3 . 利用软锰矿(主要成分是 ,其中还含有少量
,其中还含有少量 、MgO、CaO、
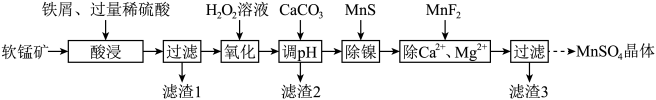
、MgO、CaO、 )生产高纯硫酸锰晶体的一种工艺流程如下:
)生产高纯硫酸锰晶体的一种工艺流程如下:
已知:常温下, ,
, ,
, ,
, 。
。
回答下列问题:
(1)“酸浸”前将矿石粉碎的目的是_______ ;“酸浸”后溶液中检测到 、
、 ,则此过程中铁屑与软锰矿反应的化学方程式为
,则此过程中铁屑与软锰矿反应的化学方程式为________ ;“滤渣1”的主要成分为________ (填化学式)。
(2)“氧化”时发生反应的离子方程式为___________ ,“调pH”的目的是___________ 。
(3)“除镍”时,使用MnS作为沉淀剂的原因是___________ 。
(4)加入 使
使 、
、 的浓度均不高于
的浓度均不高于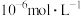 ,此时溶液中
,此时溶液中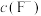 至少为
至少为_______  。
。
(5)硫酸锰的溶解度随温度变化关系如图所示,从“除 、
、 ”所得滤液中获得硫酸锰晶体的方法是
”所得滤液中获得硫酸锰晶体的方法是________ 。

 ,其中还含有少量
,其中还含有少量 、MgO、CaO、
、MgO、CaO、 )生产高纯硫酸锰晶体的一种工艺流程如下:
)生产高纯硫酸锰晶体的一种工艺流程如下:
已知:常温下,
 ,
, ,
, ,
, 。
。回答下列问题:
(1)“酸浸”前将矿石粉碎的目的是
 、
、 ,则此过程中铁屑与软锰矿反应的化学方程式为
,则此过程中铁屑与软锰矿反应的化学方程式为(2)“氧化”时发生反应的离子方程式为
(3)“除镍”时,使用MnS作为沉淀剂的原因是
(4)加入
 使
使 、
、 的浓度均不高于
的浓度均不高于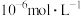 ,此时溶液中
,此时溶液中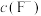 至少为
至少为 。
。(5)硫酸锰的溶解度随温度变化关系如图所示,从“除
 、
、 ”所得滤液中获得硫酸锰晶体的方法是
”所得滤液中获得硫酸锰晶体的方法是
您最近一年使用:0次
解题方法
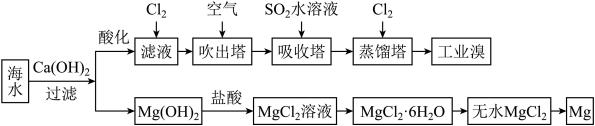
4 . 海水中蕴藏着大量资源,利用海水可提取溴和镁,主要工业生产流程如下图所示:
请回答下列问题。
(1)吸收塔中发生的主要反应的离子方程式为___________ 。
(2)提取溴的过程中,经过两次 的转化,其目的是
的转化,其目的是___________ 。
(3)吹出塔吹出的含溴空气经由吸收塔吸收溴后回到吹出塔进行循环利用。吹出塔中 吹出率与吸收塔中
吹出率与吸收塔中 流量的关系如图所示。
流量的关系如图所示。
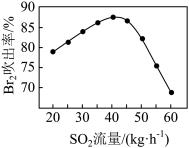
 流量过大,
流量过大, 吹出率反而下降的原因是
吹出率反而下降的原因是___________ 。
(4)工业上也可用 溶液吸收吹出的
溶液吸收吹出的 ,将以下方程式补充完整。
,将以下方程式补充完整。________
___________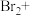 ___________
___________ ___________
___________ __________
__________
 ___________
___________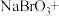 ___________
___________
(5)从 溶液中得到
溶液中得到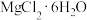 晶体的主要操作为
晶体的主要操作为___________ 、___________ 、过滤、洗涤、干燥(在HCl气流的保护下)。
(6)工业上用无水氯化镁得到金属镁的冶炼方法为___________ 。
(7)请写出上述过程中可以循环利用的一种物质___________ 。(写出化学式)。

请回答下列问题。
(1)吸收塔中发生的主要反应的离子方程式为
(2)提取溴的过程中,经过两次
 的转化,其目的是
的转化,其目的是(3)吹出塔吹出的含溴空气经由吸收塔吸收溴后回到吹出塔进行循环利用。吹出塔中
 吹出率与吸收塔中
吹出率与吸收塔中 流量的关系如图所示。
流量的关系如图所示。
 流量过大,
流量过大, 吹出率反而下降的原因是
吹出率反而下降的原因是(4)工业上也可用
 溶液吸收吹出的
溶液吸收吹出的 ,将以下方程式补充完整。
,将以下方程式补充完整。___________
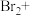 ___________
___________ ___________
___________ __________
__________
 ___________
___________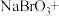 ___________
___________
(5)从
 溶液中得到
溶液中得到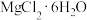 晶体的主要操作为
晶体的主要操作为(6)工业上用无水氯化镁得到金属镁的冶炼方法为
(7)请写出上述过程中可以循环利用的一种物质
您最近一年使用:0次
5 . 黄铁矿(FeS2)中-1价硫元素在酸性条件下可以与ClO3-发生反应,其离子方程式如下
_____ ClO3-+_____ FeS2+_____H+=_____ClO2↑+_____Fe3++_____ SO42-+_____H2O(未配平):下列说法正确的是
_____ ClO3-+_____ FeS2+_____H+=_____ClO2↑+_____Fe3++_____ SO42-+_____H2O(未配平):下列说法正确的是
| A. ClO3-是氧化剂,Fe3+是还原产物 |
| B. ClO3-的氧化性强于Fe3+ |
| C.生成l mol SO42-时,转移7mol 电子 |
| D.取反应后的溶液加KSCN溶液,可观察到有红色沉淀产生 |
您最近一年使用:0次
2020-02-20更新
|
471次组卷
|
3卷引用:辽宁师范大学附属中学2017-2018学年高一上学期期末考试化学试题
辽宁师范大学附属中学2017-2018学年高一上学期期末考试化学试题2020届高三化学化学二轮复习——高考常考题:氧化还原反应的规律:先后律、强弱律【精编选择25题】(已下线)考点05 氧化还原反应方程式的配平与计算(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)
名校
解题方法
6 . 高锰酸钾是中学常用的试剂。工业上用软锰矿制备高锰酸钾流程。
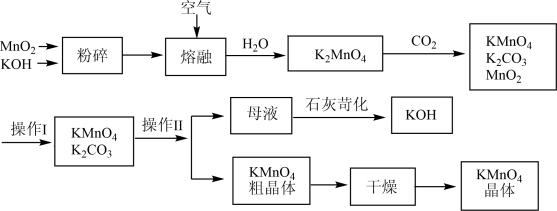
(1)上述流程中可以循环使用的物质有________ 、________ (写化学式)。
(2)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是________ (填代号)。
a.84消毒液(NaClO溶液) b.75%酒精c.苯酚
(3)理论上(若不考虑物质循环与制备过程中的损失)1molMnO2可制得________ molKMnO4。
(4)操作Ⅰ的名称是________ ;操作Ⅱ根据KMnO4和K2CO3两物质在________ (填性质)上的差异,采用________ (填操作步骤)、趁热过滤得到KMnO4粗晶体。

(1)上述流程中可以循环使用的物质有
(2)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是
a.84消毒液(NaClO溶液) b.75%酒精c.苯酚
(3)理论上(若不考虑物质循环与制备过程中的损失)1molMnO2可制得
(4)操作Ⅰ的名称是
您最近一年使用:0次
2020-04-27更新
|
441次组卷
|
2卷引用:辽宁省丹东市2017-2018学年高二下学期期末质量监测化学试题
7 . 次磷酸钙[Ca(H2PO2)2,该化合物中H是+1价,O是-2价]可用作阻燃剂,食品添加剂和动物营养剂,制备次磷酸钙的反应化学方程式为:Ca(OH)2+P4+H2O→Ca(H2PO2)2+PH3↑(未配平),下列说法错误的是
| A.Ca(H2PO2)2为氧化产物 |
| B.氧化剂与还原剂物质的量之比为1:3 |
| C.生成1molPH3消耗31gP4 |
| D.次磷酸钙具有还原性 |
您最近一年使用:0次
2021-01-15更新
|
261次组卷
|
2卷引用:辽宁省丹东市2020-2021学年高一上学期期末考试化学试题
名校
解题方法
8 . 某兴趣小组利用经过初步处理的含有Fe2+的废液制备硫酸亚铁晶体的流程如图:____ ,若NaHCO3溶液浓度偏低可能会形成胶体,验证的方法为____ 。
(2)加入铁粉的作用是____ 。
(3)测定废液中Fe2+的浓度可使用已知浓度的酸性高锰酸钾溶液。配平下面方程式,并用双线桥法表示电子转移过程:____ 。
KMnO4+___FeSO4+___H2SO4=___MnSO4+___K2SO4+___Fe2(SO4)3+___H2O。
(4)已知Fe2+与NaHCO3按物质的量1:2的比例恰好完全反应,该反应的离子方程式为____ 。
(5)硫酸亚铁在空气中煅烧生成Fe2O3和一种酸性氧化物,该反应的化学方程式为____ ,该反应中每产生1molFe2O3,转移的电子数为____ NA。

(2)加入铁粉的作用是
(3)测定废液中Fe2+的浓度可使用已知浓度的酸性高锰酸钾溶液。配平下面方程式,并用双线桥法表示电子转移过程:
KMnO4+___FeSO4+___H2SO4=___MnSO4+___K2SO4+___Fe2(SO4)3+___H2O。
(4)已知Fe2+与NaHCO3按物质的量1:2的比例恰好完全反应,该反应的离子方程式为
(5)硫酸亚铁在空气中煅烧生成Fe2O3和一种酸性氧化物,该反应的化学方程式为
您最近一年使用:0次
2022-03-16更新
|
220次组卷
|
2卷引用:辽宁省渤海大学附属高级中学2021-2022学年高一上学期期末质量检测化学试题
9 . 肼(N2H4),又称联氨,为无色油状液体,能很好地混溶于水中,与卤素、过氧化氢等强氧化剂作用能自燃,长期暴露在空气中或短时间受高温作用会爆炸分解,具有强烈的吸水性。实验室设计如图装置用氨和次氯酸钠反应制备肼,并探究肼的性质。
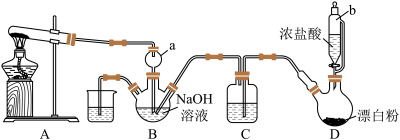
已知:硫酸肼(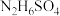 )为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。
)为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。
回答下列问题:
(1)仪器a的作用是_______ 。
(2)装置A的试管中盛放的试剂为_______ (填化学式)。
(3)装置C中盛放的试剂为_______ (填名称),其作用是_______ 。
(4)装置D中发生反应的化学方程式为_______ 。
(5)①探究性质。取装置B中溶液于试管中,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到结晶。写出生成结晶的离子方程式:_______ 。
②测定产品中肼的质量分数。称取 g装置B中溶液,加入适量
g装置B中溶液,加入适量 固体(滴定过程中,调节溶液的
固体(滴定过程中,调节溶液的 保持在6.5左右),加水配成100
保持在6.5左右),加水配成100 溶液,移取25.00
溶液,移取25.00 置于锥形瓶中,并滴加2~3滴淀粉溶液作指示剂,用c
置于锥形瓶中,并滴加2~3滴淀粉溶液作指示剂,用c 的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定终点的颜色变化为
的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定终点的颜色变化为_______ ,滴定终点平均消耗标准溶液V ,产品中肼的质量分数的表达式为
,产品中肼的质量分数的表达式为_______ 。

已知:硫酸肼(
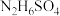 )为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。
)为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。回答下列问题:
(1)仪器a的作用是
(2)装置A的试管中盛放的试剂为
(3)装置C中盛放的试剂为
(4)装置D中发生反应的化学方程式为
(5)①探究性质。取装置B中溶液于试管中,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到结晶。写出生成结晶的离子方程式:
②测定产品中肼的质量分数。称取
 g装置B中溶液,加入适量
g装置B中溶液,加入适量 固体(滴定过程中,调节溶液的
固体(滴定过程中,调节溶液的 保持在6.5左右),加水配成100
保持在6.5左右),加水配成100 溶液,移取25.00
溶液,移取25.00 置于锥形瓶中,并滴加2~3滴淀粉溶液作指示剂,用c
置于锥形瓶中,并滴加2~3滴淀粉溶液作指示剂,用c 的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定终点的颜色变化为
的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定终点的颜色变化为 ,产品中肼的质量分数的表达式为
,产品中肼的质量分数的表达式为
您最近一年使用:0次
10 . 某工厂制备Cr(OH)3的工艺流程如图所示:
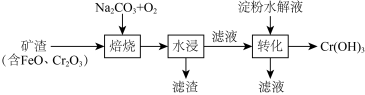
已知:焙烧后Cr元素以+6价的形式存在。
下列说法正确的是

已知:焙烧后Cr元素以+6价的形式存在。
下列说法正确的是
| A.Na2CO3俗称水玻璃 |
| B.FeO、Cr2O3、O2均不溶于稀盐酸 |
C.焙烧时发生反应的化学方程式可能为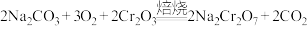 |
| D.淀粉水解液能产生丁达尔效应,且其在转化时的主要作用为作催化剂 |
您最近一年使用:0次



