1 . 高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中Na2O2是_______ (填氧化剂、还原剂)
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:_______ 。
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为_______ mol
(1)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中Na2O2是
(2)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①碱性条件下,氧化剂和还原剂的物质的量的比为3:2发生反应,写出并配平湿法制高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3mol电子,则还原产物的物质的量为
您最近一年使用:0次
名校
2 . Ⅰ、现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氯化镁;⑦Na2O2;⑧氨水;⑨NaHSO4;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的有___________ ,属于非电解质的有___________ 。
(2)④的电子式为___________ 。
(3)用电子式表示⑥的形成过程___________ 。
(4)除去③中少量②的化学方程式为___________ 。
(5)⑦中含有的化学键为___________
Ⅱ、写出下列反应的离子方程式(已知还原性: ):
):
(6)向 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为
的化学计量数之比为 :
:___________ 。
(1)上述十种物质中,属于电解质的有
(2)④的电子式为
(3)用电子式表示⑥的形成过程
(4)除去③中少量②的化学方程式为
(5)⑦中含有的化学键为
Ⅱ、写出下列反应的离子方程式(已知还原性:
 ):
):(6)向
 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为
的化学计量数之比为 :
:
您最近一年使用:0次
名校
解题方法
3 . Ⅰ.现有下列十种物质:①液态氯化氢;②小苏打;③固体纯碱;④二氧化碳;⑤葡萄糖;⑥氯化镁;⑦ ;⑧氨水;⑨
;⑧氨水;⑨ ;⑩硫酸铁溶液。
;⑩硫酸铁溶液。
(1)上述十种物质中,属于电解质的有___________ ,属于非电解质的有___________ 。
(2)④的电子式为___________ 。
(3)用电子式表示⑥的形成过程___________ 。
(4)除去③中少量②的操作是___________ ,化学方程式为___________ 。
(5)⑦中含有的化学键为___________ 。
(6)⑨在水溶液中的电离方程式为___________ 。
Ⅱ.写出下列反应的离子方程式(已知还原性: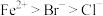 ):
):
(7)向 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 )
)___________ ;
(8)向 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为1∶l∶
的化学计量数之比为1∶l∶___________ 。
 ;⑧氨水;⑨
;⑧氨水;⑨ ;⑩硫酸铁溶液。
;⑩硫酸铁溶液。(1)上述十种物质中,属于电解质的有
(2)④的电子式为
(3)用电子式表示⑥的形成过程
(4)除去③中少量②的操作是
(5)⑦中含有的化学键为
(6)⑨在水溶液中的电离方程式为
Ⅱ.写出下列反应的离子方程式(已知还原性:
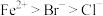 ):
):(7)向
 溶液中通入少量
溶液中通入少量 (
( 与
与 的微粒数的比值
的微粒数的比值 )
)(8)向
 溶液中通入
溶液中通入 ,
, 与
与 的化学计量数之比为1∶l∶
的化学计量数之比为1∶l∶
您最近一年使用:0次
名校
4 . 按要求书写方程式
(1)过氧化钠与水反应:___________ 。
(2)将 改写为对应的化学方程式
改写为对应的化学方程式___________ 。
(3)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的 ,配平该反应的离子方程式:
,配平该反应的离子方程式:___________ 。

(1)过氧化钠与水反应:
(2)将
 改写为对应的化学方程式
改写为对应的化学方程式(3)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的
 ,配平该反应的离子方程式:
,配平该反应的离子方程式:
您最近一年使用:0次
名校
5 . 按要求完成下列式子
Ⅰ.请书写下列反应的离子方程式。
(1)氢氧化铁溶于氢碘酸中___________
(2)酸性高锰酸钾溶液与草酸溶液混合___________
(3)等体积等物质的量浓度的 溶液与
溶液与 溶液混合:
溶液混合:___________
(4)用过氧化氢从酸化的海带灰浸出液中提取碘___________
Ⅱ.配平下列方程式
(5) ____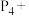 ____
____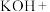 ____
____ ____
____ ____
____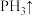
______________________
(6) ____ ____
____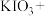 ____
____ _____
_____ _____
_____ _____
_____
______________________
(7) ____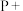 _____
_____ _____
_____ _____
_____ _____
_____ ____
____
______________________
(8)_____ _____
_____ _____
_____ _____
_____ _____
_____ _____
_____
______________________
Ⅰ.请书写下列反应的离子方程式。
(1)氢氧化铁溶于氢碘酸中
(2)酸性高锰酸钾溶液与草酸溶液混合
(3)等体积等物质的量浓度的
 溶液与
溶液与 溶液混合:
溶液混合:(4)用过氧化氢从酸化的海带灰浸出液中提取碘
Ⅱ.配平下列方程式
(5) ____
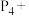 ____
____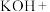 ____
____ ____
____ ____
____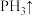
(6) ____
 ____
____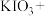 ____
____ _____
_____ _____
_____ _____
_____
(7) ____
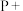 _____
_____ _____
_____ _____
_____ _____
_____ ____
____
(8)_____
 _____
_____ _____
_____ _____
_____ _____
_____ _____
_____
您最近一年使用:0次
解题方法
6 . 请回答下列问题:已知2KMnO4+16HCl(浓)=2KCl+2MnCl2+8H2O+5Cl2↑
(1)上述反应中被氧化的元素是___________ ;还原产物是___________ 。
(2)氧化剂与还原剂的个数比是___________ 。
(3)用单线桥标明该反应电子转移方向和数目:___________ 。
(4)配平反应方程式:
①_____FeS2 + ____O2 =_____ Fe2O3 + _____SO2____________________
②_____Al+____NaNO3+___H2O=______Al(OH)3+_____N2↑+______NaAlO2____________________
(1)上述反应中被氧化的元素是
(2)氧化剂与还原剂的个数比是
(3)用单线桥标明该反应电子转移方向和数目:
(4)配平反应方程式:
①_____FeS2 + ____O2 =_____ Fe2O3 + _____SO2
②_____Al+____NaNO3+___H2O=______Al(OH)3+_____N2↑+______NaAlO2
您最近一年使用:0次
解题方法
7 . 用化学知识回答下列问题。
I.实验室配制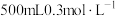 的
的 溶液。
溶液。
(1)需称量 固体
固体__________ g。
(2)在该溶液的配制过程中,用到的玻璃仪器有:量筒、烧杯、玻璃棒、__________ 。
(3)如果在定容时仰视,则溶液浓度__________ 。(填“偏大”、“偏小”或“无影响”)
II.根据元素化合物相关知识填空。
(4) 中阳离子与阴离子个数比
中阳离子与阴离子个数比__________ ,检验其组成中所含阳离子的方法是__________ 。
(5)在潜水艇和消防员的呼吸面具中, 所发生反应的化学方程式为
所发生反应的化学方程式为__________ ,从氧化剂和还原剂的角度分析,在这个反应中 的作用是
的作用是__________ 。
(6) 的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。实验室盛放氢氧化钠溶液的试剂瓶应使用橡胶塞,而不用玻璃塞。请用反应的化学方程式解释原因
的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。实验室盛放氢氧化钠溶液的试剂瓶应使用橡胶塞,而不用玻璃塞。请用反应的化学方程式解释原因__________ 。
(7)科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:(已知 为
为 和
和 混合物)
混合物)

回答下列问题:
①从物质分类的角度看,图中的物质属于酸性氧化物的有__________ (填化学式)。
②图中物质溶于水所得溶液呈碱性的是__________ (填化学式)。
③写出 与
与 反应生成
反应生成 的化学方程式:
的化学方程式:__________ 。
④氨气与一氧化氮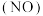 在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为
在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为__________ 。
I.实验室配制
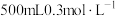 的
的 溶液。
溶液。(1)需称量
 固体
固体(2)在该溶液的配制过程中,用到的玻璃仪器有:量筒、烧杯、玻璃棒、
(3)如果在定容时仰视,则溶液浓度
II.根据元素化合物相关知识填空。
(4)
 中阳离子与阴离子个数比
中阳离子与阴离子个数比(5)在潜水艇和消防员的呼吸面具中,
 所发生反应的化学方程式为
所发生反应的化学方程式为 的作用是
的作用是(6)
 的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。实验室盛放氢氧化钠溶液的试剂瓶应使用橡胶塞,而不用玻璃塞。请用反应的化学方程式解释原因
的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。实验室盛放氢氧化钠溶液的试剂瓶应使用橡胶塞,而不用玻璃塞。请用反应的化学方程式解释原因(7)科学家研究发现含氮化合物和含硫化合物在形成雾霾时与大气中的氨有关,转化关系如图所示:(已知
 为
为 和
和 混合物)
混合物)
回答下列问题:
①从物质分类的角度看,图中的物质属于酸性氧化物的有
②图中物质溶于水所得溶液呈碱性的是
③写出
 与
与 反应生成
反应生成 的化学方程式:
的化学方程式:④氨气与一氧化氮
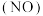 在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为
在一定条件下反应可生成对空气无污染的物质,该反应的化学方程式为
您最近一年使用:0次
名校
解题方法
8 . 铁器时代是人类发展史中⼀个极为重要的时代,铁及其化合物在人类的生产、生活中都起了巨大的作用。
(1)长期放置的 溶液易被氧化而变质,实验室⽤绿矾
溶液易被氧化而变质,实验室⽤绿矾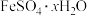 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入________ ,其原因是______________________ (用离子方程式表示)。
(2)利用部分变质的 溶液制备
溶液制备 :
:
部分变质的 溶液
溶液 溶液I
溶液I 沉淀II
沉淀II

① 溶液作用的离子方程式为
溶液作用的离子方程式为_____________________________________ 。
②写出由“溶液I”到“沉淀II”反应的离子方程式:_______________________________ 。
(3)电子工业中,常用 溶液腐蚀铜,其反应的离子方程式为
溶液腐蚀铜,其反应的离子方程式为________________________ 。
(1)长期放置的
 溶液易被氧化而变质,实验室⽤绿矾
溶液易被氧化而变质,实验室⽤绿矾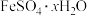 配制
配制 溶液时为了防止
溶液时为了防止 溶液变质,经常向其中加入
溶液变质,经常向其中加入(2)利用部分变质的
 溶液制备
溶液制备 :
:部分变质的
 溶液
溶液 溶液I
溶液I 沉淀II
沉淀II

①
 溶液作用的离子方程式为
溶液作用的离子方程式为②写出由“溶液I”到“沉淀II”反应的离子方程式:
(3)电子工业中,常用
 溶液腐蚀铜,其反应的离子方程式为
溶液腐蚀铜,其反应的离子方程式为
您最近一年使用:0次
解题方法
9 . 按要求完成下列问题。
(1)硒(Se)是人体必需的微量元素,与O为同一主族元素,Se原子比O原子多两个电子层,则Se的原子序数为____ ,其最高价氧化物对应的水化物化学式为____ 。
(2)X射线衍射法可以测定某些分子结构,NH3分子结构为_____ 。
(3)水在液态时,几个水分子可以形成缔合水分子(H2O)n的原因是水分子之间存在____ 。
(4)漂白粉(有效成分Ca(ClO)2)与空气中CO2和水蒸气反应的化学方程式:____ 。
(5)完成氧化还原反应的离子方程式:____ 。
Cr2O +Fe2++_____=Cr3++Fe3++____
+Fe2++_____=Cr3++Fe3++____
(6)一定条件下金属钠和H2反应生成甲,甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。化合物甲和NaAlH4都是重要的还原剂。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。
①甲的化学式____ 。
②甲与AlCl3反应得到NaAlH4的化学方程式:____ 。
③NaAlH4与水发生氧化还原反应的化学方程式:____ 。
④甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式:____ 。
(1)硒(Se)是人体必需的微量元素,与O为同一主族元素,Se原子比O原子多两个电子层,则Se的原子序数为
(2)X射线衍射法可以测定某些分子结构,NH3分子结构为
(3)水在液态时,几个水分子可以形成缔合水分子(H2O)n的原因是水分子之间存在
(4)漂白粉(有效成分Ca(ClO)2)与空气中CO2和水蒸气反应的化学方程式:
(5)完成氧化还原反应的离子方程式:
Cr2O
 +Fe2++_____=Cr3++Fe3++____
+Fe2++_____=Cr3++Fe3++____(6)一定条件下金属钠和H2反应生成甲,甲与水反应可产生H2,甲与AlCl3反应可得到NaAlH4。化合物甲和NaAlH4都是重要的还原剂。将4.80g甲加热至完全分解,得到金属钠和2.24L(已折算成标准状况)的H2。
①甲的化学式
②甲与AlCl3反应得到NaAlH4的化学方程式:
③NaAlH4与水发生氧化还原反应的化学方程式:
④甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程发生反应的化学方程式:
您最近一年使用:0次
2022-11-16更新
|
159次组卷
|
2卷引用:天津市部分区2022-2023学年高三上学期期中考试化学试题
名校
10 . 按要求回答下列问题:
Ⅰ.现有以下物质:①氮气 ②液 ③氯化氢气体 ④铜片 ⑤硫酸钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔化的
③氯化氢气体 ④铜片 ⑤硫酸钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔化的 ⑨
⑨ 溶液,请回答下列问题:
溶液,请回答下列问题:
(1)以上物质中能导电的是_______ (填序号,下同)
(2)以上物质中属于电解质的是_______ 。
(3)写出上述物质中⑨的电离方程式:_______ 。
Ⅱ.有下列6种物质: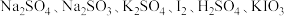 组成一个氧化还原反应。
组成一个氧化还原反应。
(4)将除 的5种物质分别填入下面对应的横线上,组成化学方程式并配平:
的5种物质分别填入下面对应的横线上,组成化学方程式并配平:_______ 。
 。
。
(5)在该反应中,还原剂是_______ (填化学式,下同),还原产物是_______ 。
Ⅲ.是“84”消毒液的有效成分,请回答下列问题:
(6) 中
中 元素的化合价是
元素的化合价是_______ 价,曾有报道,在清洗卫生间时,因混合使用“洁厕灵”(主要成分是稀盐酸)与“84”消毒液而发生氯气中毒事件。用离子方程式表示原因:_______ 。
Ⅰ.现有以下物质:①氮气 ②液
 ③氯化氢气体 ④铜片 ⑤硫酸钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔化的
③氯化氢气体 ④铜片 ⑤硫酸钡晶体 ⑥蔗糖 ⑦酒精 ⑧熔化的 ⑨
⑨ 溶液,请回答下列问题:
溶液,请回答下列问题:(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)写出上述物质中⑨的电离方程式:
Ⅱ.有下列6种物质:
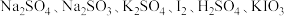 组成一个氧化还原反应。
组成一个氧化还原反应。(4)将除
 的5种物质分别填入下面对应的横线上,组成化学方程式并配平:
的5种物质分别填入下面对应的横线上,组成化学方程式并配平: 。
。(5)在该反应中,还原剂是
Ⅲ.是“84”消毒液的有效成分,请回答下列问题:
(6)
 中
中 元素的化合价是
元素的化合价是
您最近一年使用:0次



