20-21高二下·河北石家庄·期中
名校
解题方法
1 . 李克强总理在十二届全国人大五次会议上作政府工作报告时强调:坚决打好蓝天保卫战。今年二氧化硫、氮氧化物排放量要分别下降3%,重点地区细颗粒物(PM2.5)浓度明显下降。其中二氧化硫、氮氧化物等的排放与工业燃烧煤、石油等化石燃料有很大的关系,所以对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
Ⅰ.脱硝:催化剂存在下,H2还原NO2生成水蒸气和另一种无毒气体的化学方程式为___________
Ⅱ.脱碳:一定条件下CO2会和H2反应合成CH3OH。方程式为: CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。现向2 L恒容密闭容器中加入2 mol CO2、6 mol H2,在恒温下发生反应。10 s后反应达到平衡,此时容器内CH3OH的浓度为0.5 mol·L-1,请回答以下问题:
(1)前10 s内的平均反应速率v(H2O)=___________ ;平衡时CO2的转化率为___________ 。
(2)下列叙述能说明原反应达到平衡状态的是___________ 。
a.单位时间内消耗n mol CH3OH的同时生成n mol CO2
b.1 mol CO2生成的同时有3 mol H-H键断裂
c.CO2和H2的浓度保持不变
d.容器内压强保持不变
e.CO2和H2的物质的量之比保持不变
Ⅲ.脱硫:燃煤的烟气脱硫技术是当前应用最广、效率最高的脱硫技术。其更多的是利用碱溶液与烟道气相遇,烟道气中SO2溶解在水中,形成一种稀酸溶液,然后与Ca(OH)2浊液等发生中和反应。
(1)已知中和反应为常见的放热反应,下列有关反应放热、吸热的说法正确的是___________
a.可燃物燃烧一般都需要加热,所以都是吸热反应
b.化学键的断裂要吸收能量
c.当反应物的总能量低于生成物的总能量时,据能量守恒定律可知反应会放热
d.已知SO2(g)与O2(g)反应生成SO3(g)为放热反应,则SO3(g)分解生成SO2(g)与O2(g)的反应为吸热反应
(2)请写出脱硫过程发生的主要化学方程式:___________ 。
Ⅰ.脱硝:催化剂存在下,H2还原NO2生成水蒸气和另一种无毒气体的化学方程式为
Ⅱ.脱碳:一定条件下CO2会和H2反应合成CH3OH。方程式为: CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)。现向2 L恒容密闭容器中加入2 mol CO2、6 mol H2,在恒温下发生反应。10 s后反应达到平衡,此时容器内CH3OH的浓度为0.5 mol·L-1,请回答以下问题:
(1)前10 s内的平均反应速率v(H2O)=
(2)下列叙述能说明原反应达到平衡状态的是
a.单位时间内消耗n mol CH3OH的同时生成n mol CO2
b.1 mol CO2生成的同时有3 mol H-H键断裂
c.CO2和H2的浓度保持不变
d.容器内压强保持不变
e.CO2和H2的物质的量之比保持不变
Ⅲ.脱硫:燃煤的烟气脱硫技术是当前应用最广、效率最高的脱硫技术。其更多的是利用碱溶液与烟道气相遇,烟道气中SO2溶解在水中,形成一种稀酸溶液,然后与Ca(OH)2浊液等发生中和反应。
(1)已知中和反应为常见的放热反应,下列有关反应放热、吸热的说法正确的是
a.可燃物燃烧一般都需要加热,所以都是吸热反应
b.化学键的断裂要吸收能量
c.当反应物的总能量低于生成物的总能量时,据能量守恒定律可知反应会放热
d.已知SO2(g)与O2(g)反应生成SO3(g)为放热反应,则SO3(g)分解生成SO2(g)与O2(g)的反应为吸热反应
(2)请写出脱硫过程发生的主要化学方程式:
您最近一年使用:0次
2021-05-19更新
|
970次组卷
|
8卷引用:2.2.1 化学平衡状态(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
(已下线)2.2.1 化学平衡状态(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)河北省辛集中学2020-2021学年高二下学期期中考试化学试题河北省辛集中学2020-2021学年高一下学期期中考试化学试题江苏省海安市南莫中学2021-2022学年高二上学期第一次月考备考金卷B卷化学试题(已下线)第2章 化学反应速率和化学平衡(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)海南省儋州川绵中学2021-2022学年高二上学期第二次月考化学试题河南省南乐县第一高级中学2021-2022学年高二上学期9月半月考化学试题河南省商丘市宁陵县高级中学2023-2024学年高二上学期第一次考试化学试题
2 . 美国计划2028年再次登陆月球,并在月球上建立永久性基地,为人类登陆新的行星做好前期准备。为了解决基地人员的供氧问题,科学家设想利用月球富氧岩石制取氧气。其提氧原理是:用氢气还原富氧岩石获取水,再利用太阳能电池电解水得到氢气和氧气。
玄武岩(含钛铁矿)是月球的主要岩石之一,其质地坚硬,钛铁矿的主要成分为钛酸亚铁(FeTiO3)。用上述提氧原理,理论上,从1kgFeTiO3中可获取约105.3gO2。
(1)写出FeTiO3与H2反应的化学方程式:___ 。
(2)研究表明,月球上平均直径为40微米的小圆珠形成的堆积物(富含Fe2TiO4)是最适合提氧的矿物。这种堆积物作为提氧原料的优点是___ 。
(3)研究人员查阅文献后,得知钛铁矿在高温下还能被炭粉还原:2FeTiO3+C 2Fe+2TiO2+CO2↑,通过植物的光合作用可吸收CO2获得O2。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
2Fe+2TiO2+CO2↑,通过植物的光合作用可吸收CO2获得O2。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
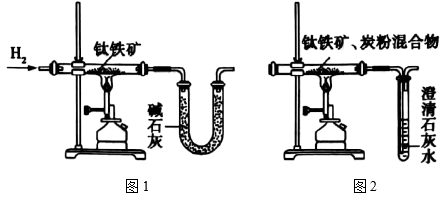
研究人员用图1装置从钛铁矿中提取氧,实验中得出的可提取氧的质量分数大于理论值,产生这种情况的原因可能是___ ;用图2装置进行实验的过程中,称得反应前钛铁矿的质量为m1g,炭粉的质量为m2g,钛铁矿完全反应后,测得生成CaCO3的质量为m3g,则钛铁矿中可提取氧的质量分数表达式为___ 。
(4)在钛铁矿提氧过程中科学家们常选用H2而不用其他还原剂,其主要原因是__ 。
玄武岩(含钛铁矿)是月球的主要岩石之一,其质地坚硬,钛铁矿的主要成分为钛酸亚铁(FeTiO3)。用上述提氧原理,理论上,从1kgFeTiO3中可获取约105.3gO2。
(1)写出FeTiO3与H2反应的化学方程式:
(2)研究表明,月球上平均直径为40微米的小圆珠形成的堆积物(富含Fe2TiO4)是最适合提氧的矿物。这种堆积物作为提氧原料的优点是
(3)研究人员查阅文献后,得知钛铁矿在高温下还能被炭粉还原:2FeTiO3+C
 2Fe+2TiO2+CO2↑,通过植物的光合作用可吸收CO2获得O2。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
2Fe+2TiO2+CO2↑,通过植物的光合作用可吸收CO2获得O2。他们设计了两套实验装置来测定钛铁矿中可提取氧的质量分数。
研究人员用图1装置从钛铁矿中提取氧,实验中得出的可提取氧的质量分数大于理论值,产生这种情况的原因可能是
(4)在钛铁矿提氧过程中科学家们常选用H2而不用其他还原剂,其主要原因是
您最近一年使用:0次
解题方法
3 . 某硫酸工厂的酸性废水中砷(As)元素含量极高,为控制砷的排放,可采用化学沉降法处理含砷废水,相关数据如下表。请回答以下问题:
表1几种盐的Ksp
表2工厂污染物排放浓度及允许排放标准
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=___ mol•L-1。
(2)若酸性废水中Fe3+的浓度为1.0×10-4mol•L-1,则c(AsO )=
)=___ mol•L-1。
(3)工厂排放出的酸性废水中的三价砷(弱酸H3AsO3)不易沉降,可投入MnO2先将其氧化成五价砷(弱酸H3AsO4),此时MnO2被还原为Mn2+,该反应的离子方程式为____ 。
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右,使五价砷以Ca3(AsO4)2的形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为____ 。
②Ca3(AsO4)2在pH调节到8左右才开始沉淀,原因为__ 。
③砷酸(H3AsO4)分步电离的平衡常数(25℃)为Ka1=5.6×10-3,Ka2=1.7×10-7,Ka3=4.0×10-12,第三步电离的平衡常数表达式为Ka3=____ ,Na3AsO4第一步水解的离子方程式为AsO +H2O
+H2O HAsO
HAsO +OH-,该步水解的平衡常数(25℃)为
+OH-,该步水解的平衡常数(25℃)为___ 。
表1几种盐的Ksp
| 难溶物 | Ksp |
| Ca3(AsO4)2 | 6.8×10-19 |
| CaSO4 | 4.9×10-5 |
| FeAsO4 | 5.7×10-21 |
表2工厂污染物排放浓度及允许排放标准
| 污染物 | H2SO4 | As |
| 废水浓度 | 29.4g•L-1 | 1.6g•L-1 |
| 排放标准 | pH=6~9 | 0.5mg•L-1 |
(1)该硫酸工厂排放的废水中硫酸的物质的量浓度c(H2SO4)=
(2)若酸性废水中Fe3+的浓度为1.0×10-4mol•L-1,则c(AsO
 )=
)=(3)工厂排放出的酸性废水中的三价砷(弱酸H3AsO3)不易沉降,可投入MnO2先将其氧化成五价砷(弱酸H3AsO4),此时MnO2被还原为Mn2+,该反应的离子方程式为
(4)在处理含砷废水时采用分段式,先向废水中投入生石灰调节pH到2,再投入生石灰将pH调节到8左右,使五价砷以Ca3(AsO4)2的形式沉降。
①将pH调节到2时废水中有大量沉淀产生,沉淀主要成分的化学式为
②Ca3(AsO4)2在pH调节到8左右才开始沉淀,原因为
③砷酸(H3AsO4)分步电离的平衡常数(25℃)为Ka1=5.6×10-3,Ka2=1.7×10-7,Ka3=4.0×10-12,第三步电离的平衡常数表达式为Ka3=
 +H2O
+H2O HAsO
HAsO +OH-,该步水解的平衡常数(25℃)为
+OH-,该步水解的平衡常数(25℃)为
您最近一年使用:0次
2020-10-14更新
|
263次组卷
|
3卷引用:人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡
人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡选择性必修1(SJ)专题3第四单元 沉淀溶解平衡(已下线)3.4.2 沉淀溶解平衡的应用(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)
4 .  在实验、医疗、化工等方面有广泛的应用。
在实验、医疗、化工等方面有广泛的应用。
(1) 中O的化合价为
中O的化合价为__________ ,具有__________ (填“氧化性”“还原性”或“氧化性和还原性”)。
(2)酸性高锰酸钾溶液可与 反应,其化学方程式是
反应,其化学方程式是
 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。
①X的化学式是___________ 。
②用双线桥法标出,上述反应中电子转移的方向和数目________ 。
③上述反应中的还原剂为_________ (填化学式),被还原的元素是__________ (填元素符号)。
④高锰酸钾溶液呈________ 色,向酸性 溶液中滴入双氧水,观察到的现象是
溶液中滴入双氧水,观察到的现象是_________ ,反应后溶液的pH________ (填“增大”“减小”或“不变”)。
⑤0.2mol 参加上述反应,转移电子
参加上述反应,转移电子_______ mol。
 在实验、医疗、化工等方面有广泛的应用。
在实验、医疗、化工等方面有广泛的应用。(1)
 中O的化合价为
中O的化合价为(2)酸性高锰酸钾溶液可与
 反应,其化学方程式是
反应,其化学方程式是
 。已知:稀
。已知:稀 溶液几乎无色。
溶液几乎无色。①X的化学式是
②用双线桥法标出,上述反应中电子转移的方向和数目
③上述反应中的还原剂为
④高锰酸钾溶液呈
 溶液中滴入双氧水,观察到的现象是
溶液中滴入双氧水,观察到的现象是⑤0.2mol
 参加上述反应,转移电子
参加上述反应,转移电子
您最近一年使用:0次
5 . ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室可通过以下反应制得:
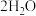 ,试回答下列问题。
,试回答下列问题。
(1)该反应中还原产物的化学式是_________ ,被氧化的元素是________ (填元素符号)。
(2)用双线桥标出上述反应的电子转移情况______ 。
(3)若反应共产生了8.96 L(标准状况)气体,则反应转移的电子的物质的量为________ mol,消耗还原剂的物质的量为________ mol。
(4)标准状况下44.8 mL的ClO2恰好能与50 mL 0.1 mol/L的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为_________ ,此过程说明ClO2具有________ (填“氧化”或“还原”)性。
(5)在硫化钠溶液中通入ClO2可发生如下反应,请将生成物补充完整并配平。
________ ClO2+________ 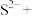
________ H2O=________ Cl-+________ 
________

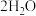 ,试回答下列问题。
,试回答下列问题。(1)该反应中还原产物的化学式是
(2)用双线桥标出上述反应的电子转移情况
(3)若反应共产生了8.96 L(标准状况)气体,则反应转移的电子的物质的量为
(4)标准状况下44.8 mL的ClO2恰好能与50 mL 0.1 mol/L的Na2SO3溶液完全反应,得到的产物之一为Na2SO4,氯元素在产物中的化合价为
(5)在硫化钠溶液中通入ClO2可发生如下反应,请将生成物补充完整并配平。
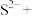

您最近一年使用:0次
解题方法
6 . 甲醇既是基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的两个反应:
反应I:
反应Ⅱ:
上述反应符合“原子经济”原则的是_______ (填“I”或“Ⅱ”)。
(2)已知在常温常压下:
①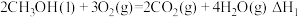
②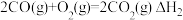
③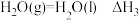
则反应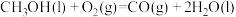 的
的
_____ 。
(3)现以甲醇燃料电池,用电解法来处理酸性含铬废水(主要含有 ),实验室利用如图装置模拟该方法:
),实验室利用如图装置模拟该方法:
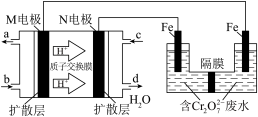
①N电极的电极反应式为_________ 。
②请完成电解池中 转化为
转化为 的离子方程式:
的离子方程式:______
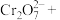 ______
______ ________[ ]=________
________[ ]=________ _____
_____ ___[ ]
___[ ]
(1)以下是工业上合成甲醇的两个反应:
反应I:

反应Ⅱ:

上述反应符合“原子经济”原则的是
(2)已知在常温常压下:
①
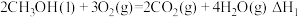
②
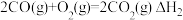
③
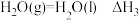
则反应
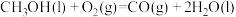 的
的
(3)现以甲醇燃料电池,用电解法来处理酸性含铬废水(主要含有
 ),实验室利用如图装置模拟该方法:
),实验室利用如图装置模拟该方法:
①N电极的电极反应式为
②请完成电解池中
 转化为
转化为 的离子方程式:
的离子方程式: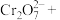 ______
______ ________[ ]=________
________[ ]=________ _____
_____ ___[ ]
___[ ]
您最近一年使用:0次
名校
7 . 三氯氧磷(POCl3)广泛用于农药、医药等生产。工业制备三氯氧磷的过程中会产生副产品亚磷酸(H3PO3)。回答下列问题:
(1)三氯氧磷可由三氯化磷、水、氯气加热反应生成,反应的化学方程式为_______
(2)已知亚磷酸(H3PO3)为二元弱酸,则Na2HPO3溶液中,各离子浓度的大小关系为_______
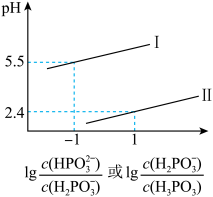
(3)常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示lg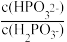 的是曲线
的是曲线_____ (填“Ⅰ”或“Ⅱ”),亚磷酸(H3PO3)的Ka1=_____ ,反应HPO32-+H2O H2PO3-+OH-的平衡常数的值是
H2PO3-+OH-的平衡常数的值是_____ 。
(4)工业上生产三氯氧磷的同时会产生含磷废水(主要成分为H3PO4、H3PO3)。向废水中先加入适量漂白粉,再加入生石灰调节pH,将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中c(Ca2+)=5×10-6 mol·L-1,则溶液中c(PO43-)=_____ mol·L-1。(已知Ksp[Ca3(PO4)2]=2×10-29)
(1)三氯氧磷可由三氯化磷、水、氯气加热反应生成,反应的化学方程式为
(2)已知亚磷酸(H3PO3)为二元弱酸,则Na2HPO3溶液中,各离子浓度的大小关系为
(3)常温下,将NaOH溶液滴加到亚磷酸(H3PO3)溶液中,混合溶液的pH与离子浓度变化的关系如图所示,则表示lg
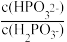 的是曲线
的是曲线 H2PO3-+OH-的平衡常数的值是
H2PO3-+OH-的平衡常数的值是
(4)工业上生产三氯氧磷的同时会产生含磷废水(主要成分为H3PO4、H3PO3)。向废水中先加入适量漂白粉,再加入生石灰调节pH,将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中c(Ca2+)=5×10-6 mol·L-1,则溶液中c(PO43-)=

您最近一年使用:0次
2020-04-03更新
|
791次组卷
|
4卷引用:人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 过综合 章末素养综合检测
8 . N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为________ 。
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2OH− 2
2 +H2O
+H2O
2NO2+2OH−
 +
+ +H2O
+H2O
①下列措施能提高尾气中NO和NO2去除率的有________ (填字母)。
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是________ (填化学式);吸收后排放的尾气中含量较高的氮氧化物是________ (填化学式)。
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
①在酸性NaClO溶液中,HClO氧化NO生成Cl−和 ,其离子方程式为
,其离子方程式为________ 。
②NaClO溶液的初始pH越小,NO转化率越高。其原因是________ 。

(1)N2O的处理。N2O是硝酸生产中氨催化氧化的副产物,用特种催化剂能使N2O分解。NH3与O2在加热和催化剂作用下生成N2O的化学方程式为
(2)NO和NO2的处理。已除去N2O的硝酸尾气可用NaOH溶液吸收,主要反应为
NO+NO2+2OH−
 2
2 +H2O
+H2O2NO2+2OH−

 +
+ +H2O
+H2O①下列措施能提高尾气中NO和NO2去除率的有
A.加快通入尾气的速率
B.采用气、液逆流的方式吸收尾气
C.吸收尾气过程中定期补加适量NaOH溶液
②吸收后的溶液经浓缩、结晶、过滤,得到NaNO2晶体,该晶体中的主要杂质是
(3)NO的氧化吸收。用NaClO溶液吸收硝酸尾气,可提高尾气中NO的去除率。其他条件相同,NO转化为
 的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。
的转化率随NaClO溶液初始pH(用稀盐酸调节)的变化如图所示。①在酸性NaClO溶液中,HClO氧化NO生成Cl−和
 ,其离子方程式为
,其离子方程式为②NaClO溶液的初始pH越小,NO转化率越高。其原因是

您最近一年使用:0次
2019-06-10更新
|
7390次组卷
|
32卷引用:2019-2020学年新人教版必修2第5章第2节《氮及其化合物》作业
2019-2020学年新人教版必修2第5章第2节《氮及其化合物》作业鲁科版(2019)高一必修第一册第三章C 高考挑战区 过高考 3年真题强化闯关专题7 第三单元综合拔高练-高中化学必修第二册苏教版2019人教版2019必修第二册 第五章 第二~三节综合拔高练2019年江苏省高考化学试题湖南省长沙市第一中学2020届高三第一次月考化学试题河北省邯郸市2019-2020学年高三上学期期中考试化学试题2020届高三化学二轮冲刺新题专练——氮及其氧化物的性质(提升练)专题3.2 非金属及其化合物(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升专题1.3 氧化还原反应(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升第2章 化学键化学反应规律 模拟高考——C挑战区 夯实基础(鲁科版(2019)第二册)第2章 化学键 化学反应与能量 模拟高考——C挑战区 夯实基础(鲁科版必修2)专题4 化学科学与人类文明——C挑战区 模拟高考(苏教版必修2)江苏省苏州新草桥中学2020届高三上学期10月月考化学试题(已下线)2020年高考化学押题预测卷01(新课标Ⅰ卷)--《2020年高考押题预测卷》(已下线)专题6.3 化学原理题(必考)(疑难突破)——巅峰冲刺2020年高考化学二轮专项提升江苏省扬州市江都区大桥高级中学2019-2020学年高二下学期期中考试化学试题江苏省启东中学2021届高三上学期期初考试化学试题江苏省苏州市工业园区星海实验中学高一下学期3月月考化学试题(已下线)【苏州新东方】04 吴县中学重庆市凤鸣山中学2020-2021学年高一下学期期中考试化学试题湖北省广水市普通中学2020-2021学年高一下学期5月月考化学试题(已下线)第12讲 氮及其化合物(练) — 2022年高考化学一轮复习讲练测(新教材新高考)广东省潮州市饶平县第二中学2021-2022学年高一下学期月考(一)化学试题海南省海南枫叶国际学校2021-2022学年高三上学期第三次月考(1月)化学试题黑龙江省大庆市第四中学2018-2019学年高二下学期第三次月考化学试题(已下线)专题17 原理综合题(已下线)常见无机物的性质江苏省镇江市句容市南京人民中学等三市四校联考2022-2023学年高一下学期4月月考化学试题湖北省黄石市第二中学2023-2024学年高二上学期第三次统测化学试题江苏省常州市联盟校2023-2024学年高一下学期3月阶段调研化学试题江苏省南京市金陵中学2023-2024学年高一下学期3月月考化学试题
解题方法
9 . 大气污染问题日益引起全民关注.
(1)PM2.5是指大气中直径小于或等于2.5μm(1μm=103nm)的颗粒物.下列说法不正确的是______ (填字母序号)。
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1~2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(2)某地科研工作者用五年时间研究出利用石灰乳除工业燃煤尾气中的硫(SO2、SO3)和氮(NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4和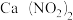
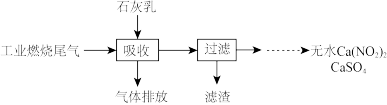
①硫酸型酸雨的形成过程是大气中的SO2溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为___________ 、__________ .
②CaSO4可以调节水泥的硬化时间.尾气中2molSO2被石灰乳逐渐吸收最终生成了1molCaSO4,该过程中转移的电子数目为___________ 。
③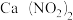 可制成混凝土防冻剂、钢筋阻锈剂等。尾气中NO、NO2与石灰乳反应生成
可制成混凝土防冻剂、钢筋阻锈剂等。尾气中NO、NO2与石灰乳反应生成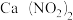 的化学方程式
的化学方程式_________________ .
(3)人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如下:
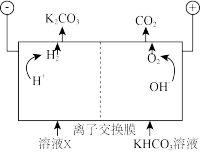
①在阳极区发生的反应包括___________ 和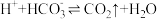 。
。
②简述 在阴极区再生的原理
在阴极区再生的原理___________ 。
③再生装置中产生的CO2和H2在一定条件下反应生成甲醇,工业上利用该反应合成甲醇。
已知:25℃,101KPa下:
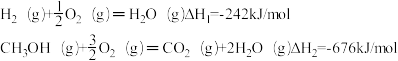
写出CO2和H2生成气态甲醇等产物的热化学方程式____________ .
(1)PM2.5是指大气中直径小于或等于2.5μm(1μm=103nm)的颗粒物.下列说法不正确的是
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1~2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(2)某地科研工作者用五年时间研究出利用石灰乳除工业燃煤尾气中的硫(SO2、SO3)和氮(NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4和
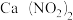

①硫酸型酸雨的形成过程是大气中的SO2溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为
②CaSO4可以调节水泥的硬化时间.尾气中2molSO2被石灰乳逐渐吸收最终生成了1molCaSO4,该过程中转移的电子数目为
③
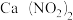 可制成混凝土防冻剂、钢筋阻锈剂等。尾气中NO、NO2与石灰乳反应生成
可制成混凝土防冻剂、钢筋阻锈剂等。尾气中NO、NO2与石灰乳反应生成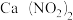 的化学方程式
的化学方程式(3)人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如下:

①在阳极区发生的反应包括
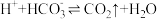 。
。②简述
 在阴极区再生的原理
在阴极区再生的原理③再生装置中产生的CO2和H2在一定条件下反应生成甲醇,工业上利用该反应合成甲醇。
已知:25℃,101KPa下:
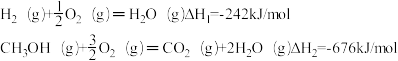
写出CO2和H2生成气态甲醇等产物的热化学方程式
您最近一年使用:0次
2016-12-09更新
|
843次组卷
|
4卷引用:苏教版2017届高三单元精练检测六化学试题
名校
解题方法
10 . 请回答下列问题
(1)向H2O2溶液中滴加FeCl3溶液,可发生下列反应:H2O2+2Fe3+=2Fe2++ O2↑+2H+, H2O2+ 2Fe2++2H+=2Fe3++ 2H2O 。在以上反应中Fe3+实际上起着___________ 作用,总反应式为___________ 。
(2)I2与Fe3+一样也可以发生上述类似反应,类比(1)在下面填入合适的化学反应方程式:H2O2+I2=2HIO,___________ 。总反应式为___________ 。
(3)在硫酸和KI的混合溶液中加入足量的H2O2,放出大量的无色气体,溶液呈棕色,并可使淀粉变蓝色。该反应的离子方程式为:___________ 。
(4)高铁酸钠(Na2FeO4)可作为一种新型净水剂,在反应中Na2FeO4被还原为Fe3+离子,请简述高铁酸钠之所以能净水,除了具有强氧化性,能消毒杀菌外,另一原因是___________ 。
(5)高铁酸钠的制备常用氧化铁在碱性溶液中与硝酸钠反应制得:Fe2O3 + NaNO3 + NaOH → Na2FeO4 + NaNO2 + H2O,配平化学方程式,并标出电子转移的方向和数目___________ 。
(1)向H2O2溶液中滴加FeCl3溶液,可发生下列反应:H2O2+2Fe3+=2Fe2++ O2↑+2H+, H2O2+ 2Fe2++2H+=2Fe3++ 2H2O 。在以上反应中Fe3+实际上起着
(2)I2与Fe3+一样也可以发生上述类似反应,类比(1)在下面填入合适的化学反应方程式:H2O2+I2=2HIO,
(3)在硫酸和KI的混合溶液中加入足量的H2O2,放出大量的无色气体,溶液呈棕色,并可使淀粉变蓝色。该反应的离子方程式为:
(4)高铁酸钠(Na2FeO4)可作为一种新型净水剂,在反应中Na2FeO4被还原为Fe3+离子,请简述高铁酸钠之所以能净水,除了具有强氧化性,能消毒杀菌外,另一原因是
(5)高铁酸钠的制备常用氧化铁在碱性溶液中与硝酸钠反应制得:Fe2O3 + NaNO3 + NaOH → Na2FeO4 + NaNO2 + H2O,配平化学方程式,并标出电子转移的方向和数目
您最近一年使用:0次



