1 . 高铁酸钠 具有强氧化性(其中具有强氧化性的是
具有强氧化性(其中具有强氧化性的是 ),高铁酸钠是一种高效水处理剂,工业制备高铁酸钠的离子方程式为
),高铁酸钠是一种高效水处理剂,工业制备高铁酸钠的离子方程式为 (未配平)。高铁酸钠处理水时,除杀菌消毒外,生成的氢氧化铁胶体还可净化水。下列有关说法正确的是
(未配平)。高铁酸钠处理水时,除杀菌消毒外,生成的氢氧化铁胶体还可净化水。下列有关说法正确的是
 具有强氧化性(其中具有强氧化性的是
具有强氧化性(其中具有强氧化性的是 ),高铁酸钠是一种高效水处理剂,工业制备高铁酸钠的离子方程式为
),高铁酸钠是一种高效水处理剂,工业制备高铁酸钠的离子方程式为 (未配平)。高铁酸钠处理水时,除杀菌消毒外,生成的氢氧化铁胶体还可净化水。下列有关说法正确的是
(未配平)。高铁酸钠处理水时,除杀菌消毒外,生成的氢氧化铁胶体还可净化水。下列有关说法正确的是A.工业制备高铁酸钠反应中氧化剂和还原剂的物质的量之比为 |
B.工业制备高铁酸钠反应中,氧化性: 强于 强于 |
| C.高铁酸钠处理水时放出氧气 |
D. 高铁酸钠处理水完全反应时转移电子的物质的量为 高铁酸钠处理水完全反应时转移电子的物质的量为 |
您最近一年使用:0次
2 . 为减少对环境的污染,工业上常用电解法对煤进行脱硫处理。原理:利用电极反应先将 变为
变为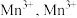 再与煤中的含硫物质(主要为
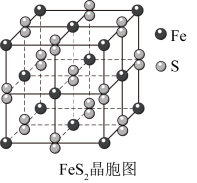
再与煤中的含硫物质(主要为 ,结构如图)发生反应:
,结构如图)发生反应: (未配平)。下列说法不正确的是
(未配平)。下列说法不正确的是
 变为
变为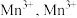 再与煤中的含硫物质(主要为
再与煤中的含硫物质(主要为 ,结构如图)发生反应:
,结构如图)发生反应: (未配平)。下列说法不正确的是
(未配平)。下列说法不正确的是
A. 中存在非极性键 中存在非极性键 |
B.氧化性: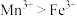 |
C.还原剂与氧化剂的物质的量之比为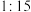 |
D.生成 ,转移电子的物质的量为 ,转移电子的物质的量为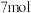 |
您最近一年使用:0次
3 . 海洋是自然界的重要组成部分,我国科学家发现某些生物酶体系能将海洋中的 转化为N2进入大气层,反应历程如图所示。
转化为N2进入大气层,反应历程如图所示。

下列说法不正确的是
 转化为N2进入大气层,反应历程如图所示。
转化为N2进入大气层,反应历程如图所示。
下列说法不正确的是
A. 2 2 2 2 4均为非极性分子 4均为非极性分子 |
| B.生成3molNO时,过程Ⅰ转移3mol电子 |
| C.反应涉及N—O键的断裂和N—N的生成 |
D.过程Ⅱ发生的离子方程式为:   H+ H+ |
您最近一年使用:0次
名校
4 . 双碱法脱硫过程如图所示。下列说法不正确 的是
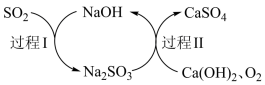

| A.过程I中,SO2表现还原性 |
| B.双碱法脱硫过程中,NaOH可以循环利用 |
| C.过程II中,1 mol O2可氧化2 mol Na2SO3 |
| D.总反应为2Ca(OH)2 + 2SO2 + O2 =2CaSO4 + 2H2O |
您最近一年使用:0次
名校
5 . 有一未完成的离子方程式: 。据此判断下列说法错误的是
。据此判断下列说法错误的是
 。据此判断下列说法错误的是
。据此判断下列说法错误的是| A.X原子最外层电子数为5 |
| B.当有3个X2生成时,转移5个电子 |
C.“□”中所填的微粒为 |
| D.氧化产物和还原产物的质量之比为5∶1 |
您最近一年使用:0次
名校
6 . 硫化氢的转化是资源利用和环境保护的重要研究课题。将H2S和空气的混合气体通入FeCl3、FeCl2和CuCl2的混合溶液中回收S,其转化如下图所示(CuS不溶于水)。下列说法中正确的是


| A.回收S的总反应为:2H2S+O2=2H2O+2S↓ |
| B.过程①中,生成CuS的反应为:Cu2++S2-=CuS↓ |
| C.过程②中,生成Cu2+和Fe2+的个数比为1:1 |
| D.过程③中,各元素化合价均未改变 |
您最近一年使用:0次
7 . 工业制备高纯硅的主要过程:石英砂 粗硅
粗硅 高纯。下列说法错误的是
高纯。下列说法错误的是
 粗硅
粗硅 高纯。下列说法错误的是
高纯。下列说法错误的是A.石英砂的主要成分为 ,可用来制备光导纤维 ,可用来制备光导纤维 |
B.制备粗硅的反应方程式为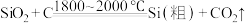 |
C.300℃时发生反应的化学方程式为 |
D.1100℃时发生反应的化学方程式为 |
您最近一年使用:0次
8 . 亚硝酸钠 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是A.滴定前滴定管尖嘴处有气泡,滴定后无气泡会使测得的 含量偏高 含量偏高 |
B.亚硝酸根( )空间结构为V形 )空间结构为V形 |
| C.酸性高锰酸钾溶液可以鉴别食盐和亚硝酸钠 |
D.滴定过程离子反应为: |
您最近一年使用:0次
名校
9 . 锰酸锂( )作为一种新型锂电池正极材料受到广泛关注。工业上利用
)作为一种新型锂电池正极材料受到广泛关注。工业上利用 溶液多途径制备锰酸锂的流程如图,下列说法错误的是
溶液多途径制备锰酸锂的流程如图,下列说法错误的是
①电解槽中反应的离子方程式为 ;
;
②“沉锰、过滤”得到 和
和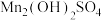 。
。
 )作为一种新型锂电池正极材料受到广泛关注。工业上利用
)作为一种新型锂电池正极材料受到广泛关注。工业上利用 溶液多途径制备锰酸锂的流程如图,下列说法错误的是
溶液多途径制备锰酸锂的流程如图,下列说法错误的是
①电解槽中反应的离子方程式为
 ;
;②“沉锰、过滤”得到
 和
和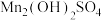 。
。A. 中硫的化合价为+6 中硫的化合价为+6 |
| B.随着电解反应进行,为保持电解液成分和浓度稳定,应不断加入MnO |
C.若“控温、氧化”时溶液的pH显著减小,此时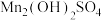 发生反应的化学方程式为 发生反应的化学方程式为 |
D.为控制碳排放,用NaOH溶液吸收煅烧窑中释放的 并转化为正盐,理论上消耗的 并转化为正盐,理论上消耗的 和NaOH的物质的量之比为2∶1 和NaOH的物质的量之比为2∶1 |
您最近一年使用:0次
10 . 锌是重要的金属材料。以硫化锌精矿(主要含有FeS、CuS等杂质)为原料制备单质锌的工业流程如图所示,下列说法不正确的是

已知:金属阳离子在阴极的放电顺序和离子浓度有关

已知:金属阳离子在阴极的放电顺序和离子浓度有关
| A.H2O2反应后生成H2O |
B.烟气主要含 可用钙基固硫法处理 可用钙基固硫法处理 |
C.电解 溶液时,阴极发生还原反应的是锌离子 溶液时,阴极发生还原反应的是锌离子 |
| D.进一步净化过程可投入铁粉去除Cu |
您最近一年使用:0次
2023-09-27更新
|
62次组卷
|
2卷引用:河北省新时代NT教育2024届高三上学期9月阶段测试化学试题



