1 . 次氯酸(HClO)消毒液高效安全,适用于一般物体表面消毒、手部消毒,以及地面、空间和环境消毒。下图装置在D中制得颜色类似于氯气的Cl2O气体,E中得到次氯酸(HClO)。已知Cl2O气体45℃可分解,与水反应生成HClO。
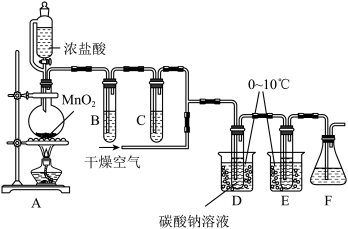
(1)装置A中使用该漏斗的目的是_______ 。
(2)装置A中发生反应的离子方程式为_______ 。
(3)C装置、F装置中分别盛装_______ 、_______ 。
(4)D中盛装碳酸钠溶液用来吸收氯气制备Cl2O。D中生成的气体中含有CO2,则生成Cl2O的化学方程式为_______ 。
(5)实验时,一直要通入干燥的空气,主要作用是_______ ,同时还可以抑制Cl2O的分解,保证实验安全。
(6)为了探究反应条件对产物的影响,另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO 两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH-
两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO
5Cl-+ClO +3H2O
+3H2O
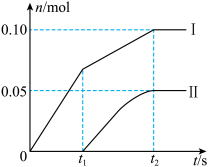
①图中曲线I表示_______ 离子的物质的量随反应时间变化的关系。
②所取石灰乳中含有Ca(OH)2的物质的量为_______ mol,参加反应的氯气的体积为_______ (标况下)
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl-的物质的量为0.37 mol,则产物中 =
=_______ 。

(1)装置A中使用该漏斗的目的是
(2)装置A中发生反应的离子方程式为
(3)C装置、F装置中分别盛装
(4)D中盛装碳酸钠溶液用来吸收氯气制备Cl2O。D中生成的气体中含有CO2,则生成Cl2O的化学方程式为
(5)实验时,一直要通入干燥的空气,主要作用是
(6)为了探究反应条件对产物的影响,另取一定量的石灰乳,缓慢、匀速地通入足量氯气,得出了ClO-、ClO
 两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH-
两种离子的物质的量(n)与反应时间(t)的关系曲线,粗略表示如图(不考虑氯气和水的反应)。已知:氯气和碱的反应为放热反应。温度较高时,氯气和碱还能发生如下反应:3Cl2+6OH- 5Cl-+ClO
5Cl-+ClO +3H2O
+3H2O
①图中曲线I表示
②所取石灰乳中含有Ca(OH)2的物质的量为
③另取一份与②等物质的量的石灰乳,以较大的速率通入足量氯气,反应后测得产物中Cl-的物质的量为0.37 mol,则产物中
 =
=
您最近一年使用:0次
名校
解题方法
2 . 下列说法正确 的是
| A.将铂丝用硫酸洗净后,在外焰上灼烧至火焰颜色与酒精灯火焰一致,再蘸取碳酸钾灼烧,直接可观察到火焰呈紫色 |
| B.容量瓶检漏方法:往瓶内加适量水,塞好瓶塞,用手指按住瓶塞,另一手托住瓶底,将瓶倒立,观察瓶塞周围是否漏水,若不漏水,将瓶正立后把瓶塞旋转180°,再把瓶倒立过来,观察瓶塞周围否漏水,经检查不漏水的容量瓶才能使用 |
| C.用饱和NaHCO3溶液均可除去CO2和Cl2中混有的HCl杂质 |
| D.在实验室制氯气实验中,可以取烧瓶中剩余的溶液少量于试管中,先加入稀硝酸,再加入硝酸银,若出现白色沉淀,即可说明盐酸仍有剩余 |
您最近一年使用:0次
名校
3 . 实验能力和创新意识是化学学科核心素养的重要内容之一、请回答以下问题:
Ⅰ.某实验小组需要 的
的 溶液,请回答:
溶液,请回答:
(1)配制所需主要玻璃仪器除了烧杯、玻璃棒、量筒外,还需要___________ ;
(2)需要称取的 固体的质量为
固体的质量为___________ 。
Ⅱ.某兴趣小组在实验室中模拟工业上用氯气制备无水氯化铝[无水 (183℃升华)遇潮湿空气即产生大量白雾)],可用下列装置制备:
(183℃升华)遇潮湿空气即产生大量白雾)],可用下列装置制备:

(3)装置B中盛放___________ ,其作用是___________ 。F中的是___________ ,其作用是___________ 。
(4)装置A实验开始时,先检查装置的气密性,接下来的操作依次是___________ (填序号)。
①往烧瓶中加入 粉末;②加热;③往烧瓶中加入浓盐酸
粉末;②加热;③往烧瓶中加入浓盐酸
(5)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,同学们提出如下方案:让残留的液体与足量Zn反应,测量生成的 体积。装置如图所示(夹持器具略去),请回答:
体积。装置如图所示(夹持器具略去),请回答:

①使丫形管中的残余清液与锌粒反应的正确操作是将___________ 转移到___________ 中;
②平视读数前应依次进行的两步操作是___________ 。
Ⅰ.某实验小组需要
 的
的 溶液,请回答:
溶液,请回答:(1)配制所需主要玻璃仪器除了烧杯、玻璃棒、量筒外,还需要
(2)需要称取的
 固体的质量为
固体的质量为Ⅱ.某兴趣小组在实验室中模拟工业上用氯气制备无水氯化铝[无水
 (183℃升华)遇潮湿空气即产生大量白雾)],可用下列装置制备:
(183℃升华)遇潮湿空气即产生大量白雾)],可用下列装置制备:
(3)装置B中盛放
(4)装置A实验开始时,先检查装置的气密性,接下来的操作依次是
①往烧瓶中加入
 粉末;②加热;③往烧瓶中加入浓盐酸
粉末;②加热;③往烧瓶中加入浓盐酸(5)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,同学们提出如下方案:让残留的液体与足量Zn反应,测量生成的
 体积。装置如图所示(夹持器具略去),请回答:
体积。装置如图所示(夹持器具略去),请回答:
①使丫形管中的残余清液与锌粒反应的正确操作是将
②平视读数前应依次进行的两步操作是
您最近一年使用:0次
4 . 实验室用图所示装置制备KClO溶液,并通过KClO溶液与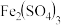 溶液的反应制备高效水处理剂高铁酸钾
溶液的反应制备高效水处理剂高铁酸钾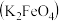 。
。

(1) ,其中铁元素的化合价为
,其中铁元素的化合价为_______ 。
(2)B装置的作用是_______ 。
(3)写出装置A中制备 的化学方程式:
的化学方程式:_______ 。
(4)装置D中发生的离子反应方程式_______ 。
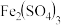 溶液的反应制备高效水处理剂高铁酸钾
溶液的反应制备高效水处理剂高铁酸钾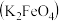 。
。
(1)
 ,其中铁元素的化合价为
,其中铁元素的化合价为(2)B装置的作用是
(3)写出装置A中制备
 的化学方程式:
的化学方程式:(4)装置D中发生的离子反应方程式
您最近一年使用:0次
5 . 根据下列装置图回答问题:

(1)实验室制备的氯气往往含有氯化氢和水蒸气杂质,需先后通过装有___________ 和___________ 的洗气瓶,才能得到干燥、纯净的氯气。
(2)A、B通入Cl2后,观察到的现象是___________ 。
(3)装置B中发生反应的离子方程式是___________ 。
(4)实验开始后,观察装置C中的现象是___________ 。
(5)通入Cl2时装置D中发生反应的离子方程式是___________ 。
(6)装置E中发生反应的离子方程式是___________ 。
(7)装置F的作用是___________ 。

(1)实验室制备的氯气往往含有氯化氢和水蒸气杂质,需先后通过装有
(2)A、B通入Cl2后,观察到的现象是
(3)装置B中发生反应的离子方程式是
(4)实验开始后,观察装置C中的现象是
(5)通入Cl2时装置D中发生反应的离子方程式是
(6)装置E中发生反应的离子方程式是
(7)装置F的作用是
您最近一年使用:0次
2021-11-15更新
|
145次组卷
|
2卷引用:浙江省宁波市三锋教研联盟2021-2022学年高一上学期11月期中考试化学试题
6 . 下列实验装置不能达到实验目的的是
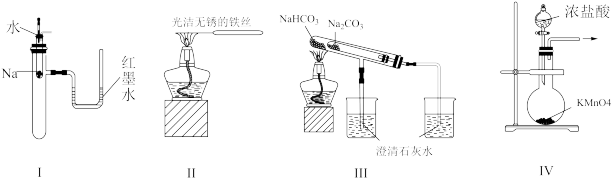

| A.图I:验证Na和水反应是否为放热反应 | B.图II:观察纯碱的焰色试验 |
| C.图III:比较Na2CO3、NaHCO3的稳定性 | D.图IV:制取Cl2 |
您最近一年使用:0次
2021-11-15更新
|
228次组卷
|
2卷引用:浙江省宁波市三锋教研联盟2021-2022学年高一上学期11月期中考试化学试题
解题方法
7 . 某同学用下列装置制备并检验Cl2的性质。下列说法正确的是
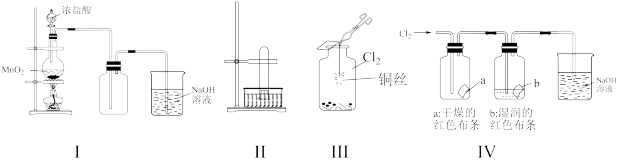

| A.I图中:如果MnO2过量,盐酸就可全部消耗 |
| B.II图中:如果倒置的试管充满了氯气,水槽内装满水,经足够长的时间光照,试管内最后剩余气体为氧气 |
| C.III图中:生成蓝色的烟 |
| D.IV图中:a、b中的有色布条褪色,将硫酸溶液滴入烧杯中至溶液呈酸性,结果有Cl2生成 |
您最近一年使用:0次
解题方法
8 . 下列“类比”结果正确的是
| A.氯气能使紫色石蕊试液先变红后褪色,则SO2也能使紫色石蕊试液先变红后褪色 |
| B.SiH4的沸点比CH4高,则PH3的沸点也比NH3高 |
| C.CO2是酸性氧化物,则NO2也是酸性氧化物 |
| D.MnO2与浓HCl共热可制Cl2,则MnO2与浓HBr共热也可制Br2 |
您最近一年使用:0次
9 . 某学习小组探究潮湿的Cl2与Na2CO3反应的产物,进行如下实验:
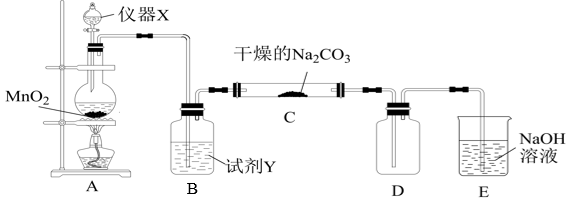
请回答:
(1)仪器X的名称是:_______ ,试剂Y是_______ 。
(2)装置E的作用是:_______ 。
(3)请写出发生装置A中的离子方程式:_______ 。
(4)装置C中潮湿Cl2与Na2CO3以等物质的量反应,生成NaHCO3、气体Cl2O和另一种盐,试写出该反应方程式:_______ 。
(5)某学习小组用下图装置研究气体Z的性质,气体Z的主要成分是氯气,其中含有少量水蒸气。请回答下列问题:
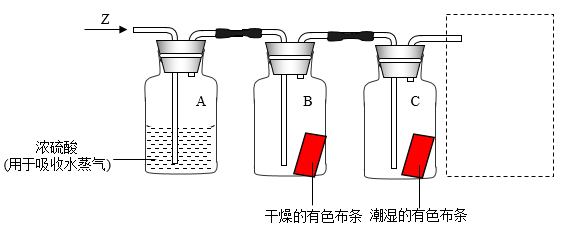
分别描述B、C装置中的现象:B_______ ,C_______ ,从物质性质说明B、C装置中现象不同的原因_______ 。

请回答:
(1)仪器X的名称是:
(2)装置E的作用是:
(3)请写出发生装置A中的离子方程式:
(4)装置C中潮湿Cl2与Na2CO3以等物质的量反应,生成NaHCO3、气体Cl2O和另一种盐,试写出该反应方程式:
(5)某学习小组用下图装置研究气体Z的性质,气体Z的主要成分是氯气,其中含有少量水蒸气。请回答下列问题:

分别描述B、C装置中的现象:B
您最近一年使用:0次
10 . 无水氯化铝常作为有机合成和石油化工的催化剂。工业上可由金属铝和纯净的氯气作用制备。某课外兴趣小组在实验室里,通过如图所示装置,制取少量纯净的无水氯化铝。据此回答下列问题:

查阅资料:常温下,无水氯化铝为白色晶体,易吸收水分,在178 ℃升华。装有无水氯化铝的试剂瓶久置潮湿空气中,会自动爆炸并产生大量白雾。
(1)写出A装置中,实验室制取Cl2的离子方程式 _______ ;
(2)仪器甲为_______ (写名称);装置B中加入的试剂是_______ ;装置C中加入的试剂是_______ ;
(3)为制得较纯净的氯化铝,实验开始时应先点燃酒精灯_______ (填“A”或“D”), F装置中碱石灰所起的作用是_______ ;
(4)若A装置中导出的气体若不经过B、C装置而直接进入D装置中,产生的后果是_______ 。

查阅资料:常温下,无水氯化铝为白色晶体,易吸收水分,在178 ℃升华。装有无水氯化铝的试剂瓶久置潮湿空气中,会自动爆炸并产生大量白雾。
(1)写出A装置中,实验室制取Cl2的
(2)仪器甲为
(3)为制得较纯净的氯化铝,实验开始时应先点燃酒精灯
(4)若A装置中导出的气体若不经过B、C装置而直接进入D装置中,产生的后果是
您最近一年使用:0次



