名校
1 . Ⅰ.实验室需要配制0.1 mol·L-1NaOH溶液500mL。
(1)根据计算用托盘天平称取的质量为__________ g。在下图所示仪器中,配制上述溶液肯定不需要的是_________ (填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是 _____________ 。

(2)配制时,其正确的操作顺序是(用字母表示,每个操作只用一次)__________ 。
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(3)下面操作造成所配NaOH溶液浓度偏高的是(_____ )
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
II.向浓度相等、体积均为100 mL 的 A、B 两份NaOH 溶液中,分别通入一定量的 CO2 后,再向所得溶液中滴加0.1 mol/L 盐酸 , 产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。
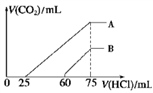
(4)①A 曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2 的最大体积是_________ mL(标准状况)。
②B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为______________ 。
III.某学生用 Na2CO3和 NaHCO3 组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等且不考虑HCl的挥发)
(5)原混合物样品中 n(Na2CO3)∶n(NaHCO3)=____________ , 盐酸的物质的量浓度为________ mol/L ,实验③反应后,至少需继续加入_____ mL的该盐酸溶液才能把混合物全部反应。
(1)根据计算用托盘天平称取的质量为

(2)配制时,其正确的操作顺序是(用字母表示,每个操作只用一次)
A.用少量水洗涤烧杯2次~3次,洗涤液均注入容量瓶,振荡
B.在盛有NaOH固体的烧杯中加入适量水溶解
C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,反复上下颠倒,摇匀
E.改用胶头滴管加水,使溶液凹液面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1 cm~2 cm处
(3)下面操作造成所配NaOH溶液浓度偏高的是(
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
II.向浓度相等、体积均为100 mL 的 A、B 两份NaOH 溶液中,分别通入一定量的 CO2 后,再向所得溶液中滴加0.1 mol/L 盐酸 , 产生 CO2 的体积(标准状况)与所加盐酸的体积关系如图所示。

(4)①A 曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2 的最大体积是
②B 曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为
III.某学生用 Na2CO3和 NaHCO3 组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等且不考虑HCl的挥发)
| 实验序号 | ① | ② | ③ |
| 盐酸体积/mL | 50 | 50 | 50 |
| 固体质量/g | 4.11 | 8.22 | 16.44 |
| 生成气体体积/L(标况) | 1.008 | 2.016 | 2.016 |
(5)原混合物样品中 n(Na2CO3)∶n(NaHCO3)=
您最近一年使用:0次
2017-03-11更新
|
539次组卷
|
2卷引用:2016-2017学年黑龙江省大庆实验中学高一下学期开学考试化学试卷
名校
解题方法
2 . 化工生产中常常用到“三酸两碱”,“三酸”指硝酸、硫酸和盐酸,“两碱”指烧碱和纯碱。
(1)从物质的分类角度看,不恰当的一种物质是_______ (填化学式)。
(2)“三酸”与“两碱”之间均可反应,酸过量时若用化学方程式表示有六个,若用离子方程式表示却只有两个,请写出这两个离子方程式_______ ,_______ 。
(3)“三酸”常用于溶解金属和金属氧化物。某化学兴趣小组在烧杯中放入铜屑和稀硫酸,加热并不断通入空气,观察到溶液逐渐变为蓝色,用化学方程式表示这一实验过程_______ 。
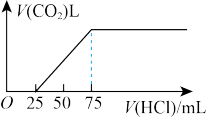
(4)烧碱可吸收CO2,当含0.2molNaOH的溶液吸收一定量CO2后,向溶液中逐滴滴加稀盐酸,下图表示加入盐酸体积和生成的CO2的体积的关系,曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是_______ ,所用的稀盐酸的物质的量浓度为_______ (保留2位小数)。
(1)从物质的分类角度看,不恰当的一种物质是
(2)“三酸”与“两碱”之间均可反应,酸过量时若用化学方程式表示有六个,若用离子方程式表示却只有两个,请写出这两个离子方程式
(3)“三酸”常用于溶解金属和金属氧化物。某化学兴趣小组在烧杯中放入铜屑和稀硫酸,加热并不断通入空气,观察到溶液逐渐变为蓝色,用化学方程式表示这一实验过程
(4)烧碱可吸收CO2,当含0.2molNaOH的溶液吸收一定量CO2后,向溶液中逐滴滴加稀盐酸,下图表示加入盐酸体积和生成的CO2的体积的关系,曲线表明原NaOH溶液中通入CO2后,所得溶液中的溶质成分是

您最近一年使用:0次
2017-02-17更新
|
619次组卷
|
2卷引用:黑龙江省哈尔滨师范大学附属中学2018届高三10月月考化学试题
3 . 把一定浓度的NaOH溶液分成两等份,一份密闭保存,另一份敞口放置,几天后分别与相同浓度的盐酸反应,都恰好完全反应时,若第一份用去盐酸V1mL,第二份用去盐酸V2mL,则两者的关系为
| A.V1=V2 | B.V1>V2 | C.V1<V2 | D.不能确定 |
您最近一年使用:0次
名校
4 . 向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体后,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl的物质的量的关系如下图(忽略CO2的溶解和HCl的挥发)。
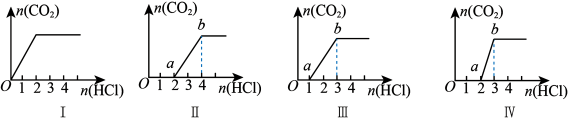
则下列分析都正确的组合是
①Ⅰ图对应溶液中的溶质为NaHCO3
②Ⅱ图对应溶液中的溶质为Na2CO3和NaHCO3,且二者的物质的量之比为1:1
③Ⅲ图对应溶液中的溶质为NaOH和Na2CO3,且二者的物质的量之比为1:1
④Ⅳ图对应溶液中的溶质为Na2CO3

则下列分析都正确的组合是
①Ⅰ图对应溶液中的溶质为NaHCO3
②Ⅱ图对应溶液中的溶质为Na2CO3和NaHCO3,且二者的物质的量之比为1:1
③Ⅲ图对应溶液中的溶质为NaOH和Na2CO3,且二者的物质的量之比为1:1
④Ⅳ图对应溶液中的溶质为Na2CO3
| A.①② | B.①③ | C.②④ | D.②③ |
您最近一年使用:0次
2016-12-09更新
|
1347次组卷
|
26卷引用:黑龙江省哈尔滨师范大学青冈实验中学校2019届高三上学期9月月考化学试题
黑龙江省哈尔滨师范大学青冈实验中学校2019届高三上学期9月月考化学试题黑龙江省哈尔滨师范大学青冈实验中学校2019届高三10月月考化学试题黑龙江省鹤岗市绥滨县第一中学2021-2022学年高三上学期期中考试化学试题黑龙江省齐齐哈尔市部分学校2022-2023学年高一上学期11月期中考试化学试题2017届海南省国兴中学高三上学期第一次月考化学试卷2018版化学(苏教版)高考总复习课时跟踪训练:钠、镁及其重要化合物陕西省西安市长安区第一中学2017-2018学年高一上学期第二次月考化学(实验班)试题(已下线)解密05 金属及其化合物(教师版)——备战2018年高考化学之高频考点解密(已下线)2019高考备考一轮复习精品资料 第三章 金属及其化合物 第1讲 钠及其氧化物【押题专练】天津市滨海新区大港油田一中2019届高三上学期期中考试化学试题内蒙古第一机械制造(集团)有限公司第一中学2018-2019学年高一上学期12月月考化学试题(已下线)2019高考热点题型和提分秘籍 第三章 金属及其化合物 第1讲 钠及化合物 (题型专练)吉林省白城市第一中学2018-2019学年高一上学期12月月考化学试题(已下线)2019年7月28日《每日一题》 2020届一轮复习 每周一测福建省莆田市莆田第二十五中学2020届高三上学期期中考试化学试题福建省福州市八县一中2019-2020学年高一年上学期期末联考化学试卷(已下线)专题3.1 金属钠及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》(已下线)【南昌新东方】师大附中2019-2020 高一(上) 期末(已下线)3.2.2 碳酸钠 碳酸氢钠练习(2)——《高中新教材同步备课》(苏教版 必修第一册)(已下线)专题05 钠及其化合物(核心精讲)——【新教材精创】2019-2020学年高中化学新教材知识讲学高一必修第一册(苏教2019版)专题3 易错疑难集训(三)(已下线)专题05 金属及其重要化合物-备战2021届高考化学二轮复习题型专练陕西省韩城市西庄中学2021-2022学年高三上学期9月月考化学试题辽宁省抚顺市抚顺县高级中学2021-2022学年高三10月月考化学试题江苏省常州市第一中学2021-2022学年高一上学期期中考试化学试题宁夏银川一中2021-2022学年高一上学期期中考试化学试题
5 . 有FeO、Fe2O3的混合物若干克,在足量H2气流中加热充分反应,冷却后称得剩余固体比原混合物减轻0.8 g;将等质量的原混合物与盐酸反应,欲使之完全溶解,至少需要1 mol/L盐酸的体积为
| A.0.1 L | B.0.2 L | C.0.5 L | D.1.0 L |
您最近一年使用:0次
6 . 在两个烧杯中分别盛有100mL 3.0mol·L-1的盐酸和氢氧化钠溶液,向两个烧杯中分别加入等质量的铝粉,在相同状况下生成的气体的体积比为2∶5,则加入的铝粉的质量为
| A.8.10g | B.5.40g | C.6.75g | D.2.70g |
您最近一年使用:0次
名校
7 . 向NaOH溶液中通入CO2气体后得到溶液M,因CO2通入的量不同,溶液M的组成也不同。若向M中逐滴加入盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图。则下列分析正确的是(不计CO2溶解)
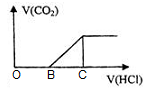

| A.若OB=0,则溶液M为Na2CO3溶液 |
| B.若OB=BC,则形成溶液M所发生反应的离子方程式为OH-+CO2 → HCO3- |
| C.若溶液M中c(NaHCO3)=2c(Na2CO3),则3OB=BC |
| D.若溶液M中大量存在的阴离子为CO32-和HCO3-,则OB>BC |
您最近一年使用:0次
2016-12-09更新
|
399次组卷
|
6卷引用:黑龙江省哈尔滨师范大学附属中学2020-2021学年高三上学期开学考试化学试题
名校
解题方法
8 . 浓度相同的NaOH溶液各100 mL倒入A、B、C三个烧杯中,分别向三份溶液中通入不等量的CO2,充分反应后,再向三份所得溶液中逐滴加入0.2 mol/L的盐酸,产生CO2的体积与所加盐酸体积之间关系如下图所示。下列判断正确的是(气体体积取标准状况计算)
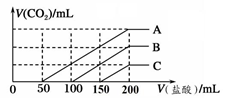

| A.通入CO2后,A烧杯中的溶质成分是Na2CO3 |
| B.B烧杯中通入的CO2体积为448 mL |
| C.原NaOH溶液的浓度为0.2 mol/L |
| D.通入CO2后,C烧杯中溶质成分的物质的量之比为n(NaOH)∶n(Na2CO3)=1∶2 |
您最近一年使用:0次
2016-12-09更新
|
1580次组卷
|
7卷引用:黑龙江省大庆市东风中学2019-2020学年高一上学期期末考试化学试题
黑龙江省大庆市东风中学2019-2020学年高一上学期期末考试化学试题2014-2015湖北省武汉华中师大附高一上学期期末化学试卷福建师大附中2017-2018学年高一上学期期末考试化学试题【全国百强校】内蒙古自治区赤峰市第二中学2018-2019学年高一上学期第二次月考化学试题山西省太原市山西大学附属中学2019-2020学年高一上学期12月月考化学试题江西省南昌市第二中学2020-2021学年高一上学期第三次月考化学试题(已下线)专题38 CO2与盐或碱溶液反应产物的判断-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)
名校
9 . 由铝硅两种物质组成的试样11 g,均匀地分成等质量的两份,一份与足量的盐酸接触可产生气体a L,一份与足量的NaOH溶液接触产生同样的气体b L,则此试样中铝与硅的质量比为
| A.4a /3(b-a) | B.9a/7(b-a) | C.a/(b-a) | D.无法计算 |
您最近一年使用:0次
2016-12-09更新
|
161次组卷
|
3卷引用:2014-2015黑龙江省哈尔滨六中高一12月月考化学试卷
名校
10 . 现有25 mL 2 mol·L-1 Na2CO3和75 mL 1 mol·L-1的稀盐酸:①将Na2CO3溶液缓缓滴到稀盐酸中 ②将稀盐酸缓缓滴到Na2CO3溶液中,在标准状况下产生气体的体积情况
| A.均为0.84 L |
| B.均为0.56 L |
| C.①>② |
| D.②>① |
您最近一年使用:0次
2016-12-09更新
|
1400次组卷
|
14卷引用:2015-2016学年黑龙江牡丹江一中高二下期末化学试卷
2015-2016学年黑龙江牡丹江一中高二下期末化学试卷2016-2017学年黑龙江哈尔滨六中高一上期末化学卷(已下线)2014年高考化学苏教版一轮复习3-1钠、镁及其化合物练习卷2015-2016学年北京大学附属中学分校高一上抽考化学试卷2016-2017学年江西省南昌市第十中学高一下学期分班考试化学试卷山西省临汾第一中学2017-2018学年高一上学期第二次调研(期中)考试化学试题【全国百强校】福建省三明市第一中学2018-2019学年高一上学期第二次月考化学试题云南省通海县三中2019-2020学年高一上学期期中考试化学试题山西省应县第一中学校2019-2020学年高一上学期第三次月考化学试题山西省晋城市高平第一中学2019-2020学年高一上学期12月月考化学试题云南省福贡县第一中学2019-2020学年高一上学期期末考试化学试题云南省元阳县第三中学2019-2020学年高一上学期期末考试化学试题福建省厦门第一中学2019-2020学年高一上学期12月月考化学试题高一必修第一册(鲁科2019)第1章 微项目 探秘膨松剂



