名校
解题方法
1 . 下列说法正确的是
| A.某黄色溶液与淀粉-KI溶液混合后呈蓝色,说明该溶液一定是氯水 |
| B.NaOH溶液可盛放在带磨口玻璃塞的玻璃瓶中,也可盛放在带橡胶塞的玻璃瓶中 |
C.若用 制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入 制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入 |
D.由 可知,硅酸的酸性强于碳酸 可知,硅酸的酸性强于碳酸 |
您最近一年使用:0次
2023-03-11更新
|
582次组卷
|
5卷引用:辽宁省沈阳市第二十中学2022-2023学年高一下学期开学考试化学试题
名校
2 . 铁是人类较早使用的金属之一,运用所学知识,回答下列问题。
(1)下列有关铁、铁矿石与铁的氧化物的说法正确的是
(2)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。写出FeCl3溶液与金属铜发生反应的离子方程式_______ 。
(3)已知FeCl3易吸收空气里的水分而潮解,100℃左右时易升华,实验室制备FeCl3的装置如图所示。

回答下列问题:
①仪器X的名称为_______ ,装置A中发生反应的化学方程式为_______ 。
②装置B中溶液为_______ ,C的作用是_______ 。
③加热时,先点燃装置A的酒精灯,当_______ 时,再点燃装置D的酒精灯。
④用粗硬质玻璃管直接连接装置D和E,比用细导管连接的优点是_______ 。
⑤装置F中碱石灰的成分是NaOH和CaO混合物,其作用是(提示:从不同角度作答2条)_______ 。
(1)下列有关铁、铁矿石与铁的氧化物的说法正确的是
| A.在自然界中,不可能有游离态的铁存在 |
| B.赤铁矿的主要成分是Fe2O3,Fe2O3俗称铁红 |
| C.能通过化合反应制得Fe(OH)3,但不能通过化合反应制得FeCl2 |
| D.铁的氧化物能与酸反应生成盐和水,因此Fe3O4、Fe2O3、FeO都是碱性氧化物 |
(3)已知FeCl3易吸收空气里的水分而潮解,100℃左右时易升华,实验室制备FeCl3的装置如图所示。

回答下列问题:
①仪器X的名称为
②装置B中溶液为
③加热时,先点燃装置A的酒精灯,当
④用粗硬质玻璃管直接连接装置D和E,比用细导管连接的优点是
⑤装置F中碱石灰的成分是NaOH和CaO混合物,其作用是(提示:从不同角度作答2条)
您最近一年使用:0次
3 . 根据下列实验内容得出的结论正确的是
| 选项 | 实验内容 | 结论 |
| A | 向某溶液中滴加 溶液后,再滴加稀盐酸,产生白色沉淀不溶解 溶液后,再滴加稀盐酸,产生白色沉淀不溶解 | 该溶液中含有 |
| B | 向某溶液逐滴加入NaOH溶液,先有白色胶状沉淀产生,后来沉淀逐渐消失 | 溶液中可能含有 |
| C | 向某溶液中滴加氯水,然后再滴加KSCN溶液后溶液显红色 | 溶液中含有 |
| D | 向某无色溶液中滴加盐酸,有无色无味的气体产生该气体能使澄清石灰水变浑浊 | 该溶液中含有 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 价类二维图是学习元素及其化合物知识的重要模型。铁元素的价类二维图如图所示,下列有关说法正确的是
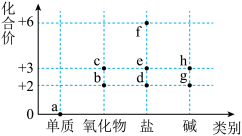

| A.铁的化学性质比较活泼,所以在自然界中没有游离态的a存在 |
| B.c是一种红棕色的固体,可由Fe、水蒸气高温反应制得 |
| C.f可以作新型的绿色净水剂 |
| D.物质g在空气中不能直接转化为h |
您最近一年使用:0次
5 . 下列说法错误的是
| A.可通过化合反应由铁制得FeCl2 |
| B.可通过复分解反应由一种强酸制一种弱酸 |
| C.可通过分解反应由一种单质制备一种化合物 |
| D.可通过非氧化还原反应由一种单质制备另一种单质 |
您最近一年使用:0次
名校
解题方法
6 . 向含有FeCl3和BaCl2的酸性溶液中通入足量的SO2,有白色沉淀生成,过滤后向滤液中滴入KSCN溶液时,无明显现象,由此得出的正确结论是
| A.白色沉淀是FeSO3 |
| B.白色沉淀是BaSO3和BaSO4的混合物 |
| C.白色沉淀是BaSO4 |
| D.FeCl3已全部被SO2氧化成FeCl2 |
您最近一年使用:0次
2023-03-07更新
|
321次组卷
|
2卷引用:辽宁省东北中山中学2022-2023学年高一下学期4月月考考化学试题
名校
解题方法
7 . 菠菜富含膳食纤维、胡萝卜素、维生素c、维生素e、钙、磷、铁、等矿物质。14~18岁青少年每日合理摄入铁量为20~25mg,某化学小组针对菠菜中含铁量进行如下实验。
(一)实验目的:菠菜含铁量是否满足青少年日常所需
(二)实验方案:取适量新鲜菠菜平均分成三份,实验操作和现象记录如下:
(1)灼烧菠菜时,除了酒精灯还需要下列仪器中的_______ (填选项)。
A. B.
B. C.
C. D.
D.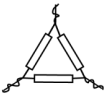 E.
E.
(2)写出实验三中 参与的最主要反应的离子方程式
参与的最主要反应的离子方程式_______ 。
(3)检验试剂KSCN溶液中的 采用
采用_______ 的方法。
(4)由三组实验做出如下推断,其中合理的是:_______(填选项)。
(三)实验数据:菠菜中含铁量的测定,实验步骤如下:
①取 新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
②向灰分中加入 盐酸和
盐酸和 ,浸泡
,浸泡 ,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并;
,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并;
③将合并液定容成 待测液,利用分光光度法测得铁的浓度为
待测液,利用分光光度法测得铁的浓度为 。
。
根据上述实验,回答下列问题:
(5)步骤②洗涤烧杯和沉淀的目的是_______ 。
(6)步骤③定容操作若仰视容量瓶刻度线,会造成菠菜样品含铁量测定结果_______ 。(填“偏高”、“偏低”或“无影响”)。
(7)根据实验数据计算菠菜含铁量为_______ 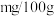 。
。
(四)实验结论:由于菠菜中含有大量草酸( )与铁元素形成沉淀影响铁元素吸收,所以不是理想的补铁剂。(附:猪肝每
)与铁元素形成沉淀影响铁元素吸收,所以不是理想的补铁剂。(附:猪肝每 中含铁量达到
中含铁量达到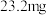 ,且容易被人体吸收。)
,且容易被人体吸收。)
(一)实验目的:菠菜含铁量是否满足青少年日常所需
(二)实验方案:取适量新鲜菠菜平均分成三份,实验操作和现象记录如下:
| 实验 | 操作步骤 | 检验试剂 | 现象 |
| 实验一 | 适量蒸馏水浸泡,过滤,取滤液,加检验试剂后加入适量 ,再次加入检验试剂 ,再次加入检验试剂 | KSCN溶液 | 均无明显现象 |
| 实验二 | 充分灼烧,加适量盐酸浸泡,取滤液,加检验试剂 | KSCN溶液 | 极浅的红色 |
| 实验三 | 充分灼烧,加适量盐酸、 浸泡,取滤液,加检验试剂 浸泡,取滤液,加检验试剂 | KSCN溶液 | 较深的红色 |
A.
 B.
B. C.
C. D.
D. E.
E.
(2)写出实验三中
 参与的最主要反应的离子方程式
参与的最主要反应的离子方程式(3)检验试剂KSCN溶液中的
 采用
采用(4)由三组实验做出如下推断,其中合理的是:_______(填选项)。
| A.菠菜样品中含铁量极低 | B.菠菜中的铁元素很难用蒸馏水直接溶出 |
| C.仅用盐酸无法溶出菠菜灰分中的铁元素 | D.灼烧的目的是将菠菜中的铁元素氧化 |
(三)实验数据:菠菜中含铁量的测定,实验步骤如下:
①取
 新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。②向灰分中加入
 盐酸和
盐酸和 ,浸泡
,浸泡 ,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并;
,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并;③将合并液定容成
 待测液,利用分光光度法测得铁的浓度为
待测液,利用分光光度法测得铁的浓度为 。
。根据上述实验,回答下列问题:
(5)步骤②洗涤烧杯和沉淀的目的是
(6)步骤③定容操作若仰视容量瓶刻度线,会造成菠菜样品含铁量测定结果
(7)根据实验数据计算菠菜含铁量为
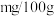 。
。(四)实验结论:由于菠菜中含有大量草酸(
 )与铁元素形成沉淀影响铁元素吸收,所以不是理想的补铁剂。(附:猪肝每
)与铁元素形成沉淀影响铁元素吸收,所以不是理想的补铁剂。(附:猪肝每 中含铁量达到
中含铁量达到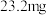 ,且容易被人体吸收。)
,且容易被人体吸收。)
您最近一年使用:0次
2023-03-02更新
|
601次组卷
|
4卷引用:辽宁省沈阳市2022-2023学年高一上学期期末教学质量监测化学试题
名校
8 . 下列实验装置或操作不能达到实验目的的是
| A | B | C | D |
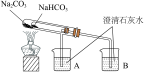 | 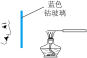 | 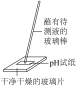 | 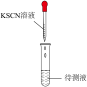 |
比较 、 、 的热稳定性 的热稳定性 | 观察 的焰色试验 的焰色试验 | 测定某浓度氯气溶液的 | 检验 溶液是否变质 溶液是否变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-03-02更新
|
211次组卷
|
3卷引用:辽宁省丹东市2022-2023学年高一上学期期末教学质量监测化学试题
解题方法
9 . 为提纯下列物质(括号内是杂质),所选试剂错误的是
| 选项 | 物质 | 除杂试剂 |
 | 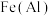 |  溶液 溶液 |
 | 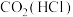 | 饱和 溶液 溶液 |
 |  溶液 溶液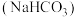 |  |
 |  溶液 溶液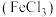 | 铁粉 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 高铁酸钠(Na2FeO4)是一种新型水处理剂。某兴趣小组欲利用废金属屑(主要成分为Fe和Cu,还含有少量Fe2O3)制取高铁酸钠并回收金属Cu,其工艺流程图如图。
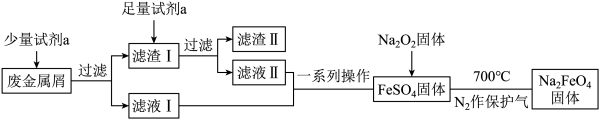
请回答下列问题:
(1)Na2FeO4处理水时,不仅能杀菌消毒,还能形成______ 吸附水中悬浮杂质而净化水。
(2)试剂a为______ (填化学式)。
(3)滤渣Ⅱ的主要成分为______ (填化学式)。
(4)在过滤操作中要使用玻璃棒,其作用是______ 。
(5)检验滤液Ⅰ中是否存在Fe3+的实验方法是______ 。
(6)滤液Ⅱ中有少量Cu2+,产生的原因是______ (用离子方程式表示)。
(7)生成Na2FeO4的反应原理是:2FeSO4+6Na2O2 2Na2FeO4+2Na2O+2Na2SO4+O2↑,当反应中转移电子总数为9.03×1023时,生成Na2FeO4的物质的量为
2Na2FeO4+2Na2O+2Na2SO4+O2↑,当反应中转移电子总数为9.03×1023时,生成Na2FeO4的物质的量为______ mol。

请回答下列问题:
(1)Na2FeO4处理水时,不仅能杀菌消毒,还能形成
(2)试剂a为
(3)滤渣Ⅱ的主要成分为
(4)在过滤操作中要使用玻璃棒,其作用是
(5)检验滤液Ⅰ中是否存在Fe3+的实验方法是
(6)滤液Ⅱ中有少量Cu2+,产生的原因是
(7)生成Na2FeO4的反应原理是:2FeSO4+6Na2O2
 2Na2FeO4+2Na2O+2Na2SO4+O2↑,当反应中转移电子总数为9.03×1023时,生成Na2FeO4的物质的量为
2Na2FeO4+2Na2O+2Na2SO4+O2↑,当反应中转移电子总数为9.03×1023时,生成Na2FeO4的物质的量为
您最近一年使用:0次



