名校
1 . 化学反应与能量变化是化学家研究的永恒话题。
(1)据报道,有科学家提出硅是“21世纪的能源”、“未来石油”的观点。硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等,硅光电池是一种把___ 能转化为___ 能的装置。
II.水煤气变换[CO(g)+H2O(g) CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域。
CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域。
(2)在800℃、2L密闭容器中,若充入3molCO和2mol水蒸气进行反应,保持温度不变,5min反应达平衡,测得生成1.2molCO2,则该反应的速率v(CO)为___ 。
(3)Shibata曾做过下列实验:721℃下,分别用氢气和一氧化碳还原氧化钴(CoO),反应如下。
i.H2(g)+CoO(s) Co(s)+H2O(g) △H1
Co(s)+H2O(g) △H1
ii.CO(g)+CoO(s) Co(s)+CO2(g) △H2
Co(s)+CO2(g) △H2
①反应CO(g)+H2O(g) CO2(g)+H2(g)△H=
CO2(g)+H2(g)△H=___ (用△H1、△H2表示)。
②一氧化碳和水蒸气的反应历程如图,下列说法正确的是___ 。
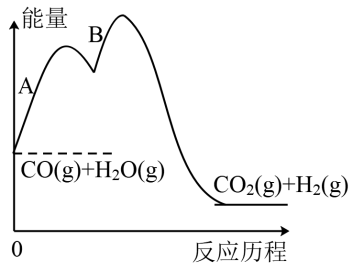
a.该反应放热
b.反应B活化能大于反应A
c.使用催化剂降低反应的△H,反应速率加快
d.该反应经过两步基元反应完成
(1)据报道,有科学家提出硅是“21世纪的能源”、“未来石油”的观点。硅光电池作为电源已广泛应用于人造卫星、灯塔和无人气象站等,硅光电池是一种把
II.水煤气变换[CO(g)+H2O(g)
 CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域。
CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域。(2)在800℃、2L密闭容器中,若充入3molCO和2mol水蒸气进行反应,保持温度不变,5min反应达平衡,测得生成1.2molCO2,则该反应的速率v(CO)为
(3)Shibata曾做过下列实验:721℃下,分别用氢气和一氧化碳还原氧化钴(CoO),反应如下。
i.H2(g)+CoO(s)
 Co(s)+H2O(g) △H1
Co(s)+H2O(g) △H1ii.CO(g)+CoO(s)
 Co(s)+CO2(g) △H2
Co(s)+CO2(g) △H2①反应CO(g)+H2O(g)
 CO2(g)+H2(g)△H=
CO2(g)+H2(g)△H=②一氧化碳和水蒸气的反应历程如图,下列说法正确的是

a.该反应放热
b.反应B活化能大于反应A
c.使用催化剂降低反应的△H,反应速率加快
d.该反应经过两步基元反应完成
您最近一年使用:0次
2 . 向Na2CO3溶液中滴加盐酸,反应过程中能量变化如图所示,下列说法正确的是
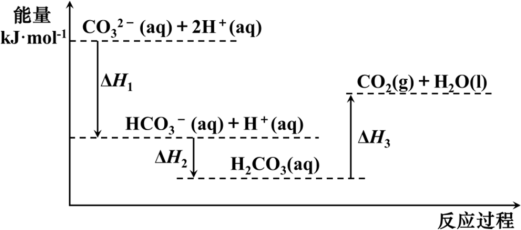

A.反应 (aq)+2H+(aq) = CO2(g)+H2O(l)为放热反应 (aq)+2H+(aq) = CO2(g)+H2O(l)为放热反应 |
| B.ΔH1>ΔH3>ΔH2 |
C. (aq)+H+(aq)=CO2(g)+H2O(l) ΔH = ΔH2—ΔH3 (aq)+H+(aq)=CO2(g)+H2O(l) ΔH = ΔH2—ΔH3 |
| D.H2CO3(aq)=CO2(g)+H2O(l) ΔH3 <0 |
您最近一年使用:0次
2021-12-06更新
|
361次组卷
|
4卷引用:福建省福清西山学校2021-2022学年高二上学期12月月考化学试题
解题方法
3 . 已知热化学方程式:①H2(g) +  O2(g) = H2O(l) △H = -285.8 kJ∙mol-1,
O2(g) = H2O(l) △H = -285.8 kJ∙mol-1,
②H2(g) + O2(g) = H2O(g) △H = -241.8 kJ∙mol-1。下列说法正确的是
O2(g) = H2O(g) △H = -241.8 kJ∙mol-1。下列说法正确的是
 O2(g) = H2O(l) △H = -285.8 kJ∙mol-1,
O2(g) = H2O(l) △H = -285.8 kJ∙mol-1,②H2(g) +
 O2(g) = H2O(g) △H = -241.8 kJ∙mol-1。下列说法正确的是
O2(g) = H2O(g) △H = -241.8 kJ∙mol-1。下列说法正确的是| A.2H2(g) + O2(g) = 2H2O △H = -527.6 kJ∙mol-1 |
| B.H2O(g) = H2O(l) △H = +44 kJ∙mol-1 |
| C.①表示在298K时,由1mol H2(g)和0.5mol O2(g)反应生成1mol H2O(l)放出285.8kJ热量 |
D.②表示在298K时,1分子氢气和 分子氧气反应生成1 分子水蒸气放出241.8kJ热量 分子氧气反应生成1 分子水蒸气放出241.8kJ热量 |
您最近一年使用:0次
2021-12-06更新
|
142次组卷
|
2卷引用:福建省福清西山学校2021-2022学年高二上学期12月月考化学试题
4 . 请回答下列问题:
(1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下16g SiH4自燃放出热量713.6kJ。SiH4自燃的热化学方程式为___________ 。
(2)标准摩尔生成焓是指在25℃和101kPa时,最稳定的单质生成1mol化合物的焓变。
已知25℃和101kPa时下列反应:①2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l) ∆H=-3116kJ/mol
②C(石墨,s)+O2(g)=CO2(g) ∆H=-393.5kJ/mol
③2H2(g)+O2(g)=2H2O(l) ∆H=-571.6kJ/mol
写出乙烷标准摩尔生成焓的热化学方程式:___________ 。
(3)肼(N2H4)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1mol化学键需的能量(kJ):N≡N为942、O=O为500、N-N为154,则断裂1mol N-H键需要___________ kJ的能量。

(1)SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态H2O。已知室温下16g SiH4自燃放出热量713.6kJ。SiH4自燃的热化学方程式为
(2)标准摩尔生成焓是指在25℃和101kPa时,最稳定的单质生成1mol化合物的焓变。
已知25℃和101kPa时下列反应:①2C2H6(g)+7O2(g)=4CO2(g)+6H2O(l) ∆H=-3116kJ/mol
②C(石墨,s)+O2(g)=CO2(g) ∆H=-393.5kJ/mol
③2H2(g)+O2(g)=2H2O(l) ∆H=-571.6kJ/mol
写出乙烷标准摩尔生成焓的热化学方程式:
(3)肼(N2H4)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1mol化学键需的能量(kJ):N≡N为942、O=O为500、N-N为154,则断裂1mol N-H键需要

您最近一年使用:0次
名校
5 . 科学家研究出一种以天然气为燃料的“燃烧前捕获系统”,其简单流程如图所示(条件及物质未标出)。

(1)已知: 、CO、
、CO、 的标准燃烧热(ΔH)分别为
的标准燃烧热(ΔH)分别为 、
、 、
、 ,则上述流程中第一步反应
,则上述流程中第一步反应 的
的
___________ 。
(2)工业中 和
和 制备甲醇的方程式为
制备甲醇的方程式为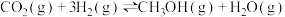 ,某温度下,将
,某温度下,将 和
和 充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下
充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下 的平衡转化率为
的平衡转化率为___________ 。
(3)某温度下,将 和
和 按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得
按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
___________  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4) 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃: 。在0.1MPa时,按
。在0.1MPa时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
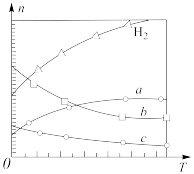
①该反应的ΔH___________ (填“>”或“<”)。
②曲线c表示的物质为___________ 。
③为提高 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是___________ 。

(1)已知:
 、CO、
、CO、 的标准燃烧热(ΔH)分别为
的标准燃烧热(ΔH)分别为 、
、 、
、 ,则上述流程中第一步反应
,则上述流程中第一步反应 的
的
(2)工业中
 和
和 制备甲醇的方程式为
制备甲醇的方程式为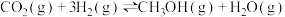 ,某温度下,将
,某温度下,将 和
和 充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下
充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下 的平衡转化率为
的平衡转化率为| 时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
 | 0.90 | 0.85 | 0.836 | 0.81 | 0.80 | 0.80 |
 和
和 按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得
按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(4)
 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃: 。在0.1MPa时,按
。在0.1MPa时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
①该反应的ΔH
②曲线c表示的物质为
③为提高
 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是
您最近一年使用:0次
名校
6 . 下列四幅图示所表示的信息与对应的叙述相符的是
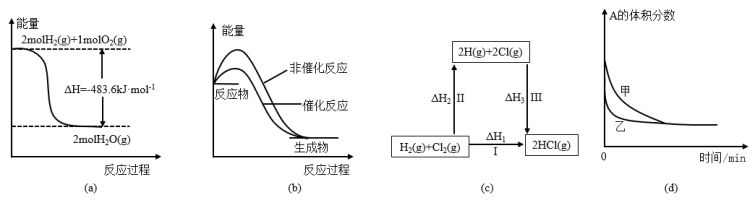

A.图(a)表示 与 与 发生反应过程中的能量变化,则 发生反应过程中的能量变化,则 的标准燃烧热为 的标准燃烧热为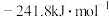 |
| B.图(b)表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
C.图(c)表示一定条件下 和 和 生成HCl的反应热与途径无关,则 生成HCl的反应热与途径无关,则 |
D.图(d)表示压强对可逆反应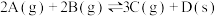 的影响,甲的压强大 的影响,甲的压强大 |
您最近一年使用:0次
2021-11-17更新
|
263次组卷
|
2卷引用:福建师范大学附属中学2021-2022学年高二上学期期中考试化学试题
7 . 煤化工中常常需研究不同温度下的平衡常数、投料比及热值等问题。
(1)在一定条件下:①C(s)+CO2(g) 2CO(g)
2CO(g)
②C(s)+H2O(g) CO(g)+H2(g)
CO(g)+H2(g)
③CO(g)+H2O(g) H2(g)+CO2(g)
H2(g)+CO2(g)
如果在一定温度下,三个反应的平衡常数分别为K1、K2和K3,则K1、K2、K3之间的关系是___________ 。
(2)已知C(s)+H2O(g) CO(g)+H2(g)的平衡常数和温度关系如表
CO(g)+H2(g)的平衡常数和温度关系如表
①该反应的平衡常数表达式___________ ;△H___________ 0(填﹤,﹥或=)
②某温度下,各物质的平衡浓度符合下式:13C(H2O)=5C(CO)·C(H2),则该温度是___________ ℃
③恒温恒容条件下,下列各项能表示该反应达到平衡状态是_____
A.消耗C(s)的物质的量与生成CO(g)的物质的量之比为1∶1
B.断开2molH—O键,同时生成1molH—H键
C.压强不再变化
D.气体密度不再变化
(3)工业上还可以利用生成的一氧化碳和氢气来合成甲醇。
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
已知某温度下向体积为1升的恒容容器中充入CO(g)和H2(g)各1mol/L。平衡时,其中某种气体反应物的浓度为0.75mol/L,同时生成甲醇的浓度为0.25mol/L。
①气体反应物是___________ ,该温度下反应的平衡常数K=_____ .另一种气体反应物的平衡转化率为___________ 。
②相同条件下,向该平衡体系中再充入三种物质各0.25mol,此时反应的V(正)___________ V(逆)(填﹤,﹥或=)。
(1)在一定条件下:①C(s)+CO2(g)
 2CO(g)
2CO(g)②C(s)+H2O(g)
 CO(g)+H2(g)
CO(g)+H2(g)③CO(g)+H2O(g)
 H2(g)+CO2(g)
H2(g)+CO2(g)如果在一定温度下,三个反应的平衡常数分别为K1、K2和K3,则K1、K2、K3之间的关系是
(2)已知C(s)+H2O(g)
 CO(g)+H2(g)的平衡常数和温度关系如表
CO(g)+H2(g)的平衡常数和温度关系如表| 温度℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 0.6 | 0.9 | 1 | 1.7 | 2.6 |
①该反应的平衡常数表达式
②某温度下,各物质的平衡浓度符合下式:13C(H2O)=5C(CO)·C(H2),则该温度是
③恒温恒容条件下,下列各项能表示该反应达到平衡状态是
A.消耗C(s)的物质的量与生成CO(g)的物质的量之比为1∶1
B.断开2molH—O键,同时生成1molH—H键
C.压强不再变化
D.气体密度不再变化
(3)工业上还可以利用生成的一氧化碳和氢气来合成甲醇。
CO(g)+2H2(g)
 CH3OH(g)
CH3OH(g)已知某温度下向体积为1升的恒容容器中充入CO(g)和H2(g)各1mol/L。平衡时,其中某种气体反应物的浓度为0.75mol/L,同时生成甲醇的浓度为0.25mol/L。
①气体反应物是
②相同条件下,向该平衡体系中再充入三种物质各0.25mol,此时反应的V(正)
您最近一年使用:0次
8 . 下图是合成氨反应和使用铁触媒作催化剂的催化历程。
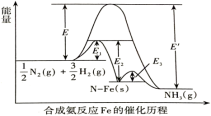
已知:① N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g) ΔH1
NH3(g) ΔH1
② N2(g)+Fe(s)=N-Fe(s) ΔH2
N2(g)+Fe(s)=N-Fe(s) ΔH2
③N-FeS(s)+ H2(g)=NH3(g)+Fe(s) ΔH3
H2(g)=NH3(g)+Fe(s) ΔH3
下列说法正确的是

已知:①
 N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g) ΔH1
NH3(g) ΔH1②
 N2(g)+Fe(s)=N-Fe(s) ΔH2
N2(g)+Fe(s)=N-Fe(s) ΔH2③N-FeS(s)+
 H2(g)=NH3(g)+Fe(s) ΔH3
H2(g)=NH3(g)+Fe(s) ΔH3下列说法正确的是
| A.反应①逆反应的活化能为E′ |
| B.ΔH2=E2-E1 |
| C.相同条件下,反应③的速率最慢 |
D.键能关系: E(N≡N)+ E(N≡N)+ E(H-H)>3E(N-H) E(H-H)>3E(N-H) |
您最近一年使用:0次
11-12高二上·河南许昌·阶段练习
名校
解题方法
9 . 已知热化学方程式:
H2O(g)=H2(g) + 1/2O2(g) △H = +241.8kJ/mol
H2(g)+ 1/2O2(g) = H2O(l) △H = -285.8kJ/mol
当1mol液态水变为水蒸气时,其热量变化是
H2O(g)=H2(g) + 1/2O2(g) △H = +241.8kJ/mol
H2(g)+ 1/2O2(g) = H2O(l) △H = -285.8kJ/mol
当1mol液态水变为水蒸气时,其热量变化是
| A.吸热88kJ | B.吸热2.44KJ | C.放热44kJ | D.吸热44KJ |
您最近一年使用:0次
2021-11-12更新
|
47次组卷
|
22卷引用:福建省福州格致鼓山中学、教院二附中、铜盘中学、十五中、十中2023-2024学年高二上学期期末联考化学试题
福建省福州格致鼓山中学、教院二附中、铜盘中学、十五中、十中2023-2024学年高二上学期期末联考化学试题(已下线)2011-2012年河南省长葛市第三实验高中高二上学期第一次月考化学试卷(已下线)2011-2012学年四川省雅安中学高二下学期3月月考化学试卷(已下线)2012-2013学年海南省农垦加来中学高二第一次月考化学试卷(已下线)2012-2013学年湖南省益阳市一中高二上学期期末考试理科化学试卷(已下线)2014-2015学年北京市第六十六中学高二上第一次质量检测化学试卷2014-2015四川省雅安中学高二下学期开学考试化学试卷2015-2016学年宁夏银川第九中学高二上学期期中测试化学试卷江西省南昌市第二中学2017-2018学年高二上学期第一次月考化学试题陕西省西安市电子科技中学2017-2018学年高二上学期第一次月考化学试题天津市杨柳青一中2017-2018第一学期高二第一次化学月考江西省九江市第一中学2017-2018学年高二上学期第二次月考化学试题(已下线)【南昌新东方】江西省九江第一中学2017-2018学年高二上学期第二次月考化学试题河北省邢台市第二中学2019-2020学年高二下学期开学考试化学试题江西省赣州市赣县区第三中学2020-2021学年高二(实验重点班)9月月考化学试题西藏拉萨市第二高级中学2019-2020学年高二上学期期中考试化学试题广西壮族自治区贺州市平桂高级中学(贺州市第五高级中学)2020-2021学年高二上学期第一次月考化学试题河南省长垣市第十中学2020-2021学年高二上学期第二次月考化学试题甘肃省庆阳市第六中学2021-2022学年高二上学期期中考试化学(理)试题四川省广安代市中学校2021-2022学年高二上学期第一次月考化学试题(已下线)2011-2012学年陕西省宝鸡中学高一下学期期中考试化学试卷2017届河北省石家庄辛集中学高三上期中化学试卷
10 . 化学链燃烧(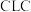 )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集
)是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于
。基于 载氧体的甲烷化学链燃烧技术示意图如下。
载氧体的甲烷化学链燃烧技术示意图如下。
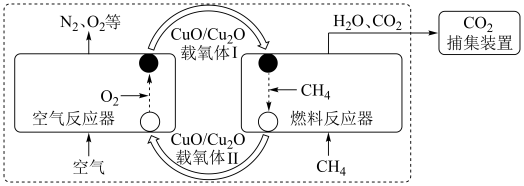
空气反应器与燃料反应器中发生的反应分别为:
①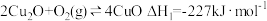
②
(1)反应

_______  。
。
(2)反应②的平衡常数表达式
_______ 。
(3)氧的质量分数:载氧体Ⅰ_______ (填“>”“=”或“<”)载氧体Ⅱ。
(4)往盛有 载氧体的刚性密闭容器中充入空气【氧气的物质的量分数
载氧体的刚性密闭容器中充入空气【氧气的物质的量分数 为21%】,发生反应①。平衡时
为21%】,发生反应①。平衡时 随反应温度T变化的曲线如图所示。
随反应温度T变化的曲线如图所示。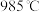 时
时 的平衡转化率
的平衡转化率
_______ (保留2位有效数字)。
(5)根据下图, 随温度升高而增大的原因是
随温度升高而增大的原因是_______ 。反应温度必须控制在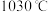 以下,原因是
以下,原因是_______ 。

(6)载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的 载氧体,反应②活化能如下表所示。
载氧体,反应②活化能如下表所示。
由表中数据判断:使用_______ (填“氧化铝”或“膨润土”)掺杂的载氧体反应较快;使用氧化铝或者膨润土掺杂的载氧体,单位时间内燃料反应器释放的热量分别为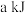 、
、 ,则a
,则a_______ b(填“>”“=”或“<”)。
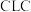 )是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集
)是利用载氧体将空气中的氧传输至燃料的新技术,与传统燃烧方式相比,避免了空气和燃料的直接接触,有利于高效捕集 。基于
。基于 载氧体的甲烷化学链燃烧技术示意图如下。
载氧体的甲烷化学链燃烧技术示意图如下。
空气反应器与燃料反应器中发生的反应分别为:
①
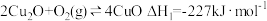
②

(1)反应


 。
。(2)反应②的平衡常数表达式

(3)氧的质量分数:载氧体Ⅰ
(4)往盛有
 载氧体的刚性密闭容器中充入空气【氧气的物质的量分数
载氧体的刚性密闭容器中充入空气【氧气的物质的量分数 为21%】,发生反应①。平衡时
为21%】,发生反应①。平衡时 随反应温度T变化的曲线如图所示。
随反应温度T变化的曲线如图所示。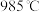 时
时 的平衡转化率
的平衡转化率
(5)根据下图,
 随温度升高而增大的原因是
随温度升高而增大的原因是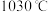 以下,原因是
以下,原因是
(6)载氧体掺杂改性,可加快化学链燃烧速率。使用不同掺杂的
 载氧体,反应②活化能如下表所示。
载氧体,反应②活化能如下表所示。| 载氧体掺杂物质 | 氧化铝 | 膨润土 |
活化能/ |  | 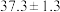 |
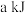 、
、 ,则a
,则a
您最近一年使用:0次
2021-11-09更新
|
5639次组卷
|
7卷引用:福建省福州市福建师范大学附属中学2022-2023学年高二下学期期末化学试题
福建省福州市福建师范大学附属中学2022-2023学年高二下学期期末化学试题福建省龙岩第一中学2021-2022学年高二下学期开学考试(实验班)化学试题北京市铁路第二中学2022-2023学年高二上学期期中检测化学试题2021年新高考福建化学高考真题(已下线)专题15 化学反应原理综合题-三年(2020-2022)高考真题分项汇编(已下线)专题17 原理综合题(已下线)专题17 原理综合题



