解题方法
1 . 利用CO2催化加氢制二甲醚,可以实现CO2的再利用,该过程中涉及以下两个反应:
①

②

则反应 的
的 为
为
①


②


则反应
 的
的 为
为A.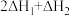 | B.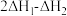 | C.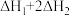 | D.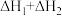 |
您最近一年使用:0次
2 . 甲醇既可用于基本有机原料,又可作为燃料用于替代矿物燃料。
(1)以下是工业上合成甲醇的反应:CO(g)+2H2(g) CH3OH(g) △H,下表所列数据是该反应在不同温度下的化学平衡常数(K)
CH3OH(g) △H,下表所列数据是该反应在不同温度下的化学平衡常数(K)
由表中数据判断反应为___________ 热反应(填“吸”或“放”);某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)=0.2mol/L,则CO的转化率为___________ ,此时的温度为___________ (从表中选择)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H1kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2kJ/mol
③H2O(g)=H2O(l) △H3kJ/mol
则CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=___________ kJ/mol(用△H1、△H2、△H3表示)
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有 )时,实验室利用如图装置模拟该法:
)时,实验室利用如图装置模拟该法:___________ 。
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10-5mol·L-1时,Cr3+沉淀完全,此时溶液的pH=___________ 。(已知,Ksp=6.4×10-31,lg2=0.3)
(1)以下是工业上合成甲醇的反应:CO(g)+2H2(g)
 CH3OH(g) △H,下表所列数据是该反应在不同温度下的化学平衡常数(K)
CH3OH(g) △H,下表所列数据是该反应在不同温度下的化学平衡常数(K)| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) △H1kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H2kJ/mol
③H2O(g)=H2O(l) △H3kJ/mol
则CH3OH(l)+O2(g)=CO(g)+2H2O(l) △H=
(3)现以甲醇燃料电池,采用电解法来处理酸性含铬废水(主要含有
 )时,实验室利用如图装置模拟该法:
)时,实验室利用如图装置模拟该法: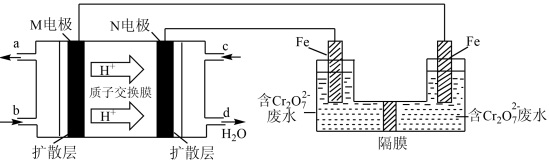
(4)处理废水时,最后Cr3+以Cr(OH)3形式除去,当c(Cr3+)=1×10-5mol·L-1时,Cr3+沉淀完全,此时溶液的pH=
您最近一年使用:0次
名校
解题方法
3 . 以CO2和H2为原料制造更高价值的化学产品是用来缓解温室效应的研究方向。
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:
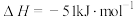
反应Ⅱ:
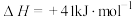
①已知几种化学键的键能如下表所示,则a=_____ kJ·mol-1.
②若反应Ⅱ逆反应活化能 ,则该反应的正反应的活化能
,则该反应的正反应的活化能
_____ kJ·mol-1.
(2)向2L容器中充入1molCO2和2molH2,若只发生反应I,测得反应在不同压强下平衡混合物中甲醇体积分数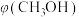 随温度变化如图1所示,逆反应速率与容器中
随温度变化如图1所示,逆反应速率与容器中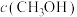 关系如图2所示:
关系如图2所示:
①图1中P1_____ P2(填“>”、“<”或“=”);
②图2中x点平衡体系时升温,反应重新达平衡状态时新平衡点可能是_____ (填字母序号)。 、
、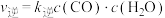 ,k正、k逆分别表示正逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lgk正随温度T变化关系的直线是
,k正、k逆分别表示正逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lgk正随温度T变化关系的直线是_____ ,表示lgk逆随温度T变化关系的直线是_____ 。
(4)已知一定温度下按照起始比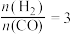 ,在一密闭容器中进行反应:
,在一密闭容器中进行反应: ,保持总压为2.1MPa不变,达到平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数
,保持总压为2.1MPa不变,达到平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数
_____ MPa-2(保留2位有效数字)(各气体分压=平衡体系中各气体的体积分数×总压)。
(5)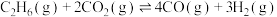
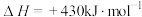 ,在四种不同容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是_____(填字母)。
,在四种不同容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是_____(填字母)。
(1)工业上常用CO2和H2为原料合成甲醇(CH3OH),过程中发生如下两个反应:
反应I:

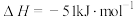
反应Ⅱ:

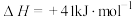
①已知几种化学键的键能如下表所示,则a=
| 化学键 | C—H | C—O | H—O | H—H | C≡O |
| 键能/kJ·mol-1 | 406 | 351 | 465 | 436 | a |
 ,则该反应的正反应的活化能
,则该反应的正反应的活化能
(2)向2L容器中充入1molCO2和2molH2,若只发生反应I,测得反应在不同压强下平衡混合物中甲醇体积分数
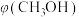 随温度变化如图1所示,逆反应速率与容器中
随温度变化如图1所示,逆反应速率与容器中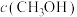 关系如图2所示:
关系如图2所示:①图1中P1
②图2中x点平衡体系时升温,反应重新达平衡状态时新平衡点可能是

 、
、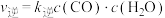 ,k正、k逆分别表示正逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lgk正随温度T变化关系的直线是
,k正、k逆分别表示正逆反应速率常数,只与温度有关。则图3中所示的甲、乙、丙、丁四条直线中,表示lgk正随温度T变化关系的直线是(4)已知一定温度下按照起始比
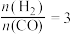 ,在一密闭容器中进行反应:
,在一密闭容器中进行反应: ,保持总压为2.1MPa不变,达到平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数
,保持总压为2.1MPa不变,达到平衡时CO的平衡转化率为50%,则该条件下用平衡体系中各气体分压表示的平衡常数
(5)
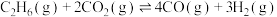
 ,在四种不同容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是_____(填字母)。
,在四种不同容器中发生上述反应,若初始温度、压强和反应物用量均相同,则CO2的转化率最高的是_____(填字母)。| A.恒温恒容容器 | B.恒容绝热容器 |
| C.恒压绝热容器 | D.恒温恒压容器 |
您最近一年使用:0次
名校
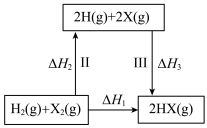
4 . 下列关于如图所示转化关系(X代表 ),说法
),说法正确 的是
 ),说法
),说法
A.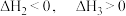 | B.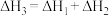 |
C. 是该反应的活化能 是该反应的活化能 | D.若X分别是 ,则过程Ⅲ放出的热量依次减少 ,则过程Ⅲ放出的热量依次减少 |
您最近一年使用:0次
名校
5 . Ⅰ.将氮氧化物进行无害化处理对治理大气污染、建设生态文明具有重要意义。
(1) 的氧化性强于
的氧化性强于 ,能更有效地氧化NO。已知:
,能更有效地氧化NO。已知:

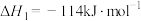

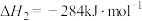
则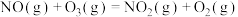
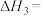
______  。
。
(2)在汽车排气管上安装催化转化器,能有效消除尾气对环境的污染:
①
 ,反应能自发进行所需温度条件
,反应能自发进行所需温度条件_______ (填“高温”或“低温”)。
②已知:反应
 ,
, 和CO在
和CO在 作用下发生的反应分两步进行:
作用下发生的反应分两步进行:
第一步;
第二步:
反应过程的能量变化如图所示:
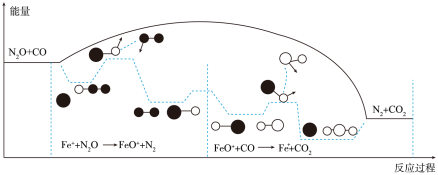
决定总反应速率的是________ (填“第一步”或“第二步)
(3)某温度下,在催化剂的作用下发生反应: ,测得密闭容器中不同时间时CO和NO的浓度如表。
,测得密闭容器中不同时间时CO和NO的浓度如表。
①温度下,该反应的平衡常数为______ 。
②该恒温恒容条件下,下列能说明该反应达到化学平衡状态的是________ (填序号)。
a.体系的压强保持不变 b.
c.混合气体的密度不变 d.NO的转化率保持不变
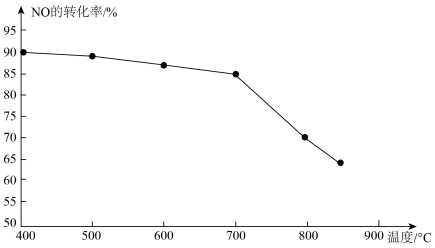
③恒容条件下,上述反应中若NO和CO的起始浓度一定,催化反应相同时间,测得NO的转化率随温度的变化如图所示,当温度超过700℃时,随温度的升高,NO的转化率下降明显,原因是________ 。
Ⅱ.由于亚硝酸钠和食盐性状相似,曾多次发生过将 误当食盐食用的事件。欲测定某样品中
误当食盐食用的事件。欲测定某样品中 的含量,某同学设计如下实验:①称取样品ag,加水溶解,配制成100mL溶液。②取25.00mL溶液于锥形概中,用
的含量,某同学设计如下实验:①称取样品ag,加水溶解,配制成100mL溶液。②取25.00mL溶液于锥形概中,用 标准溶液(酸性)进行滴定,滴定结束后消耗
标准溶液(酸性)进行滴定,滴定结束后消耗 溶液VmL。
溶液VmL。
(4)在进行滴定操作时, 溶液盛装在
溶液盛装在_____ (填“酸式”或“碱式”)滴定管中。当滴入最后半滴 溶液,
溶液,_______ 时达到滴定终点。
(5)以下操作造成测定结果偏高的是________。
(6)滴定过程中发生反应的离子方程式是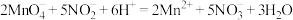 ,测得该样品中
,测得该样品中 的质量分数为
的质量分数为______ 。( 的摩尔质量
的摩尔质量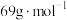 )
)
(1)
 的氧化性强于
的氧化性强于 ,能更有效地氧化NO。已知:
,能更有效地氧化NO。已知:
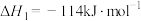

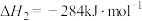
则
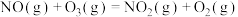
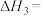
 。
。(2)在汽车排气管上安装催化转化器,能有效消除尾气对环境的污染:
①

 ,反应能自发进行所需温度条件
,反应能自发进行所需温度条件②已知:反应

 ,
, 和CO在
和CO在 作用下发生的反应分两步进行:
作用下发生的反应分两步进行:第一步;

第二步:

反应过程的能量变化如图所示:

决定总反应速率的是
(3)某温度下,在催化剂的作用下发生反应:
 ,测得密闭容器中不同时间时CO和NO的浓度如表。
,测得密闭容器中不同时间时CO和NO的浓度如表。| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
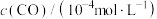 | 36.0 | 30.5 | 28.5 | 27.5 | 27.0 | 27.0 |
 | 10.0 | 4.5 | 2.5 | 1.5 | 1.0 | 1.0 |
②该恒温恒容条件下,下列能说明该反应达到化学平衡状态的是
a.体系的压强保持不变 b.

c.混合气体的密度不变 d.NO的转化率保持不变
③恒容条件下,上述反应中若NO和CO的起始浓度一定,催化反应相同时间,测得NO的转化率随温度的变化如图所示,当温度超过700℃时,随温度的升高,NO的转化率下降明显,原因是

Ⅱ.由于亚硝酸钠和食盐性状相似,曾多次发生过将
 误当食盐食用的事件。欲测定某样品中
误当食盐食用的事件。欲测定某样品中 的含量,某同学设计如下实验:①称取样品ag,加水溶解,配制成100mL溶液。②取25.00mL溶液于锥形概中,用
的含量,某同学设计如下实验:①称取样品ag,加水溶解,配制成100mL溶液。②取25.00mL溶液于锥形概中,用 标准溶液(酸性)进行滴定,滴定结束后消耗
标准溶液(酸性)进行滴定,滴定结束后消耗 溶液VmL。
溶液VmL。(4)在进行滴定操作时,
 溶液盛装在
溶液盛装在 溶液,
溶液,(5)以下操作造成测定结果偏高的是________。
A.滴定管未用 标准溶液润洗 标准溶液润洗 |
| B.盛装标准溶液的滴定管,滴定前尖端有气泡,滴定后气泡消失 |
| C.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后俯视读数 |
| D.若滴定过程中刚出现颜色变化就停止滴定 |
(6)滴定过程中发生反应的离子方程式是
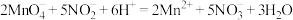 ,测得该样品中
,测得该样品中 的质量分数为
的质量分数为 的摩尔质量
的摩尔质量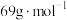 )
)
您最近一年使用:0次
6 . 党的二十大报告指出,要积极稳妥推进碳达峰、碳中和。二氧化碳的捕集、利用与封存(CCUS)已成为科学家研究的重要课题。
I.工业上用 和
和 在一定条件下可以合成乙烯:
在一定条件下可以合成乙烯: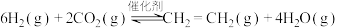

已知:①
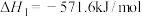
②
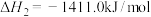
③
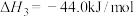
(1)
__________ (用 、
、 、
、 表示)。
表示)。
(2)恒温恒容下,向密闭容器按投料比 通入原料气,能判断该反应处于平衡状态的是_______(填标号)。
通入原料气,能判断该反应处于平衡状态的是_______(填标号)。
(3)向密闭容器按投料比 通入原料气(,不同温度对
通入原料气(,不同温度对 的平衡转化率和催化剂催化效率的影响如图所示,则压强
的平衡转化率和催化剂催化效率的影响如图所示,则压强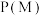
__________ 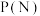 ,原因是:
,原因是:__________ 。

Ⅱ. 催化加氢可以直接合成二甲醚。涉及以下主要反应:
催化加氢可以直接合成二甲醚。涉及以下主要反应:
①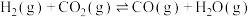

②

恒压条件下, 、起始量相等时,
、起始量相等时, 的平衡转化率和的选择性随温度变化如下图所示。
的平衡转化率和的选择性随温度变化如下图所示。
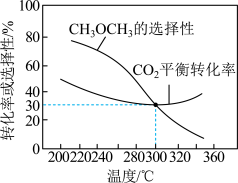
已知:的选择性 %
%
(4)300℃时,通入 、
、 各
各 ,平衡时
,平衡时 的选择性、
的选择性、 的平衡转化率均为30%,则此温度下反应①的平衡常数
的平衡转化率均为30%,则此温度下反应①的平衡常数
__________ (保留2位有效数字)。
(5)温度高于300℃, 的平衡转化率随温度升高而增大的原因可能是
的平衡转化率随温度升高而增大的原因可能是__________ 。
Ⅲ.电化学法也可还原二氧化碳制乙烯,原理如下图所示。
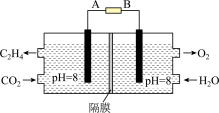
(6)该电池的阴极电极反应式为:__________ 。
I.工业上用
 和
和 在一定条件下可以合成乙烯:
在一定条件下可以合成乙烯: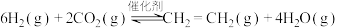

已知:①

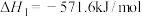
②

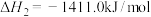
③

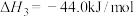
(1)

 、
、 、
、 表示)。
表示)。(2)恒温恒容下,向密闭容器按投料比
 通入原料气,能判断该反应处于平衡状态的是_______(填标号)。
通入原料气,能判断该反应处于平衡状态的是_______(填标号)。A. |
| B.混合气体的密度保持不变 |
| C.混合气体的平均相对分子质量保持不变 |
D.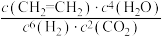 保持不变 保持不变 |
(3)向密闭容器按投料比
 通入原料气(,不同温度对
通入原料气(,不同温度对 的平衡转化率和催化剂催化效率的影响如图所示,则压强
的平衡转化率和催化剂催化效率的影响如图所示,则压强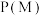
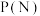 ,原因是:
,原因是:
Ⅱ.
 催化加氢可以直接合成二甲醚。涉及以下主要反应:
催化加氢可以直接合成二甲醚。涉及以下主要反应:①
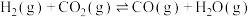

②


恒压条件下,
 、起始量相等时,
、起始量相等时, 的平衡转化率和的选择性随温度变化如下图所示。
的平衡转化率和的选择性随温度变化如下图所示。
已知:的选择性
 %
%(4)300℃时,通入
 、
、 各
各 ,平衡时
,平衡时 的选择性、
的选择性、 的平衡转化率均为30%,则此温度下反应①的平衡常数
的平衡转化率均为30%,则此温度下反应①的平衡常数
(5)温度高于300℃,
 的平衡转化率随温度升高而增大的原因可能是
的平衡转化率随温度升高而增大的原因可能是Ⅲ.电化学法也可还原二氧化碳制乙烯,原理如下图所示。

(6)该电池的阴极电极反应式为:
您最近一年使用:0次
7 . 资源化利用 ,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品.回答下列问题.
,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品.回答下列问题.
(1)理论研究表明,在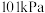 和
和 下,
下, 异构化反应过程的能量变化如图所示:计算可得
异构化反应过程的能量变化如图所示:计算可得
_____________  ,
, 与
与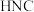 稳定性较强的是
稳定性较强的是_____________ . 吸附剂.
吸附剂.结合下图 分析聚合离子液体吸附 的有利条件是
的有利条件是_____________ .
工业上以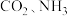 为原料生产尿素
为原料生产尿素 ,该反应分为二步进行:
,该反应分为二步进行:
第一步: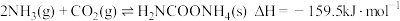
第二步: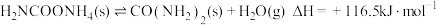
①写出上述合成尿素的热化学方程式_____________ .
②某实验小组模拟工业上合成尿素,在一定体积的密闭容器中投入 和
和 ,实验测得反应中各组分物质的量随时间的变化如下图所示:
,实验测得反应中各组分物质的量随时间的变化如下图所示:_____________ 步反应决定,总反应进行到_____________  时到达平衡.
时到达平衡.
(4)合成乙酸:
中国科学家首次以 和
和 为原料高效合成乙酸,其反应路径如下图所示:
为原料高效合成乙酸,其反应路径如下图所示:根据图示 ,写出总反应的化学方程式_____________ .
 ,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品.回答下列问题.
,不仅可以减少温室气体的排放,还可以获得燃料或重要的化工产品.回答下列问题.(1)理论研究表明,在
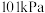 和
和 下,
下, 异构化反应过程的能量变化如图所示:计算可得
异构化反应过程的能量变化如图所示:计算可得
 ,
, 与
与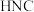 稳定性较强的是
稳定性较强的是
 吸附剂.
吸附剂. 的有利条件是
的有利条件是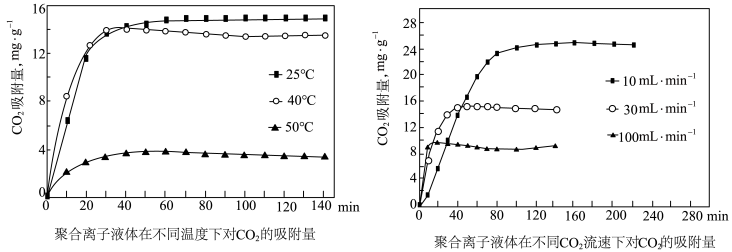
工业上以
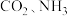 为原料生产尿素
为原料生产尿素 ,该反应分为二步进行:
,该反应分为二步进行:第一步:
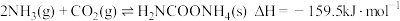
第二步:
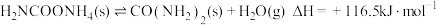
①写出上述合成尿素的热化学方程式
②某实验小组模拟工业上合成尿素,在一定体积的密闭容器中投入
 和
和 ,实验测得反应中各组分物质的量随时间的变化如下图所示:
,实验测得反应中各组分物质的量随时间的变化如下图所示: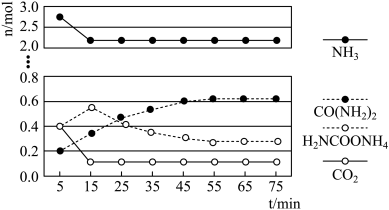
 时到达平衡.
时到达平衡.(4)合成乙酸:
中国科学家首次以
 和
和 为原料高效合成乙酸,其反应路径如下图所示:
为原料高效合成乙酸,其反应路径如下图所示: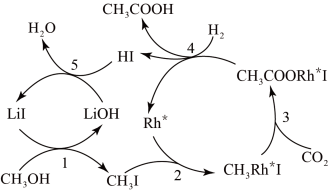
您最近一年使用:0次
8 . “绿水青山就是金山银山。”研究如何将NO2、NO、CO、SO2等大气污染物转化为能参与大气循环的物质,对建设美丽中国具有重要意义。
(1) 可在一定条件下转化为
可在一定条件下转化为 。已知:
。已知:

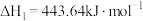

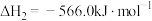
甲醇 是一种重要的化工原料,也可以直接用作燃料。试写出
是一种重要的化工原料,也可以直接用作燃料。试写出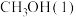 在氧气中完全燃烧生成
在氧气中完全燃烧生成 和
和 的热化学方程式:
的热化学方程式:___________ 。
(2)科研人员研发出一种由强碱溶液作电解质溶液的新型甲醇手机电池,充满电后手机可连续使用一个月,则放电时,甲醇在___________ (填“正”或“负”)极发生反应,其电极反应式为___________ 。
(3) 可在一定条件下转化为
可在一定条件下转化为 。向
。向 密闭容器中通入
密闭容器中通入 和
和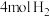 ,在适合的催化剂和
,在适合的催化剂和 温度下,发生反应
温度下,发生反应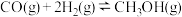
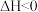 ,保持容器容积一直不变,
,保持容器容积一直不变, 时,反应达到平衡状态,
时,反应达到平衡状态,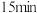 时改变温度为
时改变温度为 ,
, 时反应再次达到平衡状态,部分数据如下表:
时反应再次达到平衡状态,部分数据如下表:
① 时反应达到平衡,此时
时反应达到平衡,此时 的转化率为
的转化率为___________ ;化学平衡常数
___________
②
___________ (填“>”“<”或“=”) ;理由
;理由___________
③ 温度下,既能增大反应速率又能提高
温度下,既能增大反应速率又能提高 平䘖转化率的措施有
平䘖转化率的措施有___________ (填一种)。
④恒温恒容时,可以判断反应 达到平衡状态的有
达到平衡状态的有___________ (填标号)。
A.
B.容器内混合气体的压强不再改变
C. 和
和 的转化率的比值保持不变
的转化率的比值保持不变
D.容器内混合气体的平均相对分子质量不变
(1)
 可在一定条件下转化为
可在一定条件下转化为 。已知:
。已知:
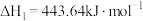

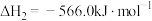
甲醇
 是一种重要的化工原料,也可以直接用作燃料。试写出
是一种重要的化工原料,也可以直接用作燃料。试写出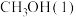 在氧气中完全燃烧生成
在氧气中完全燃烧生成 和
和 的热化学方程式:
的热化学方程式:(2)科研人员研发出一种由强碱溶液作电解质溶液的新型甲醇手机电池,充满电后手机可连续使用一个月,则放电时,甲醇在
(3)
 可在一定条件下转化为
可在一定条件下转化为 。向
。向 密闭容器中通入
密闭容器中通入 和
和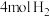 ,在适合的催化剂和
,在适合的催化剂和 温度下,发生反应
温度下,发生反应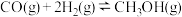
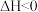 ,保持容器容积一直不变,
,保持容器容积一直不变, 时,反应达到平衡状态,
时,反应达到平衡状态,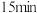 时改变温度为
时改变温度为 ,
, 时反应再次达到平衡状态,部分数据如下表:
时反应再次达到平衡状态,部分数据如下表:| 反应时间 |  | 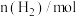 | 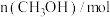 |
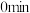 | 2 | 4 | 0 |
 | 1 | ||
 | 0.2 |
 时反应达到平衡,此时
时反应达到平衡,此时 的转化率为
的转化率为
②

 ;理由
;理由③
 温度下,既能增大反应速率又能提高
温度下,既能增大反应速率又能提高 平䘖转化率的措施有
平䘖转化率的措施有④恒温恒容时,可以判断反应
 达到平衡状态的有
达到平衡状态的有A.

B.容器内混合气体的压强不再改变
C.
 和
和 的转化率的比值保持不变
的转化率的比值保持不变 D.容器内混合气体的平均相对分子质量不变
您最近一年使用:0次
名校
9 . 铁及其化合物在生产、生活中有广泛的应用。
(1)中科院兰州化学物理研究所用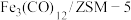 催化
催化 加氢合成低碳烯烃反应,反应过程如图,催化剂中添加助剂
加氢合成低碳烯烃反应,反应过程如图,催化剂中添加助剂 (也起催化作用)后可改变反应的选择性。
(也起催化作用)后可改变反应的选择性。
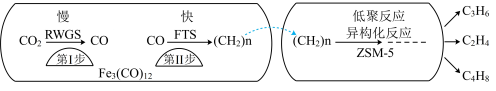
下列说法正确的是___________ 。
a.第1步所发生的反应为: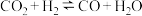
b.第1步反应的活化能低于第2步
c.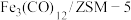 使
使 加氢合成低碳烯烃的
加氢合成低碳烯烃的 减小
减小
d.添加不同助剂后,各反应的平衡常数不变
(2)纳米铁是重要的储氢材料,可用反应 制得。在
制得。在 恒容密闭容器中加入足量铁粉和
恒容密闭容器中加入足量铁粉和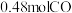 ,在
,在 不同温度下进行反应,测得
不同温度下进行反应,测得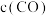 与温度、时间的关系如图所示。
与温度、时间的关系如图所示。
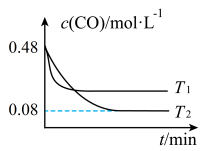

___________ 0(填“>”或“<”);
(3) 温度下,平衡时体系的压强为
温度下,平衡时体系的压强为 ,反应的标准平衡常数
,反应的标准平衡常数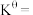
___________ (已知:标准平衡常数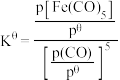 ,其中
,其中 为标准压强
为标准压强 为各组分的平衡分压。)
为各组分的平衡分压。)
(4)高铁酸钾 被称为“绿色化学”净水剂,在酸性至弱碱性条件下不稳定。
被称为“绿色化学”净水剂,在酸性至弱碱性条件下不稳定。
①电解法可制得 ,装置如图,阳极电极反应式为
,装置如图,阳极电极反应式为___________ 。

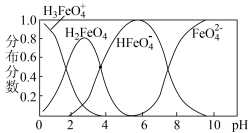
② 在水解过程中铁元素形成的微粒分布分数与
在水解过程中铁元素形成的微粒分布分数与 的关系如图所示,向
的关系如图所示,向 的溶液中加入
的溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为___________ 。
(5)复合氧化物铁酸锰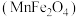 可用于热化学循环分解制氢气,原理如下:
可用于热化学循环分解制氢气,原理如下:
①

②

③

则: 与
与 、
、 的关系为
的关系为
___________
(1)中科院兰州化学物理研究所用
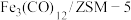 催化
催化 加氢合成低碳烯烃反应,反应过程如图,催化剂中添加助剂
加氢合成低碳烯烃反应,反应过程如图,催化剂中添加助剂 (也起催化作用)后可改变反应的选择性。
(也起催化作用)后可改变反应的选择性。
下列说法正确的是
a.第1步所发生的反应为:
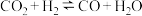
b.第1步反应的活化能低于第2步
c.
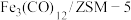 使
使 加氢合成低碳烯烃的
加氢合成低碳烯烃的 减小
减小d.添加不同助剂后,各反应的平衡常数不变
(2)纳米铁是重要的储氢材料,可用反应
 制得。在
制得。在 恒容密闭容器中加入足量铁粉和
恒容密闭容器中加入足量铁粉和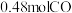 ,在
,在 不同温度下进行反应,测得
不同温度下进行反应,测得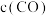 与温度、时间的关系如图所示。
与温度、时间的关系如图所示。

(3)
 温度下,平衡时体系的压强为
温度下,平衡时体系的压强为 ,反应的标准平衡常数
,反应的标准平衡常数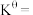
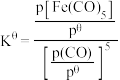 ,其中
,其中 为标准压强
为标准压强 为各组分的平衡分压。)
为各组分的平衡分压。)(4)高铁酸钾
 被称为“绿色化学”净水剂,在酸性至弱碱性条件下不稳定。
被称为“绿色化学”净水剂,在酸性至弱碱性条件下不稳定。①电解法可制得
 ,装置如图,阳极电极反应式为
,装置如图,阳极电极反应式为
②
 在水解过程中铁元素形成的微粒分布分数与
在水解过程中铁元素形成的微粒分布分数与 的关系如图所示,向
的关系如图所示,向 的溶液中加入
的溶液中加入 溶液,发生反应的离子方程式为
溶液,发生反应的离子方程式为
(5)复合氧化物铁酸锰
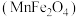 可用于热化学循环分解制氢气,原理如下:
可用于热化学循环分解制氢气,原理如下: ①


②


③


则:
 与
与 、
、 的关系为
的关系为
您最近一年使用:0次
10 . 二氧化碳的回收利用是环保领域研究的热点课题。结合所学知识回答下列问题:
Ⅰ.利用太阳能实现 制取某些物质是一种非常理想的
制取某些物质是一种非常理想的 减排途径。
减排途径。
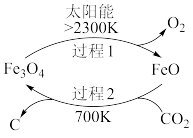
(1)在太阳能的作用下,以 为原料制取炭黑的流程如图所示。其总反应的化学方程式为
为原料制取炭黑的流程如图所示。其总反应的化学方程式为___________ 。
(2)以稀硫酸为电解质溶液,利用太阳能将 转化为低碳烯烃,工作原理如图:
转化为低碳烯烃,工作原理如图:
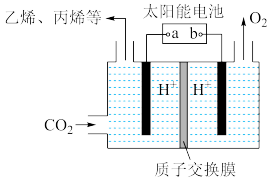
①b是电源的___________ (填“正”或“负”)极。
②生成乙烯( )的电极反应式为
)的电极反应式为___________ 。
③电场作用下,氢离子从___________ (填:“从左到右”或“从右到左”)移动。
Ⅱ.通过化学的方法实现 的资源化利用也是一种非常理想的
的资源化利用也是一种非常理想的 减排途径。
减排途径。
(3)工业上用 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知:
 ;
;
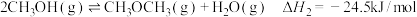 。
。
则 反应的
反应的
___________  。
。
(4)已知该反应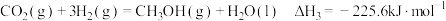 ,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。
,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。
(5)工业上用 和
和 反应合成甲醇
反应合成甲醇
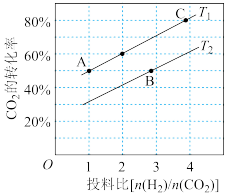
 ,在2L刚性密闭容器中,不同温度、不同投料比时,
,在2L刚性密闭容器中,不同温度、不同投料比时, 的平衡转化率如图所示。
的平衡转化率如图所示。 温度下,将
温度下,将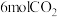 和
和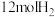 充入该密闭容器中,
充入该密闭容器中, 后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为
后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为___________ ;反应的平衡常数
___________ ,从图中可知:
___________  (填>或<或=,判断的依据是
(填>或<或=,判断的依据是___________ , 、
、 、
、 三者之间的大小关系为
三者之间的大小关系为___________ 。
Ⅰ.利用太阳能实现
 制取某些物质是一种非常理想的
制取某些物质是一种非常理想的 减排途径。
减排途径。(1)在太阳能的作用下,以
 为原料制取炭黑的流程如图所示。其总反应的化学方程式为
为原料制取炭黑的流程如图所示。其总反应的化学方程式为
(2)以稀硫酸为电解质溶液,利用太阳能将
 转化为低碳烯烃,工作原理如图:
转化为低碳烯烃,工作原理如图:
①b是电源的
②生成乙烯(
 )的电极反应式为
)的电极反应式为③电场作用下,氢离子从
Ⅱ.通过化学的方法实现
 的资源化利用也是一种非常理想的
的资源化利用也是一种非常理想的 减排途径。
减排途径。(3)工业上用
 和
和 反应合成二甲醚。已知:
反应合成二甲醚。已知: ;
;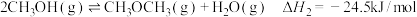 。
。则
 反应的
反应的
 。
。(4)已知该反应
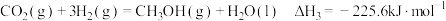 ,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。
,在恒温恒压下进行,以下叙述能说明该反应达到平衡状态的是___________(填序号)。A. 和 和 的物质的量浓度之比是 的物质的量浓度之比是 |
| B.容器中混合气体的平均摩尔质量保持不变 |
| C.容器中混合气体的体积保持不变 |
D. 的消耗速率等于 的消耗速率等于 的生成速率的3倍 的生成速率的3倍 |
(5)工业上用
 和
和 反应合成甲醇
反应合成甲醇 ,在2L刚性密闭容器中,不同温度、不同投料比时,
,在2L刚性密闭容器中,不同温度、不同投料比时, 的平衡转化率如图所示。
的平衡转化率如图所示。 温度下,将
温度下,将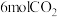 和
和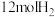 充入该密闭容器中,
充入该密闭容器中, 后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为
后反应达到平衡状态,则0-5min内的用甲醇表示的平均反应速率为

 (填>或<或=,判断的依据是
(填>或<或=,判断的依据是 、
、 、
、 三者之间的大小关系为
三者之间的大小关系为
您最近一年使用:0次



