名校
1 . 氮氧化物是形成酸雨和光化学烟雾的主要物质之一。研究消除氮氧化物的反应机理,对建设生态文明、美丽中国具有重要意义。回答下列问题:
(1)NO2是工业合成硝酸的中间产物,也是一种主要的大气污染物,工业可采用CH4消除NO2污染,主要原理为CH4(g)+2NO2(g) CO2(g)+2H2O(g)+N2(g) △H。
CO2(g)+2H2O(g)+N2(g) △H。
①已知:CH4的燃烧热△H1=-890.3kJ•mol-1
N2(g)+2O2(g)=2NO2(g) △H2=+133kJ•mol-1
H2O(g)=H2O(l) △H3=-44kJ•mol-1
则△H=________ kJ•mol-1。
②在3.0L恒温密闭容器中通入1molCH4和2molNO2,进行上述反应,容器内气体总压强(p)随反应时间(t)变化的数据如表所示:
则0~4min用NO2表示该反应的平均速率v(NO2)=________ mol/(L•min),该温度下的平衡常数Kp=_________ kPa。
(2)N2O曾用作麻醉剂,其分解的方程式为2N2O(g) 2N2(g)+O2(g),分别向四个密闭容器中充入如表所示相应气体,进行上述反应。容器I、II、III中N2O的平衡转化率随温度变化的曲线如图所示:
2N2(g)+O2(g),分别向四个密闭容器中充入如表所示相应气体,进行上述反应。容器I、II、III中N2O的平衡转化率随温度变化的曲线如图所示:
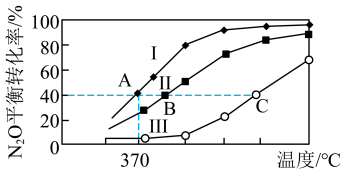
①若容器IV保持370℃,则起始反应速率v正(N2O)_______ 2v逆(O2)(填“>”“<”或“=”)。
②A、B、C三点中压强最大的是_______ 。
③碘蒸气的存在能大幅度提高N2O的分解速率,反应历程如下:
第一步I2(g) 2I(g)(快速平衡,平衡常数为K)
2I(g)(快速平衡,平衡常数为K)
第二步I(g)+N2O(g) N2(g)+IO(g)(慢反应)
N2(g)+IO(g)(慢反应)
第三步2IO(g)+2N2O(g) 2N2(g)+2O2(g)+I2(g)(快反应)
2N2(g)+2O2(g)+I2(g)(快反应)
则第二步的活化能________ (填“>”“<”或“=”)第三步的活化能。
实验表明,碘蒸气存在时N2O分解速率方程v=k•c(N2O)•c0.5(I2)(k为速率常数),已知第二步反应不影响第一步的平衡,其反应速率方程v=k1•c(N2O)•c(I)(k1为速率常数)。则第一步反应的平衡常数K=________ (用k和k1表示)。
(1)NO2是工业合成硝酸的中间产物,也是一种主要的大气污染物,工业可采用CH4消除NO2污染,主要原理为CH4(g)+2NO2(g)
 CO2(g)+2H2O(g)+N2(g) △H。
CO2(g)+2H2O(g)+N2(g) △H。①已知:CH4的燃烧热△H1=-890.3kJ•mol-1
N2(g)+2O2(g)=2NO2(g) △H2=+133kJ•mol-1
H2O(g)=H2O(l) △H3=-44kJ•mol-1
则△H=
②在3.0L恒温密闭容器中通入1molCH4和2molNO2,进行上述反应,容器内气体总压强(p)随反应时间(t)变化的数据如表所示:
| 反应时间t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| 总压强p/×100kPa | 4.80 | 5.44 | 5.76 | 5.92 | 6.00 | 6.00 |
(2)N2O曾用作麻醉剂,其分解的方程式为2N2O(g)
 2N2(g)+O2(g),分别向四个密闭容器中充入如表所示相应气体,进行上述反应。容器I、II、III中N2O的平衡转化率随温度变化的曲线如图所示:
2N2(g)+O2(g),分别向四个密闭容器中充入如表所示相应气体,进行上述反应。容器I、II、III中N2O的平衡转化率随温度变化的曲线如图所示:
| 容器 | 物质的量/mol | |||
| 编号 | 体积/L | N2O | N2 | O2 |
| I | V1=1.0 | 0.1 | 0 | 0 |
| II | V2 | 0.1 | 0 | 0 |
| III | V3 | 0.1 | 0 | 0 |
| IV | V4=1.0 | 0.06 | 0.04 | 0.04 |
②A、B、C三点中压强最大的是
③碘蒸气的存在能大幅度提高N2O的分解速率,反应历程如下:
第一步I2(g)
 2I(g)(快速平衡,平衡常数为K)
2I(g)(快速平衡,平衡常数为K)第二步I(g)+N2O(g)
 N2(g)+IO(g)(慢反应)
N2(g)+IO(g)(慢反应)第三步2IO(g)+2N2O(g)
 2N2(g)+2O2(g)+I2(g)(快反应)
2N2(g)+2O2(g)+I2(g)(快反应)则第二步的活化能
实验表明,碘蒸气存在时N2O分解速率方程v=k•c(N2O)•c0.5(I2)(k为速率常数),已知第二步反应不影响第一步的平衡,其反应速率方程v=k1•c(N2O)•c(I)(k1为速率常数)。则第一步反应的平衡常数K=
您最近一年使用:0次
2023-09-14更新
|
348次组卷
|
4卷引用:湖北省高中名校联盟2024届高三第一次联合测评化学试题
名校
2 . 用 制备
制备 ,既可减少碳排放,又可获得实用的含碳物质,有利于实现“双碳”目标。主要反应为:
,既可减少碳排放,又可获得实用的含碳物质,有利于实现“双碳”目标。主要反应为:
I.

II.
 。
。
回答下列问题:
(1)①25℃,101kPa时,CO的燃烧热为283 ,
, 的燃烧热为286
的燃烧热为286 ;
;
②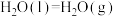
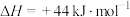 。
。
则
_________  。反应I能自发进行的条件是
。反应I能自发进行的条件是________ (填“高温”或“低温”)。
(2)向某刚性容器中,按投料比 充入
充入 和
和 在不同催化剂(M、N)下发生上述反应。一段时间后,测得
在不同催化剂(M、N)下发生上述反应。一段时间后,测得 的转化率、
的转化率、 的选择性(含碳生成物中
的选择性(含碳生成物中 的百分含量)随温度的变化如图所示。
的百分含量)随温度的变化如图所示。
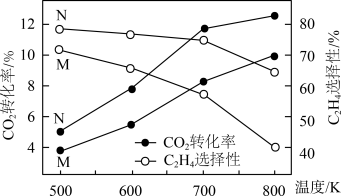
①由图可知,催化效果M___________ N(填“优于”或“劣于”)。
②已知活化能 (看作不受温度影响),反应温度T和速率常数k之间符合公式:
(看作不受温度影响),反应温度T和速率常数k之间符合公式: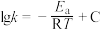 (R和C为常数),下列关于反应Ⅰ在题设条件下的
(R和C为常数),下列关于反应Ⅰ在题设条件下的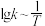 图像与上述两种催化剂关系对应正确的是
图像与上述两种催化剂关系对应正确的是___________ (填标号)。
a.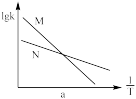 b.
b.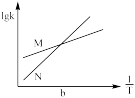 c.
c.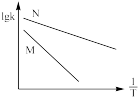 d.
d.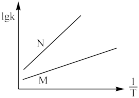
③500~800K之间,乙烯的选择性随温度变化的原因是___________ 。
④能加快制备 的速率且提高
的速率且提高 选择性的措施有
选择性的措施有___________ (填标号)。
A.降低温度 B.增大压强 C.移走 (g) D.更换适宜的催化剂
(g) D.更换适宜的催化剂
(3)T℃时,在恒容容器中加入1molCO(g)、1mol (g)以及催化剂,仅发生反应II。反应后测得各组分的平衡分压:
(g)以及催化剂,仅发生反应II。反应后测得各组分的平衡分压: 和
和 ,则反应的平衡常数
,则反应的平衡常数
_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 制备
制备 ,既可减少碳排放,又可获得实用的含碳物质,有利于实现“双碳”目标。主要反应为:
,既可减少碳排放,又可获得实用的含碳物质,有利于实现“双碳”目标。主要反应为:I.


II.

 。
。回答下列问题:
(1)①25℃,101kPa时,CO的燃烧热为283
 ,
, 的燃烧热为286
的燃烧热为286 ;
;②
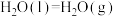
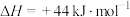 。
。则

 。反应I能自发进行的条件是
。反应I能自发进行的条件是(2)向某刚性容器中,按投料比
 充入
充入 和
和 在不同催化剂(M、N)下发生上述反应。一段时间后,测得
在不同催化剂(M、N)下发生上述反应。一段时间后,测得 的转化率、
的转化率、 的选择性(含碳生成物中
的选择性(含碳生成物中 的百分含量)随温度的变化如图所示。
的百分含量)随温度的变化如图所示。
①由图可知,催化效果M
②已知活化能
 (看作不受温度影响),反应温度T和速率常数k之间符合公式:
(看作不受温度影响),反应温度T和速率常数k之间符合公式: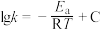 (R和C为常数),下列关于反应Ⅰ在题设条件下的
(R和C为常数),下列关于反应Ⅰ在题设条件下的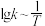 图像与上述两种催化剂关系对应正确的是
图像与上述两种催化剂关系对应正确的是a.
 b.
b. c.
c. d.
d.
③500~800K之间,乙烯的选择性随温度变化的原因是
④能加快制备
 的速率且提高
的速率且提高 选择性的措施有
选择性的措施有A.降低温度 B.增大压强 C.移走
 (g) D.更换适宜的催化剂
(g) D.更换适宜的催化剂(3)T℃时,在恒容容器中加入1molCO(g)、1mol
 (g)以及催化剂,仅发生反应II。反应后测得各组分的平衡分压:
(g)以及催化剂,仅发生反应II。反应后测得各组分的平衡分压: 和
和 ,则反应的平衡常数
,则反应的平衡常数
您最近一年使用:0次
2023-09-08更新
|
255次组卷
|
2卷引用:湖北省孝感市重点高中教科研协作体2023-2024学年高三上学期开学考试化学试题
解题方法
3 . 工业合成氨是人类科学技术的一项重大突破,目前已有三位科学家因其获得诺贝尔奖。工业合成氨生产示意图如图所示。

(1)下列有关合成氨工业的说法正确的是_________
(2)循环利用的Y是氮气和氢气,目的是__________________ 。
(3)在合成氨工业中,要使氨的产率增大,同时又能提高反应速率,可采取的措施有_________ (填编号)。
①使用催化剂 ②恒温恒容,增大原料气 和
和 充入量 ③及时分离产生的
充入量 ③及时分离产生的
④升高温度 ⑤恒温恒容,充入惰性气体 使压强增大
使压强增大
(4)氮的固定和氮的循环是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分 值。
值。
分析数据可知:
①在 下模拟工业固氮,某时刻
下模拟工业固氮,某时刻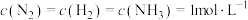 ,此时
,此时
_________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
②人类不适合大规模模拟大气固氮的原因是__________________ 。
(5)为获得合成氨的原料气氢气,某科研小组以太阳能为热源分解 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如下。
的过程如下。
已知: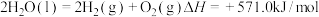 。
。
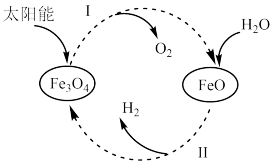
过程Ⅰ: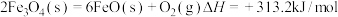
过程Ⅱ:……
过程Ⅱ的热化学方程式为_________ 。

(1)下列有关合成氨工业的说法正确的是_________
| A.工业合成氨的反应是熵减小的放热反应,在低温或常温时可自发进行 |
| B.合成氨反应中,反应物的总键能小于产物的总键能 |
C.合成氨厂一般采用的压强为 ,因为该压强下铁触媒的活性最高 ,因为该压强下铁触媒的活性最高 |
D. 的量越多, 的量越多, 的转化率越大,因此,充入的 的转化率越大,因此,充入的 越多越有利于 越多越有利于 的合成 的合成 |
(3)在合成氨工业中,要使氨的产率增大,同时又能提高反应速率,可采取的措施有
①使用催化剂 ②恒温恒容,增大原料气
 和
和 充入量 ③及时分离产生的
充入量 ③及时分离产生的
④升高温度 ⑤恒温恒容,充入惰性气体
 使压强增大
使压强增大(4)氮的固定和氮的循环是几百年来科学家一直研究的课题。下表列举了不同温度下大气固氮和工业固氮的部分
 值。
值。| 反应 | 大气固氮 | 工业固氮 | |||
温度 | 27 | 2000 | 25 | 400 | 450 |
 |  | 0.1 | 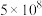 | 0.507 | 0.152 |
①在
 下模拟工业固氮,某时刻
下模拟工业固氮,某时刻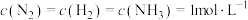 ,此时
,此时
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。②人类不适合大规模模拟大气固氮的原因是
(5)为获得合成氨的原料气氢气,某科研小组以太阳能为热源分解
 ,经热化学铁氧化合物循环分解水制
,经热化学铁氧化合物循环分解水制 的过程如下。
的过程如下。已知:
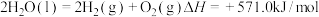 。
。
过程Ⅰ:
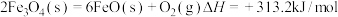
过程Ⅱ:……
过程Ⅱ的热化学方程式为
您最近一年使用:0次
4 . 能源是国民经济发展的重要基础。请根据所学知识回答下列问题:
Ⅰ.在标准状况下,1.68L家用燃料(仅由C、H两种元素组成的某气体)质量为1.2g,在25℃和101kPa下完全燃烧生成 和
和 时,放出66.77kJ的热量。
时,放出66.77kJ的热量。
(1)该气体的分子式为___________ 。该气体的燃烧热
___________ 。(保留一位小数)
Ⅱ.火箭发射时可以用肼( ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。
和水蒸气。
已知:
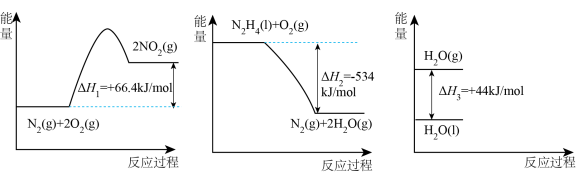
(2)请写出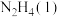 与
与 反应的热化学方程式
反应的热化学方程式___________ 。
(3)32g液态肼与足量 反应生成氮气和液态水时,放出的热量是
反应生成氮气和液态水时,放出的热量是___________ kJ。
(4)上述反应用于火箭推进器的原因:①能快速产生大量气体;②___________ 。
Ⅲ.氢能是一种极具发展潜力的清洁能源。 可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一
可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一
已知:在25℃、101kPa下,
①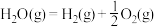
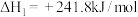
②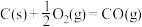
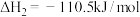
③

(5)25℃、101kPa下,CO与水蒸气反应转化为 和
和 的热化学方程式为
的热化学方程式为___________ 。
Ⅰ.在标准状况下,1.68L家用燃料(仅由C、H两种元素组成的某气体)质量为1.2g,在25℃和101kPa下完全燃烧生成
 和
和 时,放出66.77kJ的热量。
时,放出66.77kJ的热量。(1)该气体的分子式为

Ⅱ.火箭发射时可以用肼(
 ,液态)作燃料,
,液态)作燃料, 作氧化剂,二者反应生成
作氧化剂,二者反应生成 和水蒸气。
和水蒸气。已知:

(2)请写出
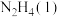 与
与 反应的热化学方程式
反应的热化学方程式(3)32g液态肼与足量
 反应生成氮气和液态水时,放出的热量是
反应生成氮气和液态水时,放出的热量是(4)上述反应用于火箭推进器的原因:①能快速产生大量气体;②
Ⅲ.氢能是一种极具发展潜力的清洁能源。
 可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一
可用CO在高温下与水蒸气反应制得,是目前大规模制取氢气的方法之一已知:在25℃、101kPa下,
①
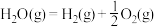
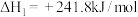
②
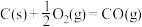
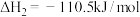
③


(5)25℃、101kPa下,CO与水蒸气反应转化为
 和
和 的热化学方程式为
的热化学方程式为
您最近一年使用:0次
名校
解题方法
5 . 完成下列问题
Ⅰ.氨是重要的化工原料,已知NH3(g)在纯氧中燃烧的能量变化如图。

(1)已知: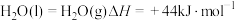 ,则NH3(g)的燃烧热的热化学方程式为
,则NH3(g)的燃烧热的热化学方程式为_______ 。
Ⅱ.火箭推进器中装有肼(N2H4)和过氧化氢。已知下列各物质反应的热化学方程式:
①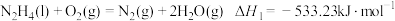
②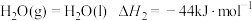
③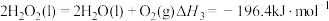
(2)以下选项中,是氮原子激发态的电子排布式,且其中能量较高的是_______ 。(填标号)
a.1s22s22p23s1 b.ls22s22p43d2 c.1s22s12p5 d.1s22s22p13p2
(3)N2H4晶体的晶胞结构_______ (填“是”或者“不”)符合分子密堆积,原因是_______ 。
(4)16g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出热量为:_______ (保留小数点后一位有效数字)。
(5)在高温下,N2H4可完全分解为NH3、N2及H2,实验测得分解产物中N2与H2的物质的量之比为3∶2,则该分解反应的化学方程式为_______ 。
(6)有以下物质:①碘、②金刚砂、③氨气、④氯化钠、⑤水晶、⑥肼,它们的熔点由高到低的顺序为_______ (用序号表示)。
Ⅰ.氨是重要的化工原料,已知NH3(g)在纯氧中燃烧的能量变化如图。

(1)已知:
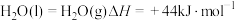 ,则NH3(g)的燃烧热的热化学方程式为
,则NH3(g)的燃烧热的热化学方程式为Ⅱ.火箭推进器中装有肼(N2H4)和过氧化氢。已知下列各物质反应的热化学方程式:
①
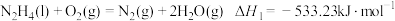
②
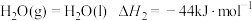
③
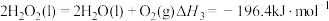
(2)以下选项中,是氮原子激发态的电子排布式,且其中能量较高的是
a.1s22s22p23s1 b.ls22s22p43d2 c.1s22s12p5 d.1s22s22p13p2
(3)N2H4晶体的晶胞结构
(4)16g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出热量为:
(5)在高温下,N2H4可完全分解为NH3、N2及H2,实验测得分解产物中N2与H2的物质的量之比为3∶2,则该分解反应的化学方程式为
(6)有以下物质:①碘、②金刚砂、③氨气、④氯化钠、⑤水晶、⑥肼,它们的熔点由高到低的顺序为
您最近一年使用:0次
6 . 乙醇汽油是一种由粮食及各种植物纤维加工成的燃料乙醇和普通汽油按一定比例混配形成的替代能源。在汽油中加入适量乙醇作为汽车燃料,可节省石油资源,减少汽车尾气对空气的污染,还可促进农业的生产。
(1)已知:①某些常见化学键的键能(常温常压下,1 mol理想气体分子AB断裂为中性气态原子A和B所需要的能量或A、B合成理想气体分子所放出的能量)数据如下:
②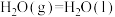
 ;
;
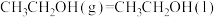
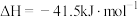 。
。
则表示乙醇燃烧热的热化学方程式为__________ 。
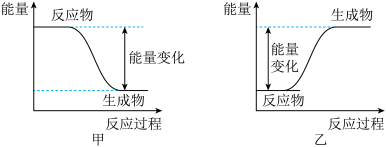
(2)下列能正确表示乙醇燃烧的能量变化图为图__________ (填“甲”或“乙”)。
(3) 加氢也可以制备乙醇,反应的化学方程式为
加氢也可以制备乙醇,反应的化学方程式为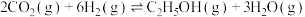 。在一定温度下,将
。在一定温度下,将 和
和 放入2 L恒容密闭容器中,5min时反应达到平衡,此时
放入2 L恒容密闭容器中,5min时反应达到平衡,此时 的体积分数为
的体积分数为 。
。
①下列条件能判断该反应达到化学平衡状态的是______ (填标号)。
a. b.
b. 的消耗速率是
的消耗速率是 的生成速率的3倍
的生成速率的3倍
c.容器中气体的平均摩尔质量不变 d. 的百分含量保持不变
的百分含量保持不变
② 内,
内, 为
为__________  ,
, 为
为__________  。
。
③平衡时, 的转化率为
的转化率为__________  。
。
④平衡时的压强为起始压强的__________ 倍。
(4)汽油的主要成分为 脂肪烃和环烷烃类,以及一定量芳香烃,汽油具有较高的辛烷值(抗爆震燃烧性能),并按辛烷值的高低分为90号、93号、95号、97号等标号。已知辛烷的燃烧热
脂肪烃和环烷烃类,以及一定量芳香烃,汽油具有较高的辛烷值(抗爆震燃烧性能),并按辛烷值的高低分为90号、93号、95号、97号等标号。已知辛烷的燃烧热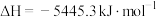 ,则燃烧相同质量的乙醇和辛烷,放热多的是
,则燃烧相同质量的乙醇和辛烷,放热多的是__________ (填名称)。
(1)已知:①某些常见化学键的键能(常温常压下,1 mol理想气体分子AB断裂为中性气态原子A和B所需要的能量或A、B合成理想气体分子所放出的能量)数据如下:
| 化学键 |  | H—O | C—O | C—H |  | C—C |
键能 | 803 | 463 | 351 | 414 | 498 | 348 |
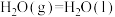
 ;
;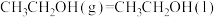
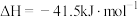 。
。则表示乙醇燃烧热的热化学方程式为
(2)下列能正确表示乙醇燃烧的能量变化图为图

(3)
 加氢也可以制备乙醇,反应的化学方程式为
加氢也可以制备乙醇,反应的化学方程式为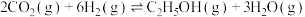 。在一定温度下,将
。在一定温度下,将 和
和 放入2 L恒容密闭容器中,5min时反应达到平衡,此时
放入2 L恒容密闭容器中,5min时反应达到平衡,此时 的体积分数为
的体积分数为 。
。①下列条件能判断该反应达到化学平衡状态的是
a.
 b.
b. 的消耗速率是
的消耗速率是 的生成速率的3倍
的生成速率的3倍c.容器中气体的平均摩尔质量不变 d.
 的百分含量保持不变
的百分含量保持不变②
 内,
内, 为
为 ,
, 为
为 。
。③平衡时,
 的转化率为
的转化率为 。
。④平衡时的压强为起始压强的
(4)汽油的主要成分为
 脂肪烃和环烷烃类,以及一定量芳香烃,汽油具有较高的辛烷值(抗爆震燃烧性能),并按辛烷值的高低分为90号、93号、95号、97号等标号。已知辛烷的燃烧热
脂肪烃和环烷烃类,以及一定量芳香烃,汽油具有较高的辛烷值(抗爆震燃烧性能),并按辛烷值的高低分为90号、93号、95号、97号等标号。已知辛烷的燃烧热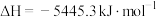 ,则燃烧相同质量的乙醇和辛烷,放热多的是
,则燃烧相同质量的乙醇和辛烷,放热多的是
您最近一年使用:0次
7 . 一定条件下,水气变换反应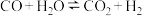 的中间产物是
的中间产物是 。为探究该反应过程,研究
。为探究该反应过程,研究 水溶液在密封石英管中的分解反应:
水溶液在密封石英管中的分解反应:
Ⅰ.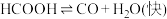
Ⅱ.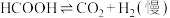
研究发现,在反应Ⅰ、Ⅱ中, 仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
(1)一定条件下,反应Ⅰ、Ⅱ的焓变分别为 、
、 ,则该条件下水气变换反应的焓变
,则该条件下水气变换反应的焓变
_____ (用含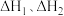 的代数式表示)。
的代数式表示)。
(2)反应Ⅰ正反应速率方程为: ,k为反应速率常数。
,k为反应速率常数。 温度下,
温度下, 电离平衡常数为
电离平衡常数为 ,当
,当 平衡浓度为
平衡浓度为 时,
时, 浓度为
浓度为_____  ,此时反应Ⅰ的反应速率
,此时反应Ⅰ的反应速率
_____  (用含
(用含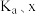 和k的代数式表示)。
和k的代数式表示)。
(3) 温度下,在密封石英管内完全充满
温度下,在密封石英管内完全充满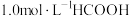 水溶液,使
水溶液,使 分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。
分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。 时刻测得
时刻测得 的浓度分别为
的浓度分别为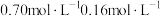 ,反应Ⅱ达平衡时,测得
,反应Ⅱ达平衡时,测得 的浓度为
的浓度为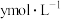 。体系达平衡后
。体系达平衡后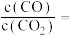
_____ (用含y的代数式表示,下同),反应Ⅱ的平衡常数为_____ 。
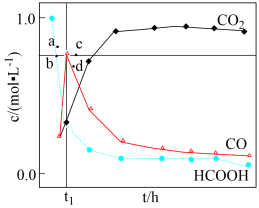
相同条件下,若反应起始时溶液中同时还含有 盐酸,则图示点
盐酸,则图示点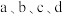 中,
中, 的浓度峰值点可能是
的浓度峰值点可能是_____ (填标号)。与不含盐酸相比, 达浓度峰值时,
达浓度峰值时, 浓度
浓度_____ (填“增大”“减小”或“不变”), 的值
的值_____ (填“增大”“减小”或“不变”)。
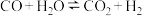 的中间产物是
的中间产物是 。为探究该反应过程,研究
。为探究该反应过程,研究 水溶液在密封石英管中的分解反应:
水溶液在密封石英管中的分解反应:Ⅰ.
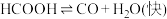
Ⅱ.
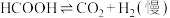
研究发现,在反应Ⅰ、Ⅱ中,
 仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:
仅对反应Ⅰ有催加速作用;反应Ⅰ速率远大于反应Ⅱ,近似认为反应Ⅰ建立平衡后始终处于平衡状态。忽略水电离,其浓度视为常数。回答下列问题:(1)一定条件下,反应Ⅰ、Ⅱ的焓变分别为
 、
、 ,则该条件下水气变换反应的焓变
,则该条件下水气变换反应的焓变
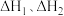 的代数式表示)。
的代数式表示)。(2)反应Ⅰ正反应速率方程为:
 ,k为反应速率常数。
,k为反应速率常数。 温度下,
温度下, 电离平衡常数为
电离平衡常数为 ,当
,当 平衡浓度为
平衡浓度为 时,
时, 浓度为
浓度为 ,此时反应Ⅰ的反应速率
,此时反应Ⅰ的反应速率
 (用含
(用含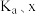 和k的代数式表示)。
和k的代数式表示)。(3)
 温度下,在密封石英管内完全充满
温度下,在密封石英管内完全充满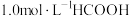 水溶液,使
水溶液,使 分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。
分解,分解产物均完全溶于水。含碳物种浓度与反应时间的变化关系如图所示(忽略碳元素的其他存在形式)。 时刻测得
时刻测得 的浓度分别为
的浓度分别为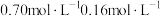 ,反应Ⅱ达平衡时,测得
,反应Ⅱ达平衡时,测得 的浓度为
的浓度为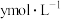 。体系达平衡后
。体系达平衡后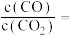

相同条件下,若反应起始时溶液中同时还含有
 盐酸,则图示点
盐酸,则图示点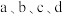 中,
中, 的浓度峰值点可能是
的浓度峰值点可能是 达浓度峰值时,
达浓度峰值时, 浓度
浓度 的值
的值
您最近一年使用:0次
2023-06-19更新
|
10715次组卷
|
10卷引用:湖北省武汉市第二中学2023-2024学年高二上学期10月月考化学试题
湖北省武汉市第二中学2023-2024学年高二上学期10月月考化学试题湖北省武汉市第二中学2023-2024学年高三上学期10月月考化学试题2023年高考山东卷化学真题四川省宜宾市第四中学校2022-2023学年高二下学期6月期末化学试题(已下线)2023年高考山东卷化学真题变式题(原理综合题)(已下线)专题17 原理综合题(已下线)专题17 原理综合题(已下线)第20练 化学反应原理综合题 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)(已下线)专题04 电离平衡 水的电离和溶液的pH-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)
8 . 聚苯乙烯是一类重要的高分子材料,可通过苯乙烯聚合制得。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①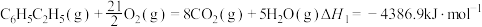
②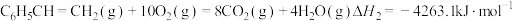
③
计算反应④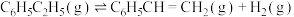 的
的
_______  ;
;
(2)在某温度、 下,向反应器中充入
下,向反应器中充入 气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入
气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入_______  水蒸气作为稀释气(计算时忽略副反应);
水蒸气作为稀释气(计算时忽略副反应);
(3)在 、
、 下,以水蒸气作稀释气。
下,以水蒸气作稀释气。 作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
⑤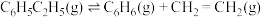
⑥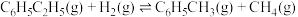
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S( )随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是
)随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是_______ ,理由是_______ ; 的描述错误的是_______;
的描述错误的是_______;
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某 (Ⅰ)的配合物促进
(Ⅰ)的配合物促进 (引发剂,X表示卤素)生成自由基
(引发剂,X表示卤素)生成自由基 ,实现苯乙烯可控聚合。
,实现苯乙烯可控聚合。
(5)引发剂 中活性最高的是
中活性最高的是_______ ;
(6)室温下,① 在配体L的水溶液中形成
在配体L的水溶液中形成 ,其反应平衡常数为K;②
,其反应平衡常数为K;② 在水中的溶度积常数为
在水中的溶度积常数为 。由此可知,
。由此可知, 在配体L的水溶液中溶解反应的平衡常数为
在配体L的水溶液中溶解反应的平衡常数为_______ (所有方程式中计量系数关系均为最简整数比)。
Ⅰ.苯乙烯的制备
(1)已知下列反应的热化学方程式:
①
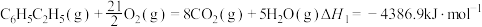
②
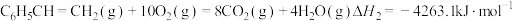
③

计算反应④
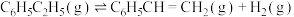 的
的
 ;
;(2)在某温度、
 下,向反应器中充入
下,向反应器中充入 气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入
气态乙苯发生反应④,其平衡转化率为50%,欲将平衡转化率提高至75%,需要向反应器中充入 水蒸气作为稀释气(计算时忽略副反应);
水蒸气作为稀释气(计算时忽略副反应);(3)在
 、
、 下,以水蒸气作稀释气。
下,以水蒸气作稀释气。 作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:
作催化剂,乙苯除脱氢生成苯乙烯外,还会发生如下两个副反应:⑤
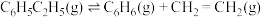
⑥
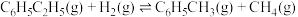
以上反应体系中,芳香烃产物苯乙烯、苯和甲苯的选择性S(
 )随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是
)随乙苯转化率的变化曲线如图所示,其中曲线b代表的产物是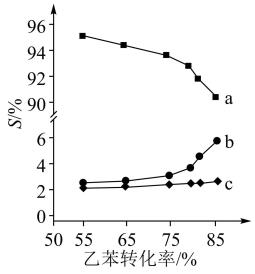
 的描述错误的是_______;
的描述错误的是_______;A.X射线衍射技术可测定 晶体结构 晶体结构 |
B. 可改变乙苯平衡转化率 可改变乙苯平衡转化率 |
C. 降低了乙苯脱氢反应的活化能 降低了乙苯脱氢反应的活化能 |
D.改变 颗粒大小不影响反应速率 颗粒大小不影响反应速率 |
Ⅱ.苯乙烯的聚合
苯乙烯聚合有多种方法,其中一种方法的关键步骤是某
 (Ⅰ)的配合物促进
(Ⅰ)的配合物促进 (引发剂,X表示卤素)生成自由基
(引发剂,X表示卤素)生成自由基 ,实现苯乙烯可控聚合。
,实现苯乙烯可控聚合。(5)引发剂
 中活性最高的是
中活性最高的是(6)室温下,①
 在配体L的水溶液中形成
在配体L的水溶液中形成 ,其反应平衡常数为K;②
,其反应平衡常数为K;② 在水中的溶度积常数为
在水中的溶度积常数为 。由此可知,
。由此可知, 在配体L的水溶液中溶解反应的平衡常数为
在配体L的水溶液中溶解反应的平衡常数为
您最近一年使用:0次
2023-06-16更新
|
7678次组卷
|
9卷引用:湖北省沙市中学2023-2024学年高三下学期3月月考化学试题
湖北省沙市中学2023-2024学年高三下学期3月月考化学试题2023年高考湖南卷化学真题(已下线)专题17 原理综合题(已下线)2023年湖南卷高考真题变式题(原理综合题)(已下线)专题14 化学反应原理综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题15 化学反应原理综合题-2023年高考化学真题题源解密(全国通用)湖南省长沙市麓山国际实验学校2023-2024学年高三上学期第一次月考化学试题 浙江省义乌中学2024届高三上学期首考适应性考试化学试题(已下线)压轴题13 化学反应原理综合题(方法总结+题型密押+压轴题速练)-2024年高考化学压轴题专项训练(浙江专用)
解题方法
9 . 硫及其化合物之间的转化具有重要意义。回答下列问题:
(1) 分子可形成单斜硫和斜方硫,其转化过程为
分子可形成单斜硫和斜方硫,其转化过程为 ,这是一个正反应放热的可逆反应。则
,这是一个正反应放热的可逆反应。则 、
、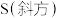 相比,较稳定的是
相比,较稳定的是___________ [填“ ”或“
”或“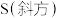 ”]。
”]。
(2)硫酸工业的一步重要反应是 的催化氧化
的催化氧化 。向一恒压密闭容器中充入一定量的
。向一恒压密闭容器中充入一定量的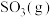 发生上述反应,能判断反应已达平衡状态的叙述是___________(填标号)。
发生上述反应,能判断反应已达平衡状态的叙述是___________(填标号)。
(3)某实验小组通过铁块与稀硫酸反应的实验,研究化学反应速率的影响因素,并绘制出如下图示:
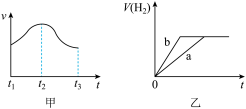
①图甲中, 到
到 速率明显加快的主要原因是
速率明显加快的主要原因是___________ 。
②图乙中,曲线a为铁块与足量稀硫酸反应生成 的体积随时间变化关系。能将曲线a转化为b的实验措施有
的体积随时间变化关系。能将曲线a转化为b的实验措施有___________ (填标号)。
A.将铁块换成铁粉
B.加 固体
固体
C.加 固体
固体
D.将稀硫酸换成98%的硫酸溶液
E.滴入几滴硫酸铜溶液
(4)硫氧化菌电池在废水处理和新能源开发域有广阔的应用前景,其工作原理如图所示。
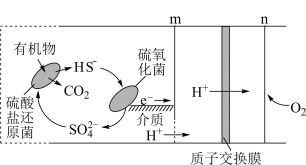
① 在硫氧化菌作用下转化为
在硫氧化菌作用下转化为 的电极反应式为
的电极反应式为___________ 。
②处理0.05mol 时,从质子交换膜左侧迁移至右侧的
时,从质子交换膜左侧迁移至右侧的
___________ mol。
(5)将 与空气的混合气体通入到
与空气的混合气体通入到 、
、 和
和 的混合溶液中,转化过程如图所示:
的混合溶液中,转化过程如图所示:
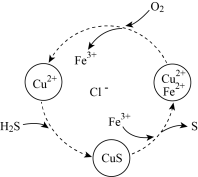
总过程的化学方程式为___________ 。
(1)
 分子可形成单斜硫和斜方硫,其转化过程为
分子可形成单斜硫和斜方硫,其转化过程为 ,这是一个正反应放热的可逆反应。则
,这是一个正反应放热的可逆反应。则 、
、 相比,较稳定的是
相比,较稳定的是 ”或“
”或“ ”]。
”]。(2)硫酸工业的一步重要反应是
 的催化氧化
的催化氧化 。向一恒压密闭容器中充入一定量的
。向一恒压密闭容器中充入一定量的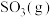 发生上述反应,能判断反应已达平衡状态的叙述是___________(填标号)。
发生上述反应,能判断反应已达平衡状态的叙述是___________(填标号)。| A.混合气体的密度不再改变 |
B.混合气体中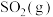 和 和 的分压之比不再改变 的分压之比不再改变 |
C. |
| D.混合气体的平均相对分子质量不再改变 |

①图甲中,
 到
到 速率明显加快的主要原因是
速率明显加快的主要原因是②图乙中,曲线a为铁块与足量稀硫酸反应生成
 的体积随时间变化关系。能将曲线a转化为b的实验措施有
的体积随时间变化关系。能将曲线a转化为b的实验措施有A.将铁块换成铁粉
B.加
 固体
固体C.加
 固体
固体D.将稀硫酸换成98%的硫酸溶液
E.滴入几滴硫酸铜溶液
(4)硫氧化菌电池在废水处理和新能源开发域有广阔的应用前景,其工作原理如图所示。

①
 在硫氧化菌作用下转化为
在硫氧化菌作用下转化为 的电极反应式为
的电极反应式为②处理0.05mol
 时,从质子交换膜左侧迁移至右侧的
时,从质子交换膜左侧迁移至右侧的
(5)将
 与空气的混合气体通入到
与空气的混合气体通入到 、
、 和
和 的混合溶液中,转化过程如图所示:
的混合溶液中,转化过程如图所示:
总过程的化学方程式为
您最近一年使用:0次
10 . 石油化工、煤气化等行业废气普遍含有 ,需要回收处理并加以利用。回答下列问题:
,需要回收处理并加以利用。回答下列问题:
已知:反应Ⅰ: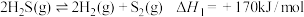
反应II: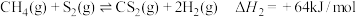
反应Ⅲ: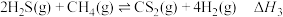
(1)
___________ 。
(2)在总压强为 条件下,
条件下,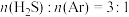 的混合气在不同温度下发生反应I,反应相同时间后测得
的混合气在不同温度下发生反应I,反应相同时间后测得 的体积分数及
的体积分数及 在不同温度下的平衡体积分数如下图所示:
在不同温度下的平衡体积分数如下图所示:

①从平衡移动的角度判断,通入Ar稀释的目的是___________ 。
②图中表示平衡状态的曲线为___________ (填“a”或“b”)。某温度下,平衡时 的体积分数为20%,则该反应的平衡常数
的体积分数为20%,则该反应的平衡常数
___________  。
。
(3)按体积比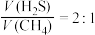 投料,压强恒定,在不同温度下反应相同时间后测得
投料,压强恒定,在不同温度下反应相同时间后测得 和
和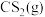 的体积分数如下表:
的体积分数如下表:
试解释在950~1150℃内(其他条件不变),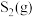 的体积分数随温度升高先增大后减小的原因是
的体积分数随温度升高先增大后减小的原因是___________ 。
(4) 可用于处理工业废水中的重金属离子(如:
可用于处理工业废水中的重金属离子(如: 、
、 、
、 等)
等)
已知反应IV: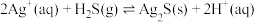
①温度为T时,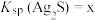 ,则
,则 饱和溶液中
饱和溶液中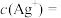
___________ 。
②下列关于反应IV及相关物质的说法正确的是___________ 。
A.纯银器表面生成 属于电化学腐蚀
属于电化学腐蚀
B.将 从反应IV体系中及时分离出去有利于该反应平衡右移
从反应IV体系中及时分离出去有利于该反应平衡右移
C.适当增大压强有利于反应IV平衡右移
D.反应IV能够自发进行说明该反应
 ,需要回收处理并加以利用。回答下列问题:
,需要回收处理并加以利用。回答下列问题:已知:反应Ⅰ:
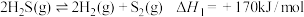
反应II:
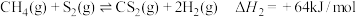
反应Ⅲ:
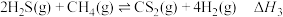
(1)

(2)在总压强为
 条件下,
条件下,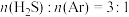 的混合气在不同温度下发生反应I,反应相同时间后测得
的混合气在不同温度下发生反应I,反应相同时间后测得 的体积分数及
的体积分数及 在不同温度下的平衡体积分数如下图所示:
在不同温度下的平衡体积分数如下图所示:
①从平衡移动的角度判断,通入Ar稀释的目的是
②图中表示平衡状态的曲线为
 的体积分数为20%,则该反应的平衡常数
的体积分数为20%,则该反应的平衡常数
 。
。(3)按体积比
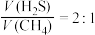 投料,压强恒定,在不同温度下反应相同时间后测得
投料,压强恒定,在不同温度下反应相同时间后测得 和
和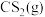 的体积分数如下表:
的体积分数如下表:| 温度/℃ | 950 | 1000 | 1050 | 1100 | 1150 |
 的体积分数/% 的体积分数/% | 0.5 | 1.5 | 3.6 | 5.5 | 8.5 |
 的体积分数/% 的体积分数/% | 0.0 | 0.0 | 0.1 | 0.4 | 1.8 |
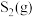 的体积分数随温度升高先增大后减小的原因是
的体积分数随温度升高先增大后减小的原因是(4)
 可用于处理工业废水中的重金属离子(如:
可用于处理工业废水中的重金属离子(如: 、
、 、
、 等)
等)已知反应IV:
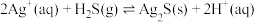
①温度为T时,
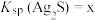 ,则
,则 饱和溶液中
饱和溶液中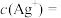
②下列关于反应IV及相关物质的说法正确的是
A.纯银器表面生成
 属于电化学腐蚀
属于电化学腐蚀B.将
 从反应IV体系中及时分离出去有利于该反应平衡右移
从反应IV体系中及时分离出去有利于该反应平衡右移C.适当增大压强有利于反应IV平衡右移
D.反应IV能够自发进行说明该反应

您最近一年使用:0次



