解题方法
1 . 回答下列问题:
(1)已知: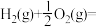
 ,
,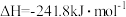
 ,
,
写出焦炭与水蒸气反应的热化学方程式_______ 。
(2)氢化亚铜( )是一种难溶物质,用
)是一种难溶物质,用 溶液和“另一物质”在40~50℃时反应可生成氢化亚铜。
溶液和“另一物质”在40~50℃时反应可生成氢化亚铜。 不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;
不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;  在酸性条件下发生反应:
在酸性条件下发生反应: 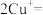
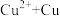 。根据以上信息,结合自己所掌握的化学知识,回答下列问题:
。根据以上信息,结合自己所掌握的化学知识,回答下列问题:
①用 溶液和“另一物质”制
溶液和“另一物质”制 的反应中,用氧化还原观点分析,“另一物质”在反应中作
的反应中,用氧化还原观点分析,“另一物质”在反应中作_______ (填“氧化剂”或“还原剂”)。
② 写出 在氯气中燃烧的化学方程式:
在氯气中燃烧的化学方程式:_______ 。
③ 溶解在稀盐酸中生成的气体是
溶解在稀盐酸中生成的气体是_______ (填化学式)。
④ 如果把 溶解在足量的稀硝酸中,生成的气体只有
溶解在足量的稀硝酸中,生成的气体只有 ,请写出
,请写出 溶解在足量稀硝酸中反应的离子方程式:
溶解在足量稀硝酸中反应的离子方程式:_______ 。
(1)已知:
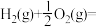
 ,
,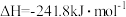
 ,
,
写出焦炭与水蒸气反应的热化学方程式
(2)氢化亚铜(
 )是一种难溶物质,用
)是一种难溶物质,用 溶液和“另一物质”在40~50℃时反应可生成氢化亚铜。
溶液和“另一物质”在40~50℃时反应可生成氢化亚铜。 不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;
不稳定,易分解;在氯气中能燃烧;与稀盐酸反应能生成气体;  在酸性条件下发生反应:
在酸性条件下发生反应: 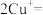
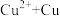 。根据以上信息,结合自己所掌握的化学知识,回答下列问题:
。根据以上信息,结合自己所掌握的化学知识,回答下列问题:①用
 溶液和“另一物质”制
溶液和“另一物质”制 的反应中,用氧化还原观点分析,“另一物质”在反应中作
的反应中,用氧化还原观点分析,“另一物质”在反应中作② 写出
 在氯气中燃烧的化学方程式:
在氯气中燃烧的化学方程式:③
 溶解在稀盐酸中生成的气体是
溶解在稀盐酸中生成的气体是④ 如果把
 溶解在足量的稀硝酸中,生成的气体只有
溶解在足量的稀硝酸中,生成的气体只有 ,请写出
,请写出 溶解在足量稀硝酸中反应的离子方程式:
溶解在足量稀硝酸中反应的离子方程式:
您最近一年使用:0次
2 . NH3和联氨(N2H4)是两种重要的氮氢化合物,在科研和生产中应用广泛。
(1)①已知:
注:拆开气态物质中 1 mol 某种共价键需要吸收的能量,就是该共价键的键能。
N2(g)+3H2(g) 2NH3(g) ∆H=
2NH3(g) ∆H=__________ kJ/mol
②联氨(N2H4)和N2O4 可作为火箭推进剂。
已知:N2(g)+2O2(g)=N2O4(g) ∆H=10.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) ∆H=-543kJ/mol
N2H4(g)和N2O4(g)反应生成 N2(g)和H2O(g)的热化学方程式为_______ 。
(2)一定温度下,向恒容的密闭容器中充入N2 和H2 发生反应:N2+3H2 2NH3,测得各组分浓度随时间变化如图所示。
2NH3,测得各组分浓度随时间变化如图所示。
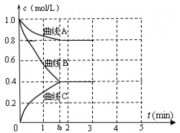
①表示c(N2)的曲线是_______ 。(填“曲线 A”、“曲线B”或“曲线C”)
②0~t0时,v(H2)=_______ mol·L-1·min-1。
③下列措施不能使该反应速率加快的是_______ 。
a.升高温度 b.降低压强 c.使用催化剂
④下列能说明该反应达到平衡的是_______ 。
a.混合气体的压强不再变化 b.2c(H2)= 3c(NH3) c.混合气体的质量不再变化
(1)①已知:
| 共价键 | 键能/ kJ·mol-1 |
| H-H | 436 |
| N≡N | 946 |
| N-H | 391 |
注:拆开气态物质中 1 mol 某种共价键需要吸收的能量,就是该共价键的键能。
N2(g)+3H2(g)
 2NH3(g) ∆H=
2NH3(g) ∆H=②联氨(N2H4)和N2O4 可作为火箭推进剂。
已知:N2(g)+2O2(g)=N2O4(g) ∆H=10.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) ∆H=-543kJ/mol
N2H4(g)和N2O4(g)反应生成 N2(g)和H2O(g)的热化学方程式为
(2)一定温度下,向恒容的密闭容器中充入N2 和H2 发生反应:N2+3H2
 2NH3,测得各组分浓度随时间变化如图所示。
2NH3,测得各组分浓度随时间变化如图所示。
①表示c(N2)的曲线是
②0~t0时,v(H2)=
③下列措施不能使该反应速率加快的是
a.升高温度 b.降低压强 c.使用催化剂
④下列能说明该反应达到平衡的是
a.混合气体的压强不再变化 b.2c(H2)= 3c(NH3) c.混合气体的质量不再变化
您最近一年使用:0次
名校
解题方法
3 . 在二氧化碳加氢制甲烷的反应体系中,主要发生反应的热化学方程式为
反应I:CO2(g)+4H2(g)=CH4(g)+2H2O(g)ΔH=-164.7kJ·mol-1
反应II:CO2(g)+H2(g)=CO(g)+H2O(g)ΔH=41.2kJ·mol-1
反应III:2CO(g)+2H2(g)=CO2(g)+CH4(g)ΔH=-247.1kJ·mol-1
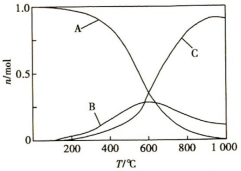
向恒压、密闭容器中通入lmolCO2和4molH2,平衡时CH4、CO、CO2的物质的量随温度的变化如图所示,下列说法不正确的是
反应I:CO2(g)+4H2(g)=CH4(g)+2H2O(g)ΔH=-164.7kJ·mol-1
反应II:CO2(g)+H2(g)=CO(g)+H2O(g)ΔH=41.2kJ·mol-1
反应III:2CO(g)+2H2(g)=CO2(g)+CH4(g)ΔH=-247.1kJ·mol-1
向恒压、密闭容器中通入lmolCO2和4molH2,平衡时CH4、CO、CO2的物质的量随温度的变化如图所示,下列说法不正确的是

| A.图中曲线A表示CO2的物质的量随温度的变化 |
| B.图中曲线B表示CH4的物质的量随温度的变化 |
| C.图中曲线C表示CO的物质的量随温度的变化 |
| D.CH4(g)+H2O(g)=CO(g)+3H2(g)的ΔH=-205.9kJ·mol-1 |
您最近一年使用:0次
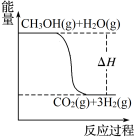
4 . 下列说法正确的是

| A.红热的C 与H2O 蒸气反应制取水煤气是放热反应 |
| B.反应物的总能量低于生成物的总能量时,一定不能发生反应 |
| C.同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照或点燃的条件下的 ΔH 相同 |
| D.由图可知:CH3OH(g)+H2O(g)=CO2(g)+3H2(g) ΔH>0 |
您最近一年使用:0次
名校
解题方法
5 . 氢能是最具前景的清洁能源之一,目前水分解制氢技术及贮氢材料的开发应用都取得了很大进展。已知:2H2(g)+ O2(g)=2H2O(1)∆H=-571.6kJ·mol-1。下列说法错误的是
| A.1mol H2O(l)分解制得1molH2需要吸收571.6kJ的能量 |
| B.氢气作为新能源具有热值高、无污染、资源丰富、可再生等优点 |
| C.贮氢材料具有能大量、快速和高效率地吸收和释放氢气的特点 |
| D.利用太阳能光催化分解水制氢是一种理想的制氢手段 |
您最近一年使用:0次
2021-03-09更新
|
272次组卷
|
3卷引用:江苏省沭阳县修远中学2020-2021学年高一下学期第一次月考化学试题
江苏省沭阳县修远中学2020-2021学年高一下学期第一次月考化学试题(已下线)6.2.2 燃料燃烧释放的能量 氢燃料的应用前景(练习)-2020-2021学年下学期高一化学同步精品课堂(苏教版2019必修第二册)江苏省淮安市涟水县第一中学2021-2022学年高一下学期第一次阶段检测化学试题



