名校
1 . CH4-CO2催化重整是减少温室气体排放的重要途径。回答下列问题:
(1)已知:C(s)+2H2(g)=CH4(g)△H=-75kJ·mol-1
C(s)+O2(g)=CO2(g)△H=-394kJ·mol-1
C(s)+ O2(g)=CO(g)△H=-111kJ·mol-1
O2(g)=CO(g)△H=-111kJ·mol-1
则催化重整反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的△H=
2CO(g)+2H2(g)的△H=____ kJ·mol-1。
若在恒容的密闭容器中,充入1molCH4和1molCO2,发生催化重整反应,下列选项中不能说明该反应已经达到平衡状态的是____ (填标号)。
A.CH4和CO2的物质的量不变B.混合气体的密度保持不变
C.混合气体的压强保持不变D.2v(CH4)正=v(CO2)逆
(2)催化重整时催化剂的活性随积碳的增多而减弱,有关积碳反应和消碳反应的数据如表:
①由表中数据分析:从有利于催化重整的角度考虑,应选用的催化剂为____ (填“X”或“Y”);催化剂可以改变同一化学反应的____ (填“活化能”或“反应热”,下同),但不能改变其____ 。
②化学反应速率与反应物浓度的关系式称为速率方程,是通过实验测定的。在一定温度下,测得某催化剂上沉积碳的生成速率方程为v=k•p(CH4)•[p(CO2)]-0.5,k为速率常数,与温度有关。下列说法错误的是_____ 。
A.增大反应物浓度,k增大导致反应速率加快
B.温度升高,k的数值增大
C.沉积碳的生成速率v与p(CO2)成反比
D.增大CH4的浓度2倍,反应速率加快2倍
(1)已知:C(s)+2H2(g)=CH4(g)△H=-75kJ·mol-1
C(s)+O2(g)=CO2(g)△H=-394kJ·mol-1
C(s)+
 O2(g)=CO(g)△H=-111kJ·mol-1
O2(g)=CO(g)△H=-111kJ·mol-1则催化重整反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的△H=
2CO(g)+2H2(g)的△H=若在恒容的密闭容器中,充入1molCH4和1molCO2,发生催化重整反应,下列选项中不能说明该反应已经达到平衡状态的是
A.CH4和CO2的物质的量不变B.混合气体的密度保持不变
C.混合气体的压强保持不变D.2v(CH4)正=v(CO2)逆
(2)催化重整时催化剂的活性随积碳的增多而减弱,有关积碳反应和消碳反应的数据如表:
| 积碳反应/消碳反应 | 催化剂 | 活化能/(kJ·mol-1) |
| CH4(g)=C(s)+2H2(g)△H=+75kJ·mol-1 | X | 33 |
| Y | 43 | |
| CO2(g)+C(s)=2CO(g)△H=+172kJ·mol-1 | X | 91 |
| Y | 72 |
②化学反应速率与反应物浓度的关系式称为速率方程,是通过实验测定的。在一定温度下,测得某催化剂上沉积碳的生成速率方程为v=k•p(CH4)•[p(CO2)]-0.5,k为速率常数,与温度有关。下列说法错误的是
A.增大反应物浓度,k增大导致反应速率加快
B.温度升高,k的数值增大
C.沉积碳的生成速率v与p(CO2)成反比
D.增大CH4的浓度2倍,反应速率加快2倍
您最近一年使用:0次
名校
解题方法
2 . 在如图所示的恒温、恒压密闭容器中加入2 mol X和2 mol Y,发生如下反应并达到平衡(X、Y状态未知):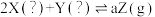 。起始时容器的体积为V L,达到平衡时X、Y、Z的物质的量之比为1:3:2,且容器的体积仍然为V L。请回答下列问题:
。起始时容器的体积为V L,达到平衡时X、Y、Z的物质的量之比为1:3:2,且容器的体积仍然为V L。请回答下列问题:

(1)a=_______ 。
(2)平衡时Y的转化率=_______ 。
(3)X的状态为_______ (填“气态”或“非气态”)。
(4)下列叙述中,能说明上述反应达到平衡状态的是_______ (填标号)。
a.气体密度不变
b.单位时间内消耗2 mol X,同时生成a mol Z
c.Y的转化率不再变化
d.Z的浓度不再变化
(5)已知:
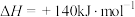

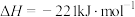
写出 和焦炭、氯气反应生成液态
和焦炭、氯气反应生成液态 和CO气体的热化学方程式:
和CO气体的热化学方程式:_______ 。
(6)依据下表信息,要精制含少量 杂质的
杂质的 ,可采用
,可采用_______ 方法。
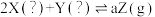 。起始时容器的体积为V L,达到平衡时X、Y、Z的物质的量之比为1:3:2,且容器的体积仍然为V L。请回答下列问题:
。起始时容器的体积为V L,达到平衡时X、Y、Z的物质的量之比为1:3:2,且容器的体积仍然为V L。请回答下列问题:
(1)a=
(2)平衡时Y的转化率=
(3)X的状态为
(4)下列叙述中,能说明上述反应达到平衡状态的是
a.气体密度不变
b.单位时间内消耗2 mol X,同时生成a mol Z
c.Y的转化率不再变化
d.Z的浓度不再变化
(5)已知:

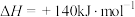

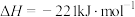
写出
 和焦炭、氯气反应生成液态
和焦炭、氯气反应生成液态 和CO气体的热化学方程式:
和CO气体的热化学方程式:(6)依据下表信息,要精制含少量
 杂质的
杂质的 ,可采用
,可采用 |  | |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
您最近一年使用:0次
名校
解题方法
3 . 源开发和利用是科学研究的热点课题。
(1)几个有关CO的热化学方程式如下:
I.CO(g)+2H2(g)⇌CH3OH(g) ∆H1
II.2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ∆H2
III.CO(g)+H2O(g)⇌CO2(g)+H2(g) ∆H3
则3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g) ∆H=_______ (用含∆H1、∆H2、∆H3的代数表示)。
(2)在1L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ∆H,测得CH3OH的浓度与温度的关系如图所示:
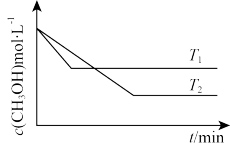
则T1_______ T2;∆H_______ 0(填“>”“<”或“=”)。
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g)⇌CH3OH(g) ∆H=-91.0kJ·mol-1,向1L的恒容密容器中加入0.1molH2和0.05molCO在一定温度下发生上述反应,10min后反应达到平衡状态,测得放出的热量为3.64kJ。
①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为_______ 。
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01molH2和0.05molCH3OH(g)时,平衡_______ (填“向左移动”、“向右移动”或“不移动”)。
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H=-49.5kJ·mol-1
II.CO(g)+2H2(g)⇌CH3OH(g) ∆H2=-90.4kJ·mol-1
III.CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H3
一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的浓度为_______ mol·L-1(用含a、b、V的代数式表示,下同),反应III的平衡常数为_______ 。
(1)几个有关CO的热化学方程式如下:
I.CO(g)+2H2(g)⇌CH3OH(g) ∆H1
II.2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ∆H2
III.CO(g)+H2O(g)⇌CO2(g)+H2(g) ∆H3
则3CO(g)+3H2(g)⇌CH3OCH3(g)+CO2(g) ∆H=
(2)在1L恒容密闭容器中充入一定量CH3OH发生反应:2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ∆H,测得CH3OH的浓度与温度的关系如图所示:

则T1
(3)工业上,利用水煤气合成CH3OH的反应表示如下:2H2(g)+CO(g)⇌CH3OH(g) ∆H=-91.0kJ·mol-1,向1L的恒容密容器中加入0.1molH2和0.05molCO在一定温度下发生上述反应,10min后反应达到平衡状态,测得放出的热量为3.64kJ。
①从反应开始恰好平衡状态时,H2的平均反应速率v(H2)为
②在温度不变条件下,上述反应达到平衡后再向容器中充入0.01molH2和0.05molCH3OH(g)时,平衡
(4)探究CH3OH合成反应化学平衡的影响因素,有利于提高CH3OH的产率。以CO2、H2为原料合成CH3OH涉及的主要反应如下:
I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H=-49.5kJ·mol-1
II.CO(g)+2H2(g)⇌CH3OH(g) ∆H2=-90.4kJ·mol-1
III.CO2(g)+H2(g)⇌CO(g)+H2O(g) ∆H3
一定条件下,向体积为VL的恒容密闭容器中通入1molCO2和3molH2发生上述反应,达到平衡时,容器中CH3OH(g)为amol,CO为bmol,此时H2O(g)的浓度为
您最近一年使用:0次
名校
解题方法
4 . 氧化亚铜常用于制船底防污漆。用CuO与Cu高温烧结可制取Cu2O。已知反应:
2Cu(s)+O2(g)=2CuO(s) ΔH=−314kJ·mol−1
2Cu2O(s)+O2(g)=4CuO(s) ΔH=−292kJ·mol−1
则CuO(s)+Cu(s)=Cu2O(s)的ΔH等于
2Cu(s)+O2(g)=2CuO(s) ΔH=−314kJ·mol−1
2Cu2O(s)+O2(g)=4CuO(s) ΔH=−292kJ·mol−1
则CuO(s)+Cu(s)=Cu2O(s)的ΔH等于
| A.−11kJ·mol−1 | B.+11kJ·mol−1 | C.+22kJ·mol−1 | D.−22kJ·mol−1 |
您最近一年使用:0次
2021-07-15更新
|
1379次组卷
|
22卷引用:湖南省长沙市周南中学2020-2021学年高一年级下学期期末考试化学试题
湖南省长沙市周南中学2020-2021学年高一年级下学期期末考试化学试题海南省北京师范大学万宁附中2020-2021学年高一下学期期中考试化学试题安徽省阜阳市第三中学2018-2019学年高一下学期期末考试化学试题安徽省合肥新城高升学校2021-2022学年高二上学期第一次月考化学试题海南省屯昌县屯昌中学2021-2022学年高二上学期10月月考化学试题云南省昭通市镇雄县第四中学2021-2022学年高二上学期第一次月考化学试题山东省济宁市微山县第二中学2021-2022学年高二上学期第一学段考试化学试题北京市第一五九中学2021-2022学年高二上学期期中考试化学试题【区级联考】北京市东城区2018-2019学年高二上学期期末检测化学试题内蒙古通辽市科左后旗甘旗卡第二高级中学2020届高三12月月考化学试题安徽省亳州市第二中学2020届高三上学期第五次月考化学试题海南省海口市灵山中学2020-2021学年高二上学期期中考试化学试题广西钦州市2021-2022学年高二上学期期末考试化学试题浙江省宁波市奉化区2021-2022学年高二上学期期末联考化学试题新疆叶城县第八中学2021-2022学年高二上学期期末考试化学(理)试题 吉林省长春市北师大附属学校2021-2022学年高二上学期期末考试化学试题天津市和平区2022-2023学年高二上学期期末质量调查化学试卷天津市和平区2022-2023学年高二上学期期末质量检测化学试题 吉林省长春市实验中学2022-2023学年高二上学期期末考试化学试题北京汇文中学2022-2023学年高二下学期期中考试化学试题河南省信阳高级中学2023-2024学年高二上学期开学考试化学试题北京市第六十六中学2023-2024学年高二上学期期中质量检测化学试题
名校
5 . 已知:①2H2O(g)===2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1 ②H2S(g)===H2(g)+S(g) ΔH=+20.1 kJ·mol-1下列判断正确的是( )
| A.氢气的燃烧热:ΔH=-241.8 kJ·mol-1 |
| B.相同条件下,充分燃烧1 mol H2(g)与1 mol S(g)的混合物比充分燃烧1 mol H2S(g)放热多20.1 kJ |
| C.由①②知,水的热稳定性小于硫化氢 |
| D.②中若生成固态硫,ΔH将增大 |
您最近一年使用:0次
2018-10-19更新
|
387次组卷
|
12卷引用:湖南省长沙市第一中学2020-2021学年高一下学期期末考试化学试题
湖南省长沙市第一中学2020-2021学年高一下学期期末考试化学试题2016届内蒙古赤峰市高三上学期期末考试化学试卷福建省泉州市泉港区第一中学2017-2018学年高二上学期期中考试化学试题【全国百强校】甘肃省会宁县第一中学2018-2019学年高二上学期第一次月考化学试题山东省济宁市第二中学2019-2020学年高二上学期第一次月考化学试题吉林省长春市第一五〇中学2019-2020学年高二上学期期中考试化学试卷安徽省滁州市定远县民族中学2019-2020学年高二上学期期中考试化学试题安徽省滁州市定远县炉桥中学2019-2020学年高二上学期第一次检测化学试题吉林公主岭范家屯一中2020-2021学年高二上学期期中考试化学试题(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)(已下线)1.3 燃料的合理利用-【帮课堂】2022-2023学年高二化学同步精品讲义(沪科版2020选择性必修第一册)辽宁省六校2022-2023学年高二上学期期初考试化学试题



