1 . 氮的氧化物是大气污染物之一,用活性炭或一氧化碳还原氮氧化物,可防止空气污染。
(1)已知:2C(s)+O2(g)⇌2CO(g)
C(s)+O2(g)⇌CO2(g)
N2(g)+O2(g)⇌2NO(g)
①则反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g)的
___________ ;(用 、
、 、
、 表示)
表示)
②在一个恒温恒容的密闭容器中发生反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g),能表明已达到平衡状态的标志有___________ 。
A.混合气体的压强保持不变
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变
D.气体的总质量
E.
F. 内生成
内生成 同时消耗
同时消耗
(2)向容积为 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g),
,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g), 和
和 的物质的量变化如下表所示。
的物质的量变化如下表所示。
①0~5min内,以 表示的该反应速率
表示的该反应速率
___________ ,最终达平衡时 的转化率
的转化率
___________ ,该温度T℃下的平衡常数
___________ 。
②若该反应ΔH>0,要提高工业上NO的转化率可采取的措施有___________ (至少写一种)。
(3)CO2和H2在一定条件下可制取甲醇,反应如下:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),向容积相同的恒容密闭容器中分别充入等量的CO2和H2,在不同催化剂(M型、N型)条件下反应相同时间,CO2转化率随反应温度变化如图。
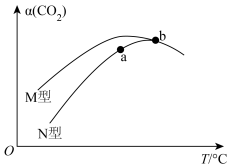
①使用___________ (选填M、N)型催化剂反应的活化能更高。
②b点不同催化剂作用下,CO2的转化率相同且均有下降趋势的原因是___________ 。
(1)已知:2C(s)+O2(g)⇌2CO(g)

C(s)+O2(g)⇌CO2(g)

N2(g)+O2(g)⇌2NO(g)

①则反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g)的

 、
、 、
、 表示)
表示)②在一个恒温恒容的密闭容器中发生反应2CO(g)+2NO(g)⇌N2(g)+2CO2(g),能表明已达到平衡状态的标志有
A.混合气体的压强保持不变
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变
D.气体的总质量
E.

F.
 内生成
内生成 同时消耗
同时消耗
(2)向容积为
 的密闭容器中加入活性炭(足量)和
的密闭容器中加入活性炭(足量)和 ,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g),
,发生反应C(s)+2NO(g)⇌N2(g)+CO2(g), 和
和 的物质的量变化如下表所示。
的物质的量变化如下表所示。| 条件 | 保持温度为 /℃ /℃ | ||||||
| 时间 | 0 | 5min | 10min | 15min | 20min | 25min | 30min |
 物质的量 物质的量 | 2.0 | 1.4 | 1.0 | 0.70 | 0.50 | 0.40 | 0.40 |
| N2物质的量/mol | 0 | 0.3 | 0.50 | 0.65 | 0.75 | 0.80 | 0.80 |
 表示的该反应速率
表示的该反应速率
 的转化率
的转化率

②若该反应ΔH>0,要提高工业上NO的转化率可采取的措施有
(3)CO2和H2在一定条件下可制取甲醇,反应如下:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),向容积相同的恒容密闭容器中分别充入等量的CO2和H2,在不同催化剂(M型、N型)条件下反应相同时间,CO2转化率随反应温度变化如图。

①使用
②b点不同催化剂作用下,CO2的转化率相同且均有下降趋势的原因是
您最近一年使用:0次
2024-02-02更新
|
112次组卷
|
2卷引用:四川省泸州市四川省泸县第五中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
2 . 二氧化碳的捕集和利用是我国能源领域的一个重要战略方向,回答下列问题:
I.工业上用 和
和 反应合成二甲醚:
反应合成二甲醚:
 。某压强下,合成二甲醚的反应在不同温度、不同投料比时,
。某压强下,合成二甲醚的反应在不同温度、不同投料比时, 的平衡转化率如图所示。
的平衡转化率如图所示。

(1)a点时, ℃下,将
℃下,将 和
和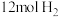 充入VL的恒容密闭容器中,发生上述反应,
充入VL的恒容密闭容器中,发生上述反应, 后,该反应达到平衡状态,则:
后,该反应达到平衡状态,则:
① 内,
内,
___________ (用含V的代数式表示) 。
。
②反应达到平衡时,混合气体的平均相对分子质量为___________ (用分数表示)。
③反应达到平衡时的平衡常数
________ (用含V的代数式表示,写出计算式即可,不用化简)。
(2)在温度为 ℃和
℃和 ℃下:
℃下:
①温度:
___________ (填“>”“<”或“=”) 。
。
② ℃,b点时,
℃,b点时,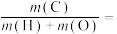
___________ (用分数表示)。
II. 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示。
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示。
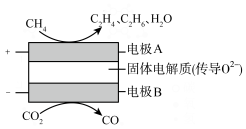
(3)若生成的乙烯和乙烷的体积比为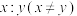 ,则消耗的
,则消耗的 和
和 的体积比为
的体积比为_________ (用含x和y的代数式表示)。
III.常温下,某天然水体中的 与空气中的
与空气中的 保持平衡。
保持平衡。
(4)已知某溶洞水体中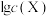 (X为
(X为 、
、 、
、 或
或 )与pH的关系如图所示。
)与pH的关系如图所示。
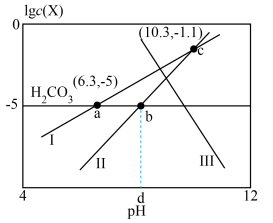
①曲线III代表___________ (填“ ”“
”“ ”“
”“ ”或“
”或“ ”)。
”)。
②d的值为___________ (填具体数字)。
I.工业上用
 和
和 反应合成二甲醚:
反应合成二甲醚:
 。某压强下,合成二甲醚的反应在不同温度、不同投料比时,
。某压强下,合成二甲醚的反应在不同温度、不同投料比时, 的平衡转化率如图所示。
的平衡转化率如图所示。
(1)a点时,
 ℃下,将
℃下,将 和
和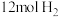 充入VL的恒容密闭容器中,发生上述反应,
充入VL的恒容密闭容器中,发生上述反应, 后,该反应达到平衡状态,则:
后,该反应达到平衡状态,则:①
 内,
内,
 。
。②反应达到平衡时,混合气体的平均相对分子质量为
③反应达到平衡时的平衡常数

(2)在温度为
 ℃和
℃和 ℃下:
℃下:①温度:

 。
。②
 ℃,b点时,
℃,b点时,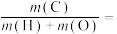
II.
 和
和 都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示。
都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示。
(3)若生成的乙烯和乙烷的体积比为
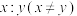 ,则消耗的
,则消耗的 和
和 的体积比为
的体积比为III.常温下,某天然水体中的
 与空气中的
与空气中的 保持平衡。
保持平衡。(4)已知某溶洞水体中
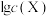 (X为
(X为 、
、 、
、 或
或 )与pH的关系如图所示。
)与pH的关系如图所示。
①曲线III代表
 ”“
”“ ”“
”“ ”或“
”或“ ”)。
”)。②d的值为
您最近一年使用:0次
2023-12-16更新
|
186次组卷
|
5卷引用:四川省泸州市泸县第一中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
3 . 在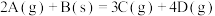 反应中,表示反应速率最快的是
反应中,表示反应速率最快的是
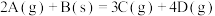 反应中,表示反应速率最快的是
反应中,表示反应速率最快的是A. | B. |
C. | D. |
您最近一年使用:0次
2023-11-28更新
|
142次组卷
|
2卷引用:四川省泸县第一中学2023-2024学年高二上学期12月月考化学试题
4 . 甲烷和甲醇(CH3OH)是重要的化工原料,也是重要的能源物质。
(1)CH3OH(l)的燃烧热为725.8 kJ/mol,请写出表示其燃烧热的热化学方程式:___________ 。
(2)已知反应:
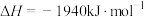 ,已知以下化学键的键能:C-H 414 kJ·mol-1,C-F 489 kJ·mol-1,H-F 565 kJ·mol-1,则F-F键能为
,已知以下化学键的键能:C-H 414 kJ·mol-1,C-F 489 kJ·mol-1,H-F 565 kJ·mol-1,则F-F键能为___________ kJ·mol-1。
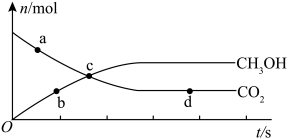
(3)在容积为1 L的恒容密闭容器中投入等物质的量的CO2(g)和H2(g),进行反应: 。
。 、
、 的物质的量随时间变化关系如图所示。图中,表示正反应速率与逆反应速率相等的点是
的物质的量随时间变化关系如图所示。图中,表示正反应速率与逆反应速率相等的点是___________ (填“a”、“b”、“c”或“d”)。用同一物质表示反应速率时,a、c两点的正反应速率:va___________ vc(填“>”、“<”或“=”,下同),该反应达到平衡时,CO2的转化率___________ 50%。
(4)将2.0 mol CH4(g)和3.0 mol H2O(g)通入容积为2 L的恒容密闭容器中,恒温条件下发生反应: 。测得在10 min时反应达到平衡,此时CH4的物质的量为1.6 mol,则0~10 min内,用CO表示该反应的平均反应速率v(CO)=
。测得在10 min时反应达到平衡,此时CH4的物质的量为1.6 mol,则0~10 min内,用CO表示该反应的平均反应速率v(CO)=___________ 。
(5)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如图所示:
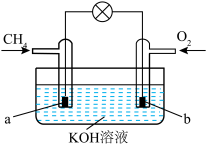
①外电路电子移动方向:___________ (填“a→b”或“b→a”)。
②b处的电极反应为___________
③标准状况下消耗5.6 L O2,外电路中通过导线的电子的数目为___________ 。
(1)CH3OH(l)的燃烧热为725.8 kJ/mol,请写出表示其燃烧热的热化学方程式:
(2)已知反应:

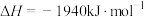 ,已知以下化学键的键能:C-H 414 kJ·mol-1,C-F 489 kJ·mol-1,H-F 565 kJ·mol-1,则F-F键能为
,已知以下化学键的键能:C-H 414 kJ·mol-1,C-F 489 kJ·mol-1,H-F 565 kJ·mol-1,则F-F键能为(3)在容积为1 L的恒容密闭容器中投入等物质的量的CO2(g)和H2(g),进行反应:
 。
。 、
、 的物质的量随时间变化关系如图所示。图中,表示正反应速率与逆反应速率相等的点是
的物质的量随时间变化关系如图所示。图中,表示正反应速率与逆反应速率相等的点是
(4)将2.0 mol CH4(g)和3.0 mol H2O(g)通入容积为2 L的恒容密闭容器中,恒温条件下发生反应:
 。测得在10 min时反应达到平衡,此时CH4的物质的量为1.6 mol,则0~10 min内,用CO表示该反应的平均反应速率v(CO)=
。测得在10 min时反应达到平衡,此时CH4的物质的量为1.6 mol,则0~10 min内,用CO表示该反应的平均反应速率v(CO)=(5)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如图所示:

①外电路电子移动方向:
②b处的电极反应为
③标准状况下消耗5.6 L O2,外电路中通过导线的电子的数目为
您最近一年使用:0次
2023-09-14更新
|
165次组卷
|
2卷引用:四川省泸州市泸县第一中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
5 . 在工业制硫酸中的一步重要反应是 在
在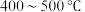 下的催化氧化,其反应:
下的催化氧化,其反应: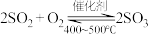 ,在一定条件下,将
,在一定条件下,将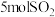 和
和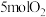 投入容积为
投入容积为 的恒容密闭容器中发生反应,反应过程中
的恒容密闭容器中发生反应,反应过程中 的物质的量 [n(SO2)]随反应时间(t)的变化如图所示。下列叙述错误的是
的物质的量 [n(SO2)]随反应时间(t)的变化如图所示。下列叙述错误的是

 在
在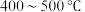 下的催化氧化,其反应:
下的催化氧化,其反应: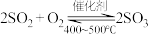 ,在一定条件下,将
,在一定条件下,将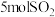 和
和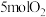 投入容积为
投入容积为 的恒容密闭容器中发生反应,反应过程中
的恒容密闭容器中发生反应,反应过程中 的物质的量 [n(SO2)]随反应时间(t)的变化如图所示。下列叙述错误的是
的物质的量 [n(SO2)]随反应时间(t)的变化如图所示。下列叙述错误的是
| A.使用催化剂可以增大反应速率,提高生产效率 |
B.当反应达到平衡时, 的转化率为 的转化率为 |
C. 内 内 的平均速率为 的平均速率为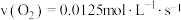 |
D.a点对应的化学反应速率: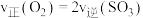 |
您最近一年使用:0次
2023-09-10更新
|
65次组卷
|
2卷引用:四川省泸县第一中学2023-2024学年高二上学期10月月考化学试题
名校
6 . 某研究小组为探究影响化学反应速率的因素,以反应 为研究对象设计如下实验:在恒容密闭容器中,改变实验条件,得到反应物
为研究对象设计如下实验:在恒容密闭容器中,改变实验条件,得到反应物 的浓度
的浓度 随反应时间
随反应时间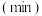 的变化情况如图所示,已知初始时
的变化情况如图所示,已知初始时 的起始浓度为0.下列说法错误的是
的起始浓度为0.下列说法错误的是
 为研究对象设计如下实验:在恒容密闭容器中,改变实验条件,得到反应物
为研究对象设计如下实验:在恒容密闭容器中,改变实验条件,得到反应物 的浓度
的浓度 随反应时间
随反应时间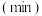 的变化情况如图所示,已知初始时
的变化情况如图所示,已知初始时 的起始浓度为0.下列说法错误的是
的起始浓度为0.下列说法错误的是
| A.比较实验①②得出:增大反应物浓度,化学反应速率加快 |
| B.若实验②③只有一个条件不同,则实验③使用了催化剂 |
| C.比较实验②④得出:升高温度,化学反应速率加快 |
D. 内,实验②的平均反应速率 内,实验②的平均反应速率 |
您最近一年使用:0次
2023-07-15更新
|
208次组卷
|
6卷引用:四川省泸州市泸县第五中学2023-2024学年高二上学期开学考试化学试题
四川省泸州市泸县第五中学2023-2024学年高二上学期开学考试化学试题河北省张家口市2022-2023学年高一下学期期末考试化学试题四川省双流棠湖中学2023-2024学年高二上学期9月月考化学试题(已下线)专题03 化学反应的速率与限度-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)(已下线)猜想05 化学反应的速率和限度(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)(已下线)重难点04 化学反应速率及平衡图像问题的分析-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
名校
解题方法
7 . 氮元素与人类的生命、生产等活动息息相关。
(1)亚硝酸钠( )在生活中有广泛应用,实验室可用如图装置制备(略去部分夹持仪器)。
)在生活中有广泛应用,实验室可用如图装置制备(略去部分夹持仪器)。 ;
;
②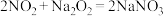
③酸性条件下, 、
、 和
和 都能与
都能与 反应生成
反应生成 和
和
请回答下列问题:
①装置A中发生反应的化学方程式为___________ 。
②装置B中的实验现象为___________ 。
③装置C的作用为___________ 。
④装置F中发生反应的离子方程式为___________ 。
(2)生物脱氮法流程如下: 的消除速率为
的消除速率为 ,则
,则 的消耗速率为
的消耗速率为___________ 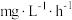 。
。
(3)目前,湿法 和
和 一体化脱除法是解决燃煤烟气领域的途径之一
一体化脱除法是解决燃煤烟气领域的途径之一
已知:两组实验中 溶液浓度均为
溶液浓度均为 ,
, 浓度均为
浓度均为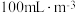
①图1是 、
、 、
、 对
对 的液相吸收。已知
的液相吸收。已知 溶液在脱除
溶液在脱除 时生成一种对空气无污染的气体,请写出该反应化学方程式
时生成一种对空气无污染的气体,请写出该反应化学方程式___________ 。 溶液同时吸收
溶液同时吸收 和
和 ,
, 脱除率在60%左右;单独吸收
脱除率在60%左右;单独吸收 时,
时, 脱除率在33%左右。结合①信息及图像解释原因
脱除率在33%左右。结合①信息及图像解释原因___________ 。
(1)亚硝酸钠(
 )在生活中有广泛应用,实验室可用如图装置制备(略去部分夹持仪器)。
)在生活中有广泛应用,实验室可用如图装置制备(略去部分夹持仪器)。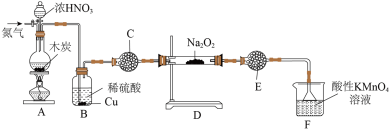
 ;
;②
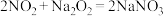
③酸性条件下,
 、
、 和
和 都能与
都能与 反应生成
反应生成 和
和
请回答下列问题:
①装置A中发生反应的化学方程式为
②装置B中的实验现象为
③装置C的作用为
④装置F中发生反应的离子方程式为
(2)生物脱氮法流程如下:
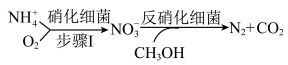
 的消除速率为
的消除速率为 ,则
,则 的消耗速率为
的消耗速率为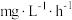 。
。(3)目前,湿法
 和
和 一体化脱除法是解决燃煤烟气领域的途径之一
一体化脱除法是解决燃煤烟气领域的途径之一已知:两组实验中
 溶液浓度均为
溶液浓度均为 ,
, 浓度均为
浓度均为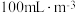
①图1是
 、
、 、
、 对
对 的液相吸收。已知
的液相吸收。已知 溶液在脱除
溶液在脱除 时生成一种对空气无污染的气体,请写出该反应化学方程式
时生成一种对空气无污染的气体,请写出该反应化学方程式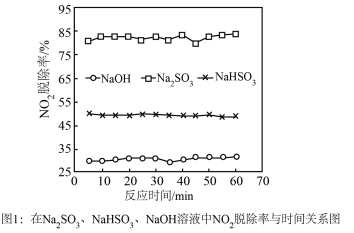
 溶液同时吸收
溶液同时吸收 和
和 ,
, 脱除率在60%左右;单独吸收
脱除率在60%左右;单独吸收 时,
时, 脱除率在33%左右。结合①信息及图像解释原因
脱除率在33%左右。结合①信息及图像解释原因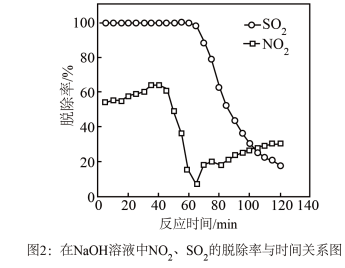
您最近一年使用:0次
2023-07-14更新
|
480次组卷
|
4卷引用:四川省泸州市泸县第五中学2023-2024学年高二上学期开学考试化学试题
四川省泸州市泸县第五中学2023-2024学年高二上学期开学考试化学试题辽宁省辽南协作校2022-2023学年高一下学期期末考试化学试题(已下线)综合02 期末压轴80题之非选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(人教版2019必修第二册)(已下线)综合突破02 期末压轴80题之非选择题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(辽宁专用)
名校
8 . 甲、乙均为容积 的恒容密闭容器。相同温度下,向甲中充入
的恒容密闭容器。相同温度下,向甲中充入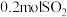 与0.1
与0.1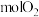 发生反应,
发生反应, 时达平衡,测得反应放出热量
时达平衡,测得反应放出热量 ;向乙中充入0.2
;向乙中充入0.2 气体,达平衡时测得反应吸收热量
气体,达平衡时测得反应吸收热量 。下列说法正确的是
。下列说法正确的是
 的恒容密闭容器。相同温度下,向甲中充入
的恒容密闭容器。相同温度下,向甲中充入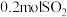 与0.1
与0.1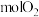 发生反应,
发生反应, 时达平衡,测得反应放出热量
时达平衡,测得反应放出热量 ;向乙中充入0.2
;向乙中充入0.2 气体,达平衡时测得反应吸收热量
气体,达平衡时测得反应吸收热量 。下列说法正确的是
。下列说法正确的是| A.甲、乙中气体密度不变时,均可认为反应达到平衡状态 |
| B.升高温度,甲中反应速率减慢,乙中反应速率加快 |
C.乙中反应的热化学方程式为  |
D.甲中从反应开始到达到平衡,用 表示的平均反应速率为 表示的平均反应速率为 |
您最近一年使用:0次
2023-07-12更新
|
875次组卷
|
4卷引用:四川省泸县第一中学2023-2024学年高二上学期开学考试化学试题
名校
9 . 利用 和
和 反应制甲醇能有效降低大气中
反应制甲醇能有效降低大气中 的含量,总反应为:
的含量,总反应为:
(1) 的物质的量浓度随时间变化的实验数据如下表:
的物质的量浓度随时间变化的实验数据如下表:
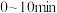 内,
内, 的反应速率为
的反应速率为___________  。
。
(2)下列措施能加快 的是___________(填字母,下同)。
的是___________(填字母,下同)。
(3)在恒温恒容的密闭容器中,充入等物质的量的 和
和 发生上述反应,下列情况
发生上述反应,下列情况不能 说明反应已达到化学平衡状态的是___________。
(4)按图1所示进行实验。

①图1中负极是___________ (填 或
或 )。
)。
②写出该装置正极的电极反应式___________ 。
③若图2中x轴表示流入正极电子的物质的量,y轴可表示___________ 。
A. B.
B.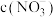 C.
C. 棒质量
棒质量
D. 棒质量 E.溶液的质量
棒质量 E.溶液的质量
 和
和 反应制甲醇能有效降低大气中
反应制甲醇能有效降低大气中 的含量,总反应为:
的含量,总反应为:
(1)
 的物质的量浓度随时间变化的实验数据如下表:
的物质的量浓度随时间变化的实验数据如下表:时间( ) ) | 0 | 5 | 10 | 15 | 20 | 25 |
 | 1.8 | 1.2 | 0.9 | 0.7 | 0.55 | 0.45 |
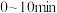 内,
内, 的反应速率为
的反应速率为 。
。(2)下列措施能加快
 的是___________(填字母,下同)。
的是___________(填字母,下同)。| A.升高温度 | B.增大 浓度 浓度 |
C.分离出 | D.扩大容器体积 |
 和
和 发生上述反应,下列情况
发生上述反应,下列情况| A.混合气体的密度不再改变 |
B. 的浓度保持不变 的浓度保持不变 |
C. 体积分数保持不变 体积分数保持不变 |
| D.混合气体的平均相对分子质量保持不变 |

①图1中负极是
 或
或 )。
)。②写出该装置正极的电极反应式
③若图2中x轴表示流入正极电子的物质的量,y轴可表示
A.
 B.
B.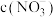 C.
C. 棒质量
棒质量D.
 棒质量 E.溶液的质量
棒质量 E.溶液的质量
您最近一年使用:0次
2023-07-11更新
|
126次组卷
|
3卷引用:四川省泸县第一中学2023-2024学年高二上学期开学考试化学试题
名校
10 . 某温度下CO2加氢制甲醇的总反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),该反应为放热反应,在固定容积为2.0L的密闭容器中充入0.8mol的CO2和2.4mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。
CH3OH(g)+H2O(g),该反应为放热反应,在固定容积为2.0L的密闭容器中充入0.8mol的CO2和2.4mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。
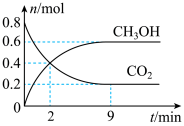
请回答:
(1)对于该反应,反应物的化学键断裂要吸收的能量________ (填“大于”、“小于”或“等于”)生成物的化学键形成要放出的能量。
(2)下列措施能加快反应速率的是________ (填标号)。
A.往容器中充入H2 B.往容器充入N2 C.及时分离出CH3OH
D.增大容器体积 E.选择高效的催化剂
(3)2min内H2的反应速率为__________ 。
(4)该反应达平衡时的压强是开始时压强的__________ 。
(5)恒温恒容条件下,不能说明反应已达平衡状态的是________ (填标号)。
A. CO2(g)体积分数保持不变
B.容器中气体压强保持不变
C.混合气体的密度保持不变
D. H2的生成速率是H2O生成速率的3倍
E.容器中CH3OH浓度与H2O浓度之比为1:1
F.容器内混合气体的平均相对分子质量保持不变
(6)将上述反应制得的甲醇设计成燃料电池,具有启动快、效率高等优点,装置如图所示(A、B为多孔碳棒)。

①实验测得OH向B电极定向移动,则________ (填“A”或“B”)处电极入口通甲醇。
②写出负极电极方程式________ 。
 CH3OH(g)+H2O(g),该反应为放热反应,在固定容积为2.0L的密闭容器中充入0.8mol的CO2和2.4mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。
CH3OH(g)+H2O(g),该反应为放热反应,在固定容积为2.0L的密闭容器中充入0.8mol的CO2和2.4mol的H2,测得CO2和CH3OH的物质的量随时间变化如图。
请回答:
(1)对于该反应,反应物的化学键断裂要吸收的能量
(2)下列措施能加快反应速率的是
A.往容器中充入H2 B.往容器充入N2 C.及时分离出CH3OH
D.增大容器体积 E.选择高效的催化剂
(3)2min内H2的反应速率为
(4)该反应达平衡时的压强是开始时压强的
(5)恒温恒容条件下,不能说明反应已达平衡状态的是
A. CO2(g)体积分数保持不变
B.容器中气体压强保持不变
C.混合气体的密度保持不变
D. H2的生成速率是H2O生成速率的3倍
E.容器中CH3OH浓度与H2O浓度之比为1:1
F.容器内混合气体的平均相对分子质量保持不变
(6)将上述反应制得的甲醇设计成燃料电池,具有启动快、效率高等优点,装置如图所示(A、B为多孔碳棒)。

①实验测得OH向B电极定向移动,则
②写出负极电极方程式
您最近一年使用:0次
2023-07-07更新
|
121次组卷
|
2卷引用:四川省泸县第四中学2023-2024学年高二上学期开学考试化学试题



