名校
1 . “绿水青山就是金山银山”,近年来,绿色发展、生态保护成为中国的新名片。
Ⅰ.已知25℃和101kPa下:
①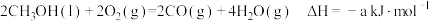
②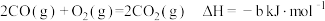
③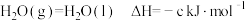
(1)则表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为___________ 。
Ⅱ. 和
和 在一定条件下反应可制得合成气,在1L密闭容器中分别通入
在一定条件下反应可制得合成气,在1L密闭容器中分别通入 和
和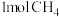 ,发生反应:
,发生反应: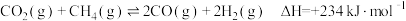 。
。
(2)该反应在___________ (填“高温”或“低温”)条件下能自发进行。
(3)下列能判断 达到平衡状态的是___________(填序号)。
达到平衡状态的是___________(填序号)。
Ⅲ.已知 催化加氢合成乙醇的反应原理为:
催化加氢合成乙醇的反应原理为: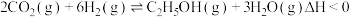 ,设m为起始时的投料比,即
,设m为起始时的投料比,即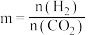 。
。
(4)图中投料比相同,温度从高到低的顺序为___________ 。
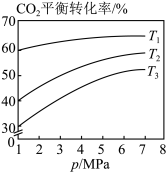
(5)图2 、
、 、
、 从大到小的顺序为
从大到小的顺序为___________ 。

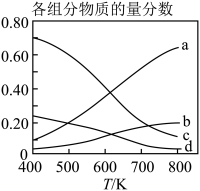
(6)下图表示在总压为5MPa的恒压条件下,且 时,平衡状态时各物质的物质的量分数与温度的关系,则曲线d代表的物质为
时,平衡状态时各物质的物质的量分数与温度的关系,则曲线d代表的物质为___________ (填化学式)。
Ⅳ.工业上可用丙烯加成法制备1,2—二氯丙烷( ),主要副产物为3—氯丙烯(
),主要副产物为3—氯丙烯( ),反应原理为:
),反应原理为:
①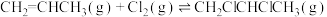
②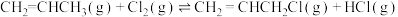
一定温度下,向恒容密闭容器中充入等物质的量的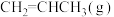 和
和 发生反应,容器内气体的压强随时间的变化如表所示:
发生反应,容器内气体的压强随时间的变化如表所示:
(7)用单位时间内气体分压的变化表示反应①的反应速率,即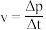 ,则前120min内平均反应速率
,则前120min内平均反应速率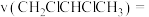
___________ 。
(8)该温度下,若平衡时HCl的体积分数为12.5%,反应①的平衡常数
___________  (
( 为以分压表示的平衡常数,保留小数点后2位)。
为以分压表示的平衡常数,保留小数点后2位)。
Ⅰ.已知25℃和101kPa下:
①
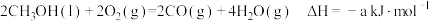
②
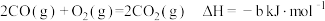
③
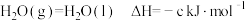
(1)则表示
 燃烧热的热化学方程式为
燃烧热的热化学方程式为Ⅱ.
 和
和 在一定条件下反应可制得合成气,在1L密闭容器中分别通入
在一定条件下反应可制得合成气,在1L密闭容器中分别通入 和
和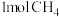 ,发生反应:
,发生反应: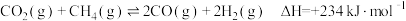 。
。(2)该反应在
(3)下列能判断
 达到平衡状态的是___________(填序号)。
达到平衡状态的是___________(填序号)。| A.一定温度下,容积固定的容器中,密度保持不变 |
| B.容积固定的绝热容器中,温度保持不变 |
| C.一定温度和容积固定的容器中,平均相对分子质量不变 |
D. 和 和 的物质的量之比不再改变 的物质的量之比不再改变 |
Ⅲ.已知
 催化加氢合成乙醇的反应原理为:
催化加氢合成乙醇的反应原理为: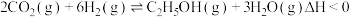 ,设m为起始时的投料比,即
,设m为起始时的投料比,即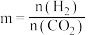 。
。(4)图中投料比相同,温度从高到低的顺序为

(5)图2
 、
、 、
、 从大到小的顺序为
从大到小的顺序为
(6)下图表示在总压为5MPa的恒压条件下,且
 时,平衡状态时各物质的物质的量分数与温度的关系,则曲线d代表的物质为
时,平衡状态时各物质的物质的量分数与温度的关系,则曲线d代表的物质为
Ⅳ.工业上可用丙烯加成法制备1,2—二氯丙烷(
 ),主要副产物为3—氯丙烯(
),主要副产物为3—氯丙烯( ),反应原理为:
),反应原理为:①
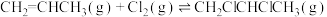
②
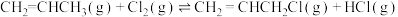
一定温度下,向恒容密闭容器中充入等物质的量的
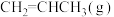 和
和 发生反应,容器内气体的压强随时间的变化如表所示:
发生反应,容器内气体的压强随时间的变化如表所示:| 时间/min | 0 | 60 | 120 | 180 | 240 | 300 | 360 |
| 压强/kPa | 80 | 74.2 | 69.2 | 65.2 | 61.6 | 57.6 | 57.6 |
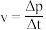 ,则前120min内平均反应速率
,则前120min内平均反应速率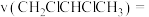
(8)该温度下,若平衡时HCl的体积分数为12.5%,反应①的平衡常数

 (
( 为以分压表示的平衡常数,保留小数点后2位)。
为以分压表示的平衡常数,保留小数点后2位)。
您最近一年使用:0次
名校
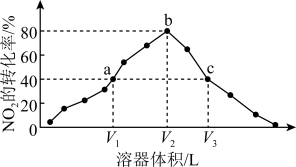
2 . 温度为T℃,向体积不等的密闭容器中分别加入足量活性炭和1molNO2,发生反应:2C(s)+2NO2(g) N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示(V1<V2<V3)。下列说法正确的是
N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示(V1<V2<V3)。下列说法正确的是
 N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示(V1<V2<V3)。下列说法正确的是
N2(g)+2CO2(g)。反应相同时间,测得各容器中NO2的转化率与容器体积的关系如图所示(V1<V2<V3)。下列说法正确的是
| A.对a点容器加压,缩小容器体积,则此时v(逆)<v(正) |
| B.若增加C的质量,则a点可能变成b点 |
| C.向a点体系中充入一定量N2,达到新平衡时,NO2转化率将减小 |
| D.图中c点所示条件下v(逆)>v(正) |
您最近一年使用:0次
名校
解题方法
3 . 在某一恒温、恒容的密闭容器中通入1molN2和3molH2发生反应:3H2(g)+N2(g) 2NH3(g)ΔH<0。t1时刻反应达到平衡,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
2NH3(g)ΔH<0。t1时刻反应达到平衡,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
 2NH3(g)ΔH<0。t1时刻反应达到平衡,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
2NH3(g)ΔH<0。t1时刻反应达到平衡,在t2时刻改变某一条件,其反应过程如图所示。下列说法正确的是
| A.Ⅰ、Ⅱ两过程达到平衡时,平衡常数:KⅠ<KⅡ |
| B.Ⅰ、Ⅱ两过程达到平衡时,NH3的体积分数:Ⅰ<Ⅱ |
| C.该反应正反应的活化能大于逆反应的活化能 |
| D.t2时刻改变的条件可以是向密闭容器中加H2和N2的混合气 |
您最近一年使用:0次
名校
4 . 氢气在富氧条件下催化还原NOx(H2-SCR)反应在低温时仍具有高活性和选择性,近年来一直备受研究学者关注。回答下列问题:
(1)已知催化剂铑(Rh)表面H2催化还原NO的部分反应机理如下表所示,其他条件一定时,决定H2催化还原NO反应速率的基元反应为_______ ,基元反应:H2+Rh(s)+Rh(s)=H(s)+H(s)的焓变ΔH=_______ kJ/mol。
(2)浸渍法合成的Pt/Al-M-10-A催化剂对H2还原NO反应的响应如图所示,由图可知该催化剂对化学反应具有_______ ,该性质受_______ 的影响。

(3)1093 K时,NO与H2以物质的量之比2:1混合,置于某恒容密闭容器中,发生化学反应:2NO(g)+H2(g) N2O(g)+H2O(g),以下物理量不再发生变化时,能说明反应达平衡的是_______(填字母代号)。
N2O(g)+H2O(g),以下物理量不再发生变化时,能说明反应达平衡的是_______(填字母代号)。
(4)将H2、NO、O2按体积比3:2:1充入恒温恒压(200℃、100 kPa)容器中,发生反应:4H2(g)+2NO(g)+O2(g)  N2(g)+4H2O(g),达平衡时,N2的体积分数为0.1。
N2(g)+4H2O(g),达平衡时,N2的体积分数为0.1。
①平衡时,NO的转化率为_______ 。平衡常数Kp=_______ (kPa)-2(以分压表示,分压=总压×物质的量分数)。
②已知该反应ΔH<0。初始温度、压强和反应物的用量均相同。下列四种容器中NO的转化率最高的是_______ (填字母代号)。
A.恒温恒容容器 B.恒温恒压容器 C.恒容绝热容器 D.恒压绝热容器
(1)已知催化剂铑(Rh)表面H2催化还原NO的部分反应机理如下表所示,其他条件一定时,决定H2催化还原NO反应速率的基元反应为
| 基元反应 | 活化能Ea(kJ/mol) |
| H2+Rh(s)+Rh(s)=H(s)+H(s) | 12.6 |
| NO(s)+Rh(s)=N(s)+O(s) | 97.5 |
| N(s)+N(s)=N2+Rh(s)+Rh(s) | 120.9 |
| H(s)+O(s)=OH(s)+Rh(s) | 83.7 |
| OH(s)+H(s)=H2O(s)+Rh(s) | 33.5 |
| H(s)+H(s)=H2+Rh(s)+Rh(s) | 77.8 |
| NO(s)=NO+Rh(s) | 108.9 |

(3)1093 K时,NO与H2以物质的量之比2:1混合,置于某恒容密闭容器中,发生化学反应:2NO(g)+H2(g)
 N2O(g)+H2O(g),以下物理量不再发生变化时,能说明反应达平衡的是_______(填字母代号)。
N2O(g)+H2O(g),以下物理量不再发生变化时,能说明反应达平衡的是_______(填字母代号)。| A.NO的转化率 | B.混合气体的密度 | C.该反应的浓度商QC | D.v(NO)=2v(H2) |
 N2(g)+4H2O(g),达平衡时,N2的体积分数为0.1。
N2(g)+4H2O(g),达平衡时,N2的体积分数为0.1。①平衡时,NO的转化率为
②已知该反应ΔH<0。初始温度、压强和反应物的用量均相同。下列四种容器中NO的转化率最高的是
A.恒温恒容容器 B.恒温恒压容器 C.恒容绝热容器 D.恒压绝热容器
您最近一年使用:0次
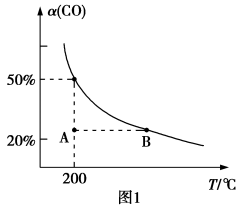
5 . 将4 mol NO(g)和4 mol CO(g)充入一个2 L恒容密闭容器中,发生反应:2NO(g)+2CO(g) 2CO2(g)+N2(g) ΔH<0,测得CO的平衡转化率随温度变化的曲线如图1所示;在催化剂、一定温度下对该反应进行研究,经过相同时间测CO转化率与反应温度的关系曲线如图2所示。下列说法错误的是
2CO2(g)+N2(g) ΔH<0,测得CO的平衡转化率随温度变化的曲线如图1所示;在催化剂、一定温度下对该反应进行研究,经过相同时间测CO转化率与反应温度的关系曲线如图2所示。下列说法错误的是
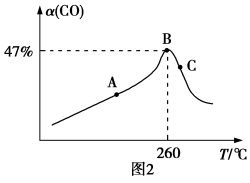
已知:反应速率v=v正−v逆=k正·c2(NO)·c2(CO)−k逆·c2(CO2)·c(N2),k正、k逆分别为正、逆反应速率常数。
 2CO2(g)+N2(g) ΔH<0,测得CO的平衡转化率随温度变化的曲线如图1所示;在催化剂、一定温度下对该反应进行研究,经过相同时间测CO转化率与反应温度的关系曲线如图2所示。下列说法错误的是
2CO2(g)+N2(g) ΔH<0,测得CO的平衡转化率随温度变化的曲线如图1所示;在催化剂、一定温度下对该反应进行研究,经过相同时间测CO转化率与反应温度的关系曲线如图2所示。下列说法错误的是

已知:反应速率v=v正−v逆=k正·c2(NO)·c2(CO)−k逆·c2(CO2)·c(N2),k正、k逆分别为正、逆反应速率常数。
| A.图像中A点逆反应速率小于B点正反应速率 |
| B.200℃时反应的平衡常数K=0.5 |
| C.200℃时当CO的转化率为40%时,v正∶v逆=20:81 |
| D.C点转化率低于B点的原因可能是催化剂活性降低或平衡逆向移动造成的 |
您最近一年使用:0次
2023-01-16更新
|
447次组卷
|
4卷引用:重庆市西南大学附属中学校高2023-2024学年高二上学期10月阶段性检测化学试题
6 . 乙醇既可作为清洁能源,又可作为有机物的萃取剂。除了用微生物发酵法制乙醇,还可用CO2或CO与H2直接反应合成乙醇。用化学法合成乙醇可能发生以下反应:
Ⅰ.2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) ∆H1=-171.4kJ·mol-1
C2H5OH(g)+3H2O(g) ∆H1=-171.4kJ·mol-1
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ∆H2=+41.1kJ·mol-1
CO(g)+H2O(g) ∆H2=+41.1kJ·mol-1
Ⅲ.2CO(g)+4H2(g) C2H5OH(g)+H2O(g) ∆H3
C2H5OH(g)+H2O(g) ∆H3
回答下列问题:
(1)∆H3=_______ 。
(2)在恒温(T>100℃)下,向刚性容器中通入2MPaCO和3MPaH2,加入少量铑(Rh)基催化剂,假设只发生反应Ⅲ,30min后达平衡,总压降低至原来的60%。则该温度下反应Ⅲ的平衡常数Kp为_______ ,CO的平衡转化率为_______ 。可采取_______ 措施(填选项)来提高乙醇的平衡产率。
A.反应容器体积不变,充入一定量氩气 B.适当升高温度
C.再向容器中通入2 MPa CO和3 MPa H2 D.将H2O(g)从体系中分离出去
(3)已知lnk= + lnA(Ea为活化能,k为速率常数,R和A为常数),下图线段b为反应Ⅲ中温度和速率常数的关系,则线段a可能改变的外界条件是
+ lnA(Ea为活化能,k为速率常数,R和A为常数),下图线段b为反应Ⅲ中温度和速率常数的关系,则线段a可能改变的外界条件是_______ 。

(4)研究者认为利用反应Ⅲ制乙醇时,铑基催化剂的催化反应机理如下图:

(“ad”表示被吸附;x=2或3)
该反应产生的副产物有_______ ;已知反应Ⅲ的速率方程为 正=k正c2(CO),且H2、CO在催化剂上的吸附速度很快,则该反应决速步骤最可能为第
正=k正c2(CO),且H2、CO在催化剂上的吸附速度很快,则该反应决速步骤最可能为第_______ 步。(填序号)
Ⅰ.2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g) ∆H1=-171.4kJ·mol-1
C2H5OH(g)+3H2O(g) ∆H1=-171.4kJ·mol-1Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ∆H2=+41.1kJ·mol-1
CO(g)+H2O(g) ∆H2=+41.1kJ·mol-1Ⅲ.2CO(g)+4H2(g)
 C2H5OH(g)+H2O(g) ∆H3
C2H5OH(g)+H2O(g) ∆H3回答下列问题:
(1)∆H3=
(2)在恒温(T>100℃)下,向刚性容器中通入2MPaCO和3MPaH2,加入少量铑(Rh)基催化剂,假设只发生反应Ⅲ,30min后达平衡,总压降低至原来的60%。则该温度下反应Ⅲ的平衡常数Kp为
A.反应容器体积不变,充入一定量氩气 B.适当升高温度
C.再向容器中通入2 MPa CO和3 MPa H2 D.将H2O(g)从体系中分离出去
(3)已知lnk=
 + lnA(Ea为活化能,k为速率常数,R和A为常数),下图线段b为反应Ⅲ中温度和速率常数的关系,则线段a可能改变的外界条件是
+ lnA(Ea为活化能,k为速率常数,R和A为常数),下图线段b为反应Ⅲ中温度和速率常数的关系,则线段a可能改变的外界条件是
(4)研究者认为利用反应Ⅲ制乙醇时,铑基催化剂的催化反应机理如下图:

(“ad”表示被吸附;x=2或3)
该反应产生的副产物有
 正=k正c2(CO),且H2、CO在催化剂上的吸附速度很快,则该反应决速步骤最可能为第
正=k正c2(CO),且H2、CO在催化剂上的吸附速度很快,则该反应决速步骤最可能为第
您最近一年使用:0次
名校
7 . 在恒容密闭容器中充入一定量的H2S气体,平衡时三种组分的物质的量与温度的关系如图所示。下列说法正确的是
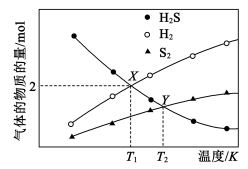

A.反应2H2S(g) S2(g)+2H2(g)的∆H<0 S2(g)+2H2(g)的∆H<0 |
| B.T1时,该反应的平衡常数K=1mol/L |
| C.T2时,H2S的平衡转化率大于50% |
| D.H2S在X点的逆反应速率大于Y点的正反应速率 |
您最近一年使用:0次
2022-04-03更新
|
216次组卷
|
2卷引用:重庆市西南大学附属中学校 2021-2022学年高三上学期第四次月考化学试题
8 . 含铬废水会严重污染环境,一种烟气协同处理含铬废水(含 、
、 、泥沙等)的流程如图:
、泥沙等)的流程如图:

下列说法不正确的是
 、
、 、泥沙等)的流程如图:
、泥沙等)的流程如图:
下列说法不正确的是
| A.“沉降”的主要目的是除去泥沙等不溶物 |
B.溶液A通常选用硫酸“调pH”,目的是将 转化为 转化为 |
| C.“还原”过程涉及的氧化还原反应,氧化剂与还原剂的物质的量之比为2∶3 |
D.母液经处理可获得 |
您最近一年使用:0次
2022-03-22更新
|
322次组卷
|
4卷引用:重庆市北碚区2022-2023学年高三上学期10月月考化学试题
重庆市北碚区2022-2023学年高三上学期10月月考化学试题湖南省长郡中学2021-2022学年高三上学期第四次月考化学试题(已下线)秘籍17 工艺流程的条件控制与计算-备战2022年高考化学抢分秘籍(全国通用)宁夏平罗中学2022-2023学年高二下学期期末考试(重点班)化学试题
名校
解题方法
9 . 已知: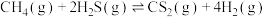 。向恒容密闭容器中充入0.1mol
。向恒容密闭容器中充入0.1mol 和0.2mol
和0.2mol ,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如图所示,下列说法正确的是
,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如图所示,下列说法正确的是

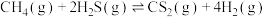 。向恒容密闭容器中充入0.1mol
。向恒容密闭容器中充入0.1mol 和0.2mol
和0.2mol ,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如图所示,下列说法正确的是
,不断升高温度,测得平衡时体系中各物质的物质的量分数与温度的关系如图所示,下列说法正确的是
| A.该反应的△H<0 |
B.X点 的转化率为33.3% 的转化率为33.3% |
| C.X点与Y点容器内压强比为51∶55 |
D.维持Z点温度,向容器中再充入 、 、 、 、 、 、 各0.1mol时,v(正)<v(逆) 各0.1mol时,v(正)<v(逆) |
您最近一年使用:0次
名校
10 . 下列有关生活生产中的叙述合理的是
| A.水库的钢闸门与电源负极相连以防止其生锈,此为牺牲阳极法 |
| B.明矾和漂白粉用于自来水的净化和杀菌消毒,两者的作用原理相同 |
C.将 中毒的病人移至高压氧舱,救治原理与平衡移动有关 中毒的病人移至高压氧舱,救治原理与平衡移动有关 |
D.硫酸工业中 转化为 转化为 时采用常压,是因为增大压强不会提高 时采用常压,是因为增大压强不会提高 的转化率 的转化率 |
您最近一年使用:0次



