真题
解题方法
1 . 磷酸二氢钾在工农业生产及国防工业等领域都有广泛的应用。某研究小组用质量分数为85%的磷酸与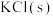 反应制备
反应制备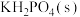 ,反应方程式为
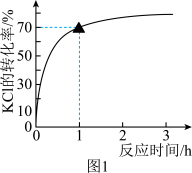
,反应方程式为 一定条件下的实验结果如图1所示。
一定条件下的实验结果如图1所示。
回答问题:
(1)该条件下,反应至1h时KCl的转化率为_______ 。
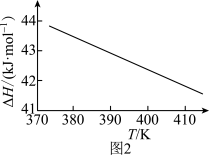
(2)该制备反应的 随温度变化关系如图2所示。该条件下反应为
随温度变化关系如图2所示。该条件下反应为_______ 反应(填“吸热”或“放热”),且反应热随温度升高而_______ 。
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸_______ ;通入水蒸气_______ 。
(4)298K时,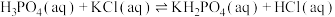 的平衡常数
的平衡常数
_______ 。(已知 的
的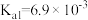 )
)
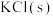 反应制备
反应制备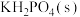 ,反应方程式为
,反应方程式为 一定条件下的实验结果如图1所示。
一定条件下的实验结果如图1所示。
回答问题:
(1)该条件下,反应至1h时KCl的转化率为
(2)该制备反应的
 随温度变化关系如图2所示。该条件下反应为
随温度变化关系如图2所示。该条件下反应为
(3)该小组为提高转化率采用的措施中有:使用浓磷酸作反应物、向系统中不断通入水蒸气等。它们能提高转化率的原因是:不使用稀磷酸
(4)298K时,
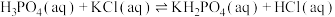 的平衡常数
的平衡常数
 的
的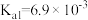 )
)
您最近一年使用:0次
名校
解题方法
2 . CO2的资源化利用一直是科学研究的热点领域。回答下列问题
(1)CO2的甲烷化反应为:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H,该反应又称Sabatier反应。相关的化学键键能数据如表,上述反应的△H=
CH4(g)+2H2O(g) △H,该反应又称Sabatier反应。相关的化学键键能数据如表,上述反应的△H=______ kJ•mol-1。
(2)以CO2和H2为原料合成甲醇(CH3OH)。300℃时,将6molCO2和8molH2的气态混合物充入2L密闭容器中发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0,该容器中n(H2)随时间变化如图中实线所示:
CH3OH(g)+H2O(g) △H<0,该容器中n(H2)随时间变化如图中实线所示:
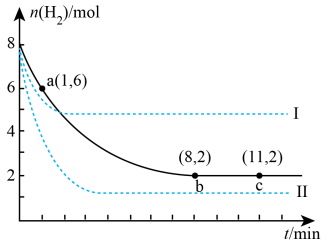
①从反应开始到a点,用CO2表示的反应速率为v(CO2)=______ (保留2位有效数字),此时H2的转化率为______ 。
②根据图中平衡状态计算该反应的平衡常数______ 。
③图中虚线______ (填“I”或“Ⅱ”)表示的是该反应升温时n(H2)随时间变化的曲线,判断依据______ 。
(3)以CO2、NaCl和NH3为原料可以制备NaHCO3。如图为某实验测得NaHCO3溶液的pH随温度的变化曲线(不考虑水挥发)。
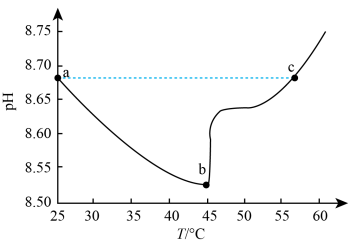
溶液中的c(OH-):a点______ c点(填“>”“<”或“=”)。
(1)CO2的甲烷化反应为:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H,该反应又称Sabatier反应。相关的化学键键能数据如表,上述反应的△H=
CH4(g)+2H2O(g) △H,该反应又称Sabatier反应。相关的化学键键能数据如表,上述反应的△H=| 化学键 | H-H | H-O | C-H | C=O |
| E(kJ•mol-1) | 436 | 463 | 413 | 803 |
 CH3OH(g)+H2O(g) △H<0,该容器中n(H2)随时间变化如图中实线所示:
CH3OH(g)+H2O(g) △H<0,该容器中n(H2)随时间变化如图中实线所示:
①从反应开始到a点,用CO2表示的反应速率为v(CO2)=
②根据图中平衡状态计算该反应的平衡常数
③图中虚线
(3)以CO2、NaCl和NH3为原料可以制备NaHCO3。如图为某实验测得NaHCO3溶液的pH随温度的变化曲线(不考虑水挥发)。

溶液中的c(OH-):a点
您最近一年使用:0次
名校
解题方法
3 . 从低品位铜镍矿(含有Fe2O3、FeO、MgO、CuO等杂质)资源中提取镍和铜的一种工艺流程如下:
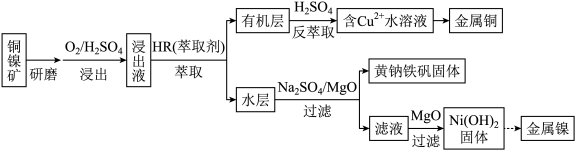
(1)上述流程中,加快反应速率的措施是_______ 。
(2)萃取时发生反应:Cu2+ + 2HR CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:
CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:_______ 。
(3)黄钠铁矾[NaFe3(OH)6(SO4)2]比Fe(OH)3更易形成沉淀。反应终点pH与Fe3+、Ni2+沉淀率的关系如下表。
① 生成黄钠铁矾的离子方程式是_______ 。
② 沉淀Fe3+时最适宜选用的反应终点pH是_______ 。
(4)第二次使用MgO调节pH使Ni2+沉淀完全,宜将pH调节至_______ (填序号)(已知Ksp[Ni(OH)2 ] = 2.1×10-15)。
a.6~7 b.9~10 c.11~12

(1)上述流程中,加快反应速率的措施是
(2)萃取时发生反应:Cu2+ + 2HR
 CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:
CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:(3)黄钠铁矾[NaFe3(OH)6(SO4)2]比Fe(OH)3更易形成沉淀。反应终点pH与Fe3+、Ni2+沉淀率的关系如下表。
| 反应终点pH | 沉淀率/% | |
| Fe3+ | Ni2+ | |
| 1.5 | 94.04 | 0.19 |
| 2.5 | 99.21 | 0.56 |
| 3.8 | 99.91 | 3.31 |
② 沉淀Fe3+时最适宜选用的反应终点pH是
(4)第二次使用MgO调节pH使Ni2+沉淀完全,宜将pH调节至
a.6~7 b.9~10 c.11~12
您最近一年使用:0次
名校
4 . 已知反应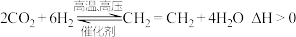 可用于合成烯烃。下列有关该反应的说法
可用于合成烯烃。下列有关该反应的说法错误 的是
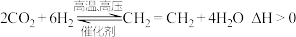 可用于合成烯烃。下列有关该反应的说法
可用于合成烯烃。下列有关该反应的说法| A.增大压强可增大该反应速率 |
B.升高温度能增大 的转化率 的转化率 |
C.增大 的浓度,该反应的平衡常数不变 的浓度,该反应的平衡常数不变 |
D.密闭容器中,通入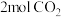 和 和 ,反应生成 ,反应生成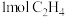 |
您最近一年使用:0次
5 . 200℃时,向体积可变的密闭容器中加入足量草酸锰固体(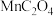 ),发生反应:
),发生反应: 。达到平衡时,
。达到平衡时,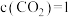 mol·L
mol·L 。温度不变,将体积缩小至原来的一半且保持不变,达到二次平衡。与第一次平衡相比,第二次平衡时,下列说法错误的是
。温度不变,将体积缩小至原来的一半且保持不变,达到二次平衡。与第一次平衡相比,第二次平衡时,下列说法错误的是
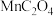 ),发生反应:
),发生反应: 。达到平衡时,
。达到平衡时,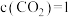 mol·L
mol·L 。温度不变,将体积缩小至原来的一半且保持不变,达到二次平衡。与第一次平衡相比,第二次平衡时,下列说法错误的是
。温度不变,将体积缩小至原来的一半且保持不变,达到二次平衡。与第一次平衡相比,第二次平衡时,下列说法错误的是| A.平衡常数不变 | B. 不变 不变 | C.MnO的质量不变 | D.逆反应速率增大 |
您最近一年使用:0次
2023-02-18更新
|
222次组卷
|
2卷引用:海南省2022-2023学年高二上学期期末学业水平诊断(一)化学试题
6 . 从植物花汁中提取的一种有机物,可简化表示为HIn,在水溶液中因存在下列电离平衡,故可用作酸、碱指示剂:HIn(溶液,红色) H+(溶液)+In-(溶液,黄色),在上述溶液中加入适量下列物质,最终能使指示剂显黄色的是
H+(溶液)+In-(溶液,黄色),在上述溶液中加入适量下列物质,最终能使指示剂显黄色的是
 H+(溶液)+In-(溶液,黄色),在上述溶液中加入适量下列物质,最终能使指示剂显黄色的是
H+(溶液)+In-(溶液,黄色),在上述溶液中加入适量下列物质,最终能使指示剂显黄色的是| A.盐酸 | B.NaHCO3溶液 | C.NaHSO4溶液 | D.NaClO(固体) |
您最近一年使用:0次
2022-12-13更新
|
162次组卷
|
4卷引用:海南省海桂中学2023-2024学年高二上学期12月教学检测(三)化学试题
名校
7 . 在一定条件下,反应2A(g)+2B(g) 3C(g)+D(g),达到平衡状态的标志是:
3C(g)+D(g),达到平衡状态的标志是:
 3C(g)+D(g),达到平衡状态的标志是:
3C(g)+D(g),达到平衡状态的标志是:| A.单位时间内生成2nmolA,同时生成nmolD | B.容器内压强不随时间而变化 |
| C.单位时间内生成nmolB,同时消耗1.5nmolC | D.容器内混合气体密度不随时间而变化 |
您最近一年使用:0次
2022-09-01更新
|
1361次组卷
|
3卷引用:海南省儋州市川绵中学2022-2023学年高二下学期期末考试化学试题
名校
8 . 在一定温度下的密闭容器中发生反应:xA(g)+yB(g)⇌zC(g),平衡时测得A的浓度为0.80mol/L。保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得A的浓度为0.50mol/L。下列有关判断正确的是
| A.x+y<z | B.平衡向正反应方向移动 |
| C.B的转化率增大 | D.C的体积分数减小 |
您最近一年使用:0次
2021-07-23更新
|
461次组卷
|
6卷引用:海南省文昌中学、华迈实验中学2023-2024学年高二上学期期中段考化学试题
名校
9 . 对于可逆反应:
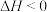 ,下列措施能加快反应速率且使平衡逆向移动的是
,下列措施能加快反应速率且使平衡逆向移动的是

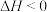 ,下列措施能加快反应速率且使平衡逆向移动的是
,下列措施能加快反应速率且使平衡逆向移动的是| A.增大压强 | B.升高温度 | C.使用催化剂 | D.充入 |
您最近一年使用:0次
2021-01-14更新
|
390次组卷
|
3卷引用:海南省三亚华侨学校(南新校区)2021-2022学年高二上学期期中考试化学试题
10 . 一定条件下: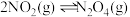
 。在测定
。在测定 的相对分子质量时,下列条件中,测定结果误差最小的是
的相对分子质量时,下列条件中,测定结果误差最小的是
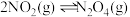
 。在测定
。在测定 的相对分子质量时,下列条件中,测定结果误差最小的是
的相对分子质量时,下列条件中,测定结果误差最小的是A.温度 、压强 、压强 | B.温度 、压强 、压强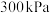 |
C.温度 、压强 、压强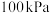 | D.温度 、压强 、压强 |
您最近一年使用:0次
2020-07-11更新
|
3792次组卷
|
56卷引用:海南省华中师范大学琼中附属中学2020-2021学年高二上学期期中考试化学试题
海南省华中师范大学琼中附属中学2020-2021学年高二上学期期中考试化学试题2020年浙江省高考化学试卷(7月选考)(已下线)专题09 反应速率、化学平衡-2020年高考真题和模拟题化学分项汇编黑龙江省大庆市铁人中学2019-2020学年高一下学期期末考试化学试题河南省鹤壁市高级中学2020-2021学年高二上学期阶段性检测(二)化学试题北京二中2020-2021学年高二上学期10月月考化学试题(已下线)【浙江新东方】97湖北省咸宁市通城二中2020-2021学年度高二上学期期中考试化学试题河北省唐山市2020-2021学年高二上学期期末考试化学试题浙江省金华市金华十校2020-2021学年高二上学期调研考试化学试题(已下线)专题06 化学反应速率和化学平衡——备战2021年高考化学纠错笔记(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密09 化学反应速率与平衡(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)【绍兴新东方】绍兴高中化学00007浙江省绍兴市上虞区2020-2021学年高二上学期期末教学质量调测化学试题(已下线)【浙江新东方】【2021.4.27】【温州】【高二上】【高中化学】【00197】(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)选择性必修1(SJ)专题2专题培优专练(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点32 化学反应条件的控制-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时36 化学平衡及平衡移动-2022年高考化学一轮复习小题多维练(全国通用)(已下线)第19讲 化学平衡(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)河北正定中学2020-2021学年高二上学期开学考试化学试题福建省武平县第一中学2021-2022学年高二上学期第一次月考化学试题(已下线)2.3.3 温度变化对化学平衡的影响-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)(已下线)专题12.化学反应速率与化学平衡-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)考向22 化学平衡状态 化学平衡的移动-备战2022年高考化学一轮复习考点微专题浙江省温州新力量联盟2021-2022学年高二上学期期中联考化学试题河南省濮阳市第一高级中学2021-2022学年高二上学期期中质量检测化学试题黑龙江省大庆实验中学2021-2022学年高二上学期期末考试化学试题陕西省宝鸡市渭滨区2021-2022学年高二上学期期末考试化学试题(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密09 化学反应速率与化学平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)浙江省吴兴高级中学高二 2021-2022学年上学期10月月考化学试题天津市部分区2021-2022学年高三上学期期末考试化学试题湖南省长沙市长郡中学2021-2022学年高三下学期月考考试(第六次)化学试题广西柳州市第三中学2021-2022学年高二下学期期中考试化学试题上海市川沙中学2021-2022学年高三下学期5月月考化学试题(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)广西桂林市第十八中学2021-2022学年高二下学期开学考试化学试题(已下线)第19讲 化学平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)广东省深圳市华中师范大学龙岗附属中学2021-2022学年高二上学期期中考试化学试题河北省石家庄市第十七中学2022-2023学年高二上学期10月月考化学试题(已下线)第七章 化学反应速率与化学平衡 第43讲 化学平衡移动原理及应用浙江省杭州第二中学2022-2023学年高二上学期期中考试化学(B卷)试题四川省凉山彝族自治州2022-2023学年高二上学期期末检测化学试题浙江省绍兴市柯桥区2022-2023学年高一下学期期末教学质量检测化学(实验班)试题作业(十二) 压强对化学平衡的影响 勒·夏特列原理广东省广州市第二中学2023-2024学年高二上学期期中考试化学试题浙江省湖州市吴兴高级中学2023-2024学年高二上学期10月阶段性测试化学试题福建省厦门市湖滨中学2023-2024学年高二上学期期中考试化学试题福建省福州高级中学2022-2023学年高二上学期学段考试化学试题黑龙江省海林市朝鲜族中学2023-2024学年高二上学期第二次月考化学试题陕西省兴平市南郊高级中学2023-2024学年高二上学期第一次质量检测化学试题天津市九十六中学2023-2024学年高三上学期12月月考化学试题



