解题方法
1 . 工业尾气脱硝是减少空气污染的重要举措.回答下列问题:
(1)已知相关反应的热力学数据如下表所示:
①理论上,反应消耗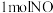 时,反应
时,反应______ (填“吸收”或“释放”)__________  的能量;
的能量;
② 时,另一脱硝反应
时,另一脱硝反应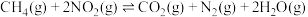 的
的
_______ ;(用含有a、b的式子表示)
(2)模拟工业尾气脱硝:一定条件下,将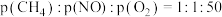 的气体与
的气体与 混合,均匀通过催化脱硝反应器,测得
混合,均匀通过催化脱硝反应器,测得 内
内 去除率与
去除率与 转化率随反应温度的变化如图所示.
转化率随反应温度的变化如图所示. 的去除率最高的原因是
的去除率最高的原因是_________________ ;
②若只考虑反应Ⅰ和Ⅲ,则温度为T时,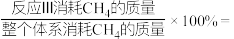
_______ ;(保留到0.1%)
③ 时,为提高反应Ⅲ中
时,为提高反应Ⅲ中 的平衡转化率,理论上能采取的措施是
的平衡转化率,理论上能采取的措施是________ ;(填选项)
A.适当降低温度 B.加入少量生石灰
C.恒容充入更多 D.使用更高效的催化剂
D.使用更高效的催化剂
(1)已知相关反应的热力学数据如下表所示:
| 反应 | 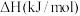 | 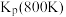 | |
| Ⅰ |  |  | |
| Ⅱ | 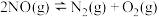 | 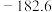 | |
| Ⅲ | 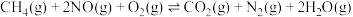 | a | |
| Ⅳ |  | b |
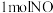 时,反应
时,反应 的能量;
的能量;②
 时,另一脱硝反应
时,另一脱硝反应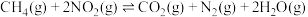 的
的
(2)模拟工业尾气脱硝:一定条件下,将
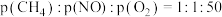 的气体与
的气体与 混合,均匀通过催化脱硝反应器,测得
混合,均匀通过催化脱硝反应器,测得 内
内 去除率与
去除率与 转化率随反应温度的变化如图所示.
转化率随反应温度的变化如图所示.
 的去除率最高的原因是
的去除率最高的原因是②若只考虑反应Ⅰ和Ⅲ,则温度为T时,
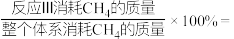
③
 时,为提高反应Ⅲ中
时,为提高反应Ⅲ中 的平衡转化率,理论上能采取的措施是
的平衡转化率,理论上能采取的措施是A.适当降低温度 B.加入少量生石灰
C.恒容充入更多
 D.使用更高效的催化剂
D.使用更高效的催化剂
您最近一年使用:0次
解题方法
2 . 卤素是典型的非金属元素。
(1)它们在自然界中都以___________ 态存在(填“游离”或“化合”)。
氯气在常温常压下溶于水的过程及其平衡常数如下:
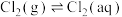
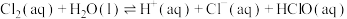
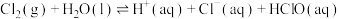

(2)
___________ (用含 和
和 的代数式表示)。若平衡时
的代数式表示)。若平衡时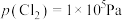 、
、 估算饱和氯水的
估算饱和氯水的
___________ (忽略次氯酸和水的电离, ,结果保留两位有效数字);
,结果保留两位有效数字);
(3)已知某氯气—氯水体系中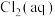 、HClO、
、HClO、 的物质的量分数(
的物质的量分数( )随pH变化如图所示。
)随pH变化如图所示。
___________ ;
(4)下表是 在蒸馏水和NaCl溶液中的溶解度数据:
在蒸馏水和NaCl溶液中的溶解度数据:
请从物质结构的角度分析氯气在NaCl溶液中溶解度减小的原因___________ ;
(5)某实验小组研究 在盐酸中的溶解性。利用数字化实验仪器,得出下列随温度和盐酸浓度变化氯气的溶解度图:
在盐酸中的溶解性。利用数字化实验仪器,得出下列随温度和盐酸浓度变化氯气的溶解度图: 浓度较大时发生反应
浓度较大时发生反应
 ,
, 热稳定性差。
热稳定性差。
① 中心氯原子3d轨道
中心氯原子3d轨道___________ 杂化(填“参与”或“不参与”);
②推测盐酸浓度较大时,随着盐酸浓度的增大, 溶解度增大的原因是
溶解度增大的原因是___________ ;
③温度升高(不考虑HCl的挥发)后盐酸浓度变化对氯气的溶解度影响变小的原因是___________ 。
(1)它们在自然界中都以
氯气在常温常压下溶于水的过程及其平衡常数如下:
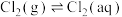
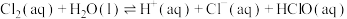
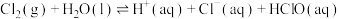

(2)

 和
和 的代数式表示)。若平衡时
的代数式表示)。若平衡时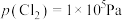 、
、 估算饱和氯水的
估算饱和氯水的
 ,结果保留两位有效数字);
,结果保留两位有效数字);(3)已知某氯气—氯水体系中
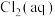 、HClO、
、HClO、 的物质的量分数(
的物质的量分数( )随pH变化如图所示。
)随pH变化如图所示。

(4)下表是
 在蒸馏水和NaCl溶液中的溶解度数据:
在蒸馏水和NaCl溶液中的溶解度数据: | 0 | 1.32 |
 | 0.095 | 0.059 |
(5)某实验小组研究
 在盐酸中的溶解性。利用数字化实验仪器,得出下列随温度和盐酸浓度变化氯气的溶解度图:
在盐酸中的溶解性。利用数字化实验仪器,得出下列随温度和盐酸浓度变化氯气的溶解度图:
 浓度较大时发生反应
浓度较大时发生反应
 ,
, 热稳定性差。
热稳定性差。①
 中心氯原子3d轨道
中心氯原子3d轨道②推测盐酸浓度较大时,随着盐酸浓度的增大,
 溶解度增大的原因是
溶解度增大的原因是③温度升高(不考虑HCl的挥发)后盐酸浓度变化对氯气的溶解度影响变小的原因是
您最近一年使用:0次
2024·广西·模拟预测
名校
解题方法
3 . 实验室用以下装置(夹持和水浴加热装置略)制备环己酮缩乙二醇。
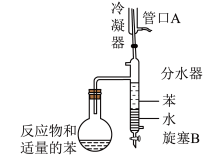

| A.以共沸体系带出水促使反应正向进行 |
| B.当观察到分水器中苯层液面高于支管口时,必须打开旋塞B将水放出 |
| C.管口A是冷凝水的进水口 |
| D.根据带出水的体积可估算反应进度 |
您最近一年使用:0次
2023-12-20更新
|
2150次组卷
|
8卷引用:辽宁省鞍山市普通高中2023-2024学年高三上学期期末联考化学试题
辽宁省鞍山市普通高中2023-2024学年高三上学期期末联考化学试题(已下线)化学01(14+4模式)2024年1月“九省联考”考前化学猜想卷(已下线)热点19 化学微型实验福建省泉州市永春一中、培元中学、石光中学、季延中学2023-2024学年高三下学期第二次联合考试化学试题河南省漯河市高级中学2023-2024学年高三下学期3月月考化学试题(已下线)专题03 化学实验基础-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)(已下线)专题02 元素化合物 有机化合物-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)2024届湖南省长沙市第一中高三下学期高考适应性演练(一)化学试题
解题方法
4 .  在化学化工领域有诸多用途。回答下列问题:
在化学化工领域有诸多用途。回答下列问题:
(1) 、
、 条件下,
条件下, 的燃烧过程中,每消耗
的燃烧过程中,每消耗 放出
放出 热量,表示
热量,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为_______ 。
(2)在 催化作用下合成
催化作用下合成 的反应为
的反应为 。
。
①下列有利于提高 的平衡转化率的是
的平衡转化率的是_______ (填字母,下同)。
A.低温高压 B.高温低压 C.高温高压 D.低温低压
②下列有关合成 的说法中正确的是
的说法中正确的是_______ 。

A.存在非极性共价键的断裂与形成
B.所有分子均为极性分子
C.如图为 的晶胞结构,图中
的晶胞结构,图中 表示
表示
D.催化剂可降低该反应的焓变
(3)工业上可利用 和
和 反应制备光气
反应制备光气 :
: 。在
。在 恒温恒容密闭容器中充入
恒温恒容密闭容器中充入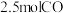 和
和 ,在催化剂作用下发生反应,测得
,在催化剂作用下发生反应,测得 及
及 的物质的量随时间变化如图所示:
的物质的量随时间变化如图所示:

①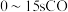 的平均反应速率为
的平均反应速率为_______  。
。
②第一次平衡时, 的平衡转化率为
的平衡转化率为_______ ;该温度下反应的平衡常数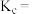
_______ (保留三位有效数字)。
③在第 时,改变的条件是
时,改变的条件是_______ 。
(4)一定条件下, 与
与 反应生成
反应生成 和
和 :
: 。已知
。已知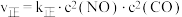 ,
,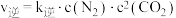 (
( 、
、 为速率常数,只与温度有关)。若在
为速率常数,只与温度有关)。若在 的密闭容器中充入
的密闭容器中充入 和
和 ,在一定温度下达到平衡时,
,在一定温度下达到平衡时, 的转化率为
的转化率为 ,则
,则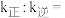
_______ 。
 在化学化工领域有诸多用途。回答下列问题:
在化学化工领域有诸多用途。回答下列问题:(1)
 、
、 条件下,
条件下, 的燃烧过程中,每消耗
的燃烧过程中,每消耗 放出
放出 热量,表示
热量,表示 燃烧热的热化学方程式为
燃烧热的热化学方程式为(2)在
 催化作用下合成
催化作用下合成 的反应为
的反应为 。
。①下列有利于提高
 的平衡转化率的是
的平衡转化率的是A.低温高压 B.高温低压 C.高温高压 D.低温低压
②下列有关合成
 的说法中正确的是
的说法中正确的是
A.存在非极性共价键的断裂与形成
B.所有分子均为极性分子
C.如图为
 的晶胞结构,图中
的晶胞结构,图中 表示
表示
D.催化剂可降低该反应的焓变

(3)工业上可利用
 和
和 反应制备光气
反应制备光气 :
: 。在
。在 恒温恒容密闭容器中充入
恒温恒容密闭容器中充入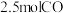 和
和 ,在催化剂作用下发生反应,测得
,在催化剂作用下发生反应,测得 及
及 的物质的量随时间变化如图所示:
的物质的量随时间变化如图所示:
①
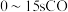 的平均反应速率为
的平均反应速率为 。
。②第一次平衡时,
 的平衡转化率为
的平衡转化率为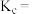
③在第
 时,改变的条件是
时,改变的条件是(4)一定条件下,
 与
与 反应生成
反应生成 和
和 :
: 。已知
。已知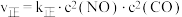 ,
,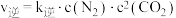 (
( 、
、 为速率常数,只与温度有关)。若在
为速率常数,只与温度有关)。若在 的密闭容器中充入
的密闭容器中充入 和
和 ,在一定温度下达到平衡时,
,在一定温度下达到平衡时, 的转化率为
的转化率为 ,则
,则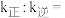
您最近一年使用:0次
2023-07-12更新
|
65次组卷
|
2卷引用:辽宁省朝阳市2022-2023学年高二下学期期末联考化学试题
5 . 在600K下,按初始投料比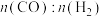 分别为1:1、1:2、1:3投料,发生反应为
分别为1:1、1:2、1:3投料,发生反应为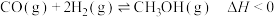 。测得不同压强下,CO平衡转化率如图所示。下列叙述正确的是
。测得不同压强下,CO平衡转化率如图所示。下列叙述正确的是
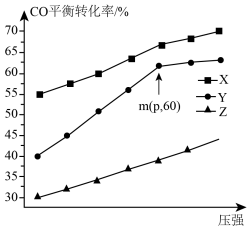
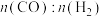 分别为1:1、1:2、1:3投料,发生反应为
分别为1:1、1:2、1:3投料,发生反应为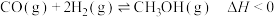 。测得不同压强下,CO平衡转化率如图所示。下列叙述正确的是
。测得不同压强下,CO平衡转化率如图所示。下列叙述正确的是
| A.曲线X代表起始投料比为1:1 |
B.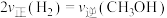 ,该反应达到平衡状态 ,该反应达到平衡状态 |
| C.若其他条件不变,升高温度会使对应的曲线上移 |
D.m点对应的 的平衡转化率为60% 的平衡转化率为60% |
您最近一年使用:0次
名校
6 . 甲烷是一种温室气体,将它转化为高附加值产品甲醇具有重要意义。目前工业上的甲烷转化大多需要先通过重整生成合成气(CO、 )再转化为甲醇,涉及的反应如下:
)再转化为甲醇,涉及的反应如下:
反应Ⅰ: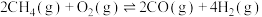

反应Ⅱ:
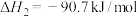
在密闭容器中通入3mol 和2mol
和2mol  ,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和2MPa下进行反应,其中
,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和2MPa下进行反应,其中 和
和 的平衡体积分数随温度变化如图所示。
的平衡体积分数随温度变化如图所示。

已知:对于反应Ⅱ, ,
, ,
, 、
、 为速率常数,只与温度有关,分压=总压×物质的量分数。下列说法不正确的是
为速率常数,只与温度有关,分压=总压×物质的量分数。下列说法不正确的是
 )再转化为甲醇,涉及的反应如下:
)再转化为甲醇,涉及的反应如下:反应Ⅰ:
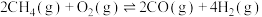

反应Ⅱ:

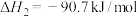
在密闭容器中通入3mol
 和2mol
和2mol  ,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和2MPa下进行反应,其中
,假设只发生反应Ⅰ和Ⅱ,分别在0.2MPa和2MPa下进行反应,其中 和
和 的平衡体积分数随温度变化如图所示。
的平衡体积分数随温度变化如图所示。
已知:对于反应Ⅱ,
 ,
, ,
, 、
、 为速率常数,只与温度有关,分压=总压×物质的量分数。下列说法不正确的是
为速率常数,只与温度有关,分压=总压×物质的量分数。下列说法不正确的是A.压强为0.2MPa时,表示 和 和 的曲线分别是b、d 的曲线分别是b、d |
| B.混合气体的平均相对分子质量保持不变时,说明反应体系已达到平衡 |
C.在升温的过程中,反应Ⅱ速率常数增大的倍数; > > |
D.500K,2MPa条件下,若平衡时CO的物质的量为1mol,则 的转化率约为66.7% 的转化率约为66.7% |
您最近一年使用:0次
2023-05-13更新
|
540次组卷
|
4卷引用:辽宁省沈阳市五校协作体2023-2024学年高三上学期期中考试化学试题
辽宁省沈阳市五校协作体2023-2024学年高三上学期期中考试化学试题 重庆市2023届高三下学期5月“三诊”化学试题(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)选择题11-14
名校
7 . 某同学进行如下实验:
①取少量稀盐酸放于试管中,投入光亮的铜片,无明显变化。
②向实验①的试管中通入足量的 ,铜片表面很快变暗,生成黑色同体,溶液逐渐变为棕色。
,铜片表面很快变暗,生成黑色同体,溶液逐渐变为棕色。
③若将稀盐酸换成稀硫酸重复实验①和②,均无明显变化。
资料: 是白色固体,难溶于水,能溶于盐酸,
是白色固体,难溶于水,能溶于盐酸,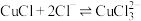 (棕色)
(棕色)
下列说法不正确 的是
①取少量稀盐酸放于试管中,投入光亮的铜片,无明显变化。
②向实验①的试管中通入足量的
 ,铜片表面很快变暗,生成黑色同体,溶液逐渐变为棕色。
,铜片表面很快变暗,生成黑色同体,溶液逐渐变为棕色。③若将稀盐酸换成稀硫酸重复实验①和②,均无明显变化。
资料:
 是白色固体,难溶于水,能溶于盐酸,
是白色固体,难溶于水,能溶于盐酸,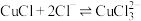 (棕色)
(棕色)下列说法
A.黑色固体不是 |
| B.将棕色溶液加水稀释,会产生白色沉淀 |
C.由实验①②能说明 增强了 增强了 的还原性 的还原性 |
D.上述过程中可能发生的反应: |
您最近一年使用:0次
2023-01-03更新
|
1022次组卷
|
7卷引用:辽宁省东北育才学校2024届高三上学期高中学段联合考试化学试题
辽宁省东北育才学校2024届高三上学期高中学段联合考试化学试题北京市海淀区2023届高三上学期期末考试化学试卷(已下线)北京市海淀区2022-2023学年高三上学期期末考试化学试卷(已下线)北京市海淀区2023届高三上学期期末考试变式汇编(8-14)北京师范大学附属实验中学2022-2023学年高二下学期3月月考化学试题北京市第一七一中学2023-2024学年高三上学期10月考化学试题湖北省襄阳市第五中学2023-2024学年高三上学期10月月考化学试题
名校
8 . 恒容密闭容器中,反应NH4HS(s) NH3(g)+H2S(g)在某一温度下达到平衡状态,其他条件不变,仅改变下列条件,不会使化学平衡发生移动的是
NH3(g)+H2S(g)在某一温度下达到平衡状态,其他条件不变,仅改变下列条件,不会使化学平衡发生移动的是
①减少部分NH4HS固体 ②充入少量氨气 ③充入氦气 ④充入SO2气体
 NH3(g)+H2S(g)在某一温度下达到平衡状态,其他条件不变,仅改变下列条件,不会使化学平衡发生移动的是
NH3(g)+H2S(g)在某一温度下达到平衡状态,其他条件不变,仅改变下列条件,不会使化学平衡发生移动的是①减少部分NH4HS固体 ②充入少量氨气 ③充入氦气 ④充入SO2气体
| A.①② | B.②③ | C.①③ | D.②④ |
您最近一年使用:0次
2022-12-03更新
|
370次组卷
|
5卷引用:辽宁省大连市滨海高中联盟2022-2023学年高一下学期期中考试化学试题
9 . 在一定温度下的密闭容器中发生反应:mA(g)+nB(g)⇌pC(g)+qD(s),平衡时测得C的浓度为 。保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得C的浓度为
。保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得C的浓度为 。下列有关判断正确的是
。下列有关判断正确的是
 。保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得C的浓度为
。保持温度不变,将容器的容积扩大到原来的二倍,再达平衡时,测得C的浓度为 。下列有关判断正确的是
。下列有关判断正确的是| A.B的转化率增大 | B.平衡向逆反应方向移动 |
| C.m+n>p+q | D.C的体积分数减小 |
您最近一年使用:0次
名校
10 . 在容积为VL的恒温密闭容器中模拟工业合成氨。充入N2和H2的总物质的量为1mol,容器内各组分的物质的量分数与反应时间t的关系如图所示。下列说法不正确的是


| A.a表示N2物质的量分数的变化情况 |
B.0~t1min,v(H2)= mol·L-1·min-1 mol·L-1·min-1 |
| C.t2min时,NH3的分解速率小于其生成速率 |
| D.t3min时改变的条件可能为减小容器容积 |
您最近一年使用:0次
2022-02-26更新
|
2119次组卷
|
17卷引用:辽宁省沈阳市第二中学2023-2024学年高二上学期10月阶段考试化学试题
辽宁省沈阳市第二中学2023-2024学年高二上学期10月阶段考试化学试题辽宁省沈阳市第二中学2023-2024学年高三上学期期中考试化学试题辽宁省沈阳市第二中学2023-2024学年高三上学期 期中化学试卷广东省深圳市普通高中2022届高三下学期第一次调研考试化学试题(已下线)二轮拔高卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(天津专用)广东省深圳市第七高级中学2021-2022学年高三第七次月考化学试题(已下线)必刷卷01-2022年高考化学考前信息必刷卷(广东专用)(已下线)卷11 化学反应速率和平衡选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)专项12 化学反应速率与化学平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)湖南省常宁市第一中学2021-2022学年高三下学期期中考试化学试题(已下线)押广东卷化学第14题 化学反应速率与化学平衡-备战2022年高考化学临考题号押题天津市新华中学2022届高三下学期高考校一模(统练8)化学试题(已下线)2022年广东卷高考真题变式题(11-16)(已下线)专题13 化学反应速率与化学平衡-备战2023年高考化学母题题源解密(广东卷)河北省石家庄市第二中学2022届高三2.5模化学试题天津市宝坻区第一中学2022-2023学年高三上学期线上期末训练化学试题广东省汕尾市华大实验学校2021-2022学年高三下学期第二次周考化学试题



