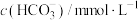1 . 含硫化合物在能源、材料及环境等工业领域均有广泛的应用。
Ⅰ.工业废气 分解可制取
分解可制取 。
。
(1)已知热化学方程式:
ⅰ.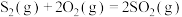

ⅱ.

ⅲ.

 热分解反应
热分解反应 的
的
___________ (用含 、
、 、
、 的式子表示)。
的式子表示)。
(2)一定温度下,2mol 在体积为VL的恒容密闭容器中发生上述分解反应,ts时
在体积为VL的恒容密闭容器中发生上述分解反应,ts时 的产率为40%,则0~ts内
的产率为40%,则0~ts内 的平均分解速率为
的平均分解速率为___________  ;
; 充分分解达到平衡时,容器中
充分分解达到平衡时,容器中 和
和 的分压相等,则该温度下的平衡常数
的分压相等,则该温度下的平衡常数
___________ 。
Ⅱ.KSCN可用于镀铬工业。常温下,用KSCN配制电镀液,溶液中 与
与 发生第一、二步络合的反应如下:
发生第一、二步络合的反应如下:
ⅳ.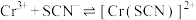
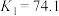
ⅴ.

(3)根据以上络合反应,下列说法正确的有___________(填字母)。
(4)常温下,某研究小组配制了起始浓度 、
、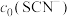 不同的系列溶液,测得平衡时
不同的系列溶液,测得平衡时 、
、 、
、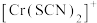 的浓度
的浓度 (含铬微粒)随
(含铬微粒)随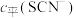 的变化曲线如图所示,平衡后其他含铬微粒
的变化曲线如图所示,平衡后其他含铬微粒 (3≤x≤6,图中未画出)总浓度为amol/L。
(3≤x≤6,图中未画出)总浓度为amol/L。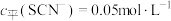 时,图中含铬微粒按浓度由大到小的顺序为
时,图中含铬微粒按浓度由大到小的顺序为___________ ;A点时,溶液中 的平衡浓度为
的平衡浓度为___________ (列出计算式即可)。
②在某电镀工艺中, 的浓度需要在
的浓度需要在 以上,结合计算判断C点所对应的溶液能否用于该电镀工艺
以上,结合计算判断C点所对应的溶液能否用于该电镀工艺________ (写出计算过程)。
Ⅰ.工业废气
 分解可制取
分解可制取 。
。(1)已知热化学方程式:
ⅰ.
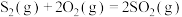

ⅱ.


ⅲ.


 热分解反应
热分解反应 的
的
 、
、 、
、 的式子表示)。
的式子表示)。(2)一定温度下,2mol
 在体积为VL的恒容密闭容器中发生上述分解反应,ts时
在体积为VL的恒容密闭容器中发生上述分解反应,ts时 的产率为40%,则0~ts内
的产率为40%,则0~ts内 的平均分解速率为
的平均分解速率为 ;
; 充分分解达到平衡时,容器中
充分分解达到平衡时,容器中 和
和 的分压相等,则该温度下的平衡常数
的分压相等,则该温度下的平衡常数
Ⅱ.KSCN可用于镀铬工业。常温下,用KSCN配制电镀液,溶液中
 与
与 发生第一、二步络合的反应如下:
发生第一、二步络合的反应如下:ⅳ.
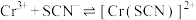
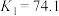
ⅴ.


(3)根据以上络合反应,下列说法正确的有___________(填字母)。
| A.加水稀释后,溶液中离子的总数减少 |
B.加入少量 固体,溶液中含铬微粒总数不变 固体,溶液中含铬微粒总数不变 |
C.反应 的平衡常数 的平衡常数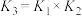 |
D.溶液中 减小, 减小, 与 与 浓度的比值减小 浓度的比值减小 |
(4)常温下,某研究小组配制了起始浓度
 、
、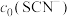 不同的系列溶液,测得平衡时
不同的系列溶液,测得平衡时 、
、 、
、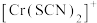 的浓度
的浓度 (含铬微粒)随
(含铬微粒)随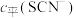 的变化曲线如图所示,平衡后其他含铬微粒
的变化曲线如图所示,平衡后其他含铬微粒 (3≤x≤6,图中未画出)总浓度为amol/L。
(3≤x≤6,图中未画出)总浓度为amol/L。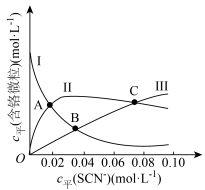
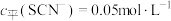 时,图中含铬微粒按浓度由大到小的顺序为
时,图中含铬微粒按浓度由大到小的顺序为 的平衡浓度为
的平衡浓度为②在某电镀工艺中,
 的浓度需要在
的浓度需要在 以上,结合计算判断C点所对应的溶液能否用于该电镀工艺
以上,结合计算判断C点所对应的溶液能否用于该电镀工艺
您最近一年使用:0次
2 . 实验室模拟某含有机酸 工业废水的处理过程。
工业废水的处理过程。
 .利用
.利用 先与金属阳离子络合再被紫外光催化降解的方法去除
先与金属阳离子络合再被紫外光催化降解的方法去除 ,其机理如下:
,其机理如下:
(1) 和
和 发生络合反应生成有色物质:
发生络合反应生成有色物质:


①基态 的价电子排布式为
的价电子排布式为___________ 。
②下列有关上述络合反应的说法中,正确的有___________ (填标号)。
A.反应达平衡时,溶液的颜色不再变化
B.增大 浓度,逆反应速率减小
浓度,逆反应速率减小
C. 过低不利于
过低不利于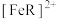 的生成
的生成
D.升高温度,该平衡正向移动
(2)紫外光催化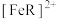 降解:
降解:
若有机酸为 ,则光催化降解反应的离子方程式为:
,则光催化降解反应的离子方程式为:___________ 。
 ___________
___________ ___________
___________ ___________
___________ ___________
___________
 .利用有机溶剂从废水中萃取
.利用有机溶剂从废水中萃取 的方法去除
的方法去除 。该过程涉及以下反应:
。该过程涉及以下反应:
(i)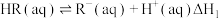
(ii)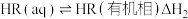
(iii)
(3)根据盖斯定律,反应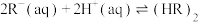 (有机相)的
(有机相)的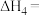
___________ 。
(4)水相的 以及体系温度
以及体系温度 对
对 的平衡分配比
的平衡分配比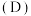 有影响。
有影响。
已知: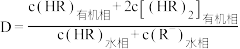 。
。
①常温下,配制体积相同、 不同、含
不同、含 粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到
粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到 随
随 变化的曲线如图所示。分析
变化的曲线如图所示。分析 随
随 升高而降低的原因
升高而降低的原因___________ 。 溶液
溶液 时,
时,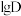 随
随 的变化曲线如图所示。
的变化曲线如图所示。 萃取宜在
萃取宜在___________ 温度下进行(填“较高”或“较低”)。
 经测定,在图中
经测定,在图中 点对应温度下,反应(ii)平衡常数
点对应温度下,反应(ii)平衡常数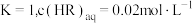 ,忽略水相中
,忽略水相中 的电离,则有机相中
的电离,则有机相中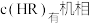
___________ 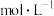 ;计算该温度下,反应(iii)的平衡常数
;计算该温度下,反应(iii)的平衡常数
___________ (写出计算过程)。
 工业废水的处理过程。
工业废水的处理过程。 .利用
.利用 先与金属阳离子络合再被紫外光催化降解的方法去除
先与金属阳离子络合再被紫外光催化降解的方法去除 ,其机理如下:
,其机理如下:(1)
 和
和 发生络合反应生成有色物质:
发生络合反应生成有色物质:

①基态
 的价电子排布式为
的价电子排布式为②下列有关上述络合反应的说法中,正确的有
A.反应达平衡时,溶液的颜色不再变化
B.增大
 浓度,逆反应速率减小
浓度,逆反应速率减小C.
 过低不利于
过低不利于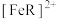 的生成
的生成 D.升高温度,该平衡正向移动
(2)紫外光催化
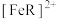 降解:
降解:若有机酸为
 ,则光催化降解反应的离子方程式为:
,则光催化降解反应的离子方程式为: ___________
___________ ___________
___________ ___________
___________ ___________
___________
 .利用有机溶剂从废水中萃取
.利用有机溶剂从废水中萃取 的方法去除
的方法去除 。该过程涉及以下反应:
。该过程涉及以下反应:(i)
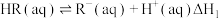
(ii)
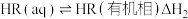
(iii)

(3)根据盖斯定律,反应
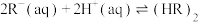 (有机相)的
(有机相)的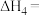
(4)水相的
 以及体系温度
以及体系温度 对
对 的平衡分配比
的平衡分配比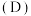 有影响。
有影响。已知:
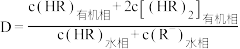 。
。①常温下,配制体积相同、
 不同、含
不同、含 粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到
粒子总浓度相同的系列溶液,分别加入等量有机溶剂萃取。测算并得到 随
随 变化的曲线如图所示。分析
变化的曲线如图所示。分析 随
随 升高而降低的原因
升高而降低的原因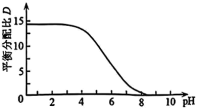
 溶液
溶液 时,
时,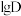 随
随 的变化曲线如图所示。
的变化曲线如图所示。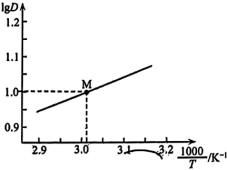
 萃取宜在
萃取宜在 经测定,在图中
经测定,在图中 点对应温度下,反应(ii)平衡常数
点对应温度下,反应(ii)平衡常数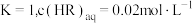 ,忽略水相中
,忽略水相中 的电离,则有机相中
的电离,则有机相中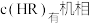
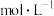 ;计算该温度下,反应(iii)的平衡常数
;计算该温度下,反应(iii)的平衡常数
您最近一年使用:0次
3 . 某小组探秘人体血液中的运载氧平衡及酸碱平衡,回答下列问题:
Ⅰ.人体运载氧平衡及CO中毒、解毒机制。
人体中的血红蛋白(Hb)能被CO结合而失去结合 能力,吸入高压氧可以使血红蛋白恢复结合
能力,吸入高压氧可以使血红蛋白恢复结合 能力,原理如下:
能力,原理如下:
ⅰ.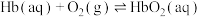

ⅱ.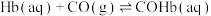

ⅱ.

ⅳ.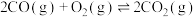

(1)
________ (用含a、b或c的代数式表示)。
(2) 也影响Hb结合
也影响Hb结合 的能力,反应如下:
的能力,反应如下:
 ,下列关于该反应的说法正确的是 。
,下列关于该反应的说法正确的是 。
(3)36.5℃时,氧饱和度[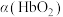 ,
,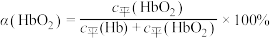 ]与氧气的平衡分压[
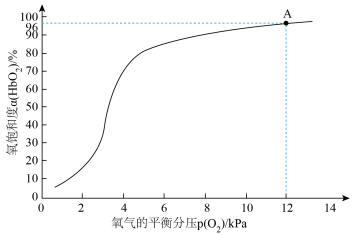
]与氧气的平衡分压[ ]关系如下图所示,计算36.5℃时A点反应ⅰ的平衡常数
]关系如下图所示,计算36.5℃时A点反应ⅰ的平衡常数
____________________ (写出计算过程;氧气的平衡浓度可用氧气的平衡分压代替)。
正常人体血液中主要含有 和形成的缓冲溶液,能缓解外界的酸碱影响而保持pH基本不变。正常人体和代谢性酸中毒病人的血气分析结果见表:
和形成的缓冲溶液,能缓解外界的酸碱影响而保持pH基本不变。正常人体和代谢性酸中毒病人的血气分析结果见表:
(4)37℃时 的水解常数
的水解常数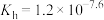 ,
,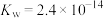 ,已知某同学血浆中
,已知某同学血浆中 ,写出人体血液中存在的水解平衡方程式
,写出人体血液中存在的水解平衡方程式___________ ;请判断该同学血液的pH是否正常________ 。(填“是”或“否”)
(5)人体酸碱平衡维持机制简要表达如下图: 会
会__________ (选填“增加”或“减少”)。
②对于重度代谢性酸中毒的病人应该采用什么治疗方法__________ 。(选填字母)
A.口服0.9% KCl溶液 B.口服5%葡萄糖溶液
C.静脉注射5% 溶液 D.静脉注射0.9% NaCl溶液
溶液 D.静脉注射0.9% NaCl溶液
Ⅰ.人体运载氧平衡及CO中毒、解毒机制。
人体中的血红蛋白(Hb)能被CO结合而失去结合
 能力,吸入高压氧可以使血红蛋白恢复结合
能力,吸入高压氧可以使血红蛋白恢复结合 能力,原理如下:
能力,原理如下:ⅰ.
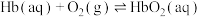

ⅱ.
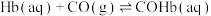

ⅱ.


ⅳ.
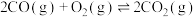

(1)

(2)
 也影响Hb结合
也影响Hb结合 的能力,反应如下:
的能力,反应如下:
 ,下列关于该反应的说法正确的是 。
,下列关于该反应的说法正确的是 。A.当 不变时,反应达到平衡 不变时,反应达到平衡 | B.若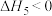 ,则该反应任意温度下能自发 ,则该反应任意温度下能自发 |
C.高氧条件下,血液中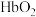 浓度增加 浓度增加 | D.人体代谢酸增加,该反应K值变大 |
(3)36.5℃时,氧饱和度[
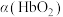 ,
,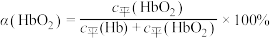 ]与氧气的平衡分压[
]与氧气的平衡分压[ ]关系如下图所示,计算36.5℃时A点反应ⅰ的平衡常数
]关系如下图所示,计算36.5℃时A点反应ⅰ的平衡常数
正常人体血液中主要含有
 和形成的缓冲溶液,能缓解外界的酸碱影响而保持pH基本不变。正常人体和代谢性酸中毒病人的血气分析结果见表:
和形成的缓冲溶液,能缓解外界的酸碱影响而保持pH基本不变。正常人体和代谢性酸中毒病人的血气分析结果见表:项目名称 | 结果浓度 | 参考范围 | |
正常人 | 代谢性酸中毒病人 | ||
| 40 | 50 | 35~45 |
| 24.2 | 19 | 23.3~24.8 |
血液酸碱度(pH) | 7.40 | 7.21 | 7.35~7.45 |
(4)37℃时
 的水解常数
的水解常数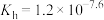 ,
,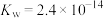 ,已知某同学血浆中
,已知某同学血浆中 ,写出人体血液中存在的水解平衡方程式
,写出人体血液中存在的水解平衡方程式(5)人体酸碱平衡维持机制简要表达如下图:
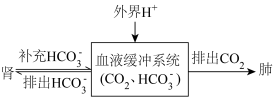
 会
会②对于重度代谢性酸中毒的病人应该采用什么治疗方法
A.口服0.9% KCl溶液 B.口服5%葡萄糖溶液
C.静脉注射5%
 溶液 D.静脉注射0.9% NaCl溶液
溶液 D.静脉注射0.9% NaCl溶液
您最近一年使用:0次
解题方法
4 .  是重要的化工原料,在生产和生活中都发挥着重要作用。
是重要的化工原料,在生产和生活中都发挥着重要作用。
(1)配合物广泛存在于自然界,其中 能与
能与 形成深蓝色
形成深蓝色 溶液。
溶液。
①基态 的3d电子轨道表示式为
的3d电子轨道表示式为_______ 。
② 的配位原子是
的配位原子是_______ ,氨气中H—N—H的键角小于配合物中H—N—H的键角,其原因是_______ 。
(2)氨是制取硝酸的重要原料。氨的催化氧化过程主要有以下两个反应:
Ⅰ.

Ⅱ.

①反应

_______ 。
②不同温度下氨催化氧化的平衡常数如下(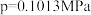 );
);
下列说法正确的是_______ 。
A.如果对反应不加控制,氨和氧气反应的最终产物主要是
B.为使反应有利于向生成更多的NO方向进行,不必关注热力学问题(平衡移动问题),需要关注动力学问题(反应速率问题)
C.在实际生产中,需采用高压氧化,以利于提高NO的产率
D.反应中需控制氨氧比、选择性催化剂的形状、气固相接触时间等
(3)已知可通过下列方法合成尿素:
第一步:
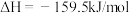
第二步:在体积为5 L的密闭容器中加入1 mol 和4 mol
和4 mol  ,在一定条件下反应进行到10 min时,测得
,在一定条件下反应进行到10 min时,测得 和尿素的物质的量均为0.25 mol,15 min后,测得
和尿素的物质的量均为0.25 mol,15 min后,测得 的物质的量为0.1 mol,如图所示。
的物质的量为0.1 mol,如图所示。
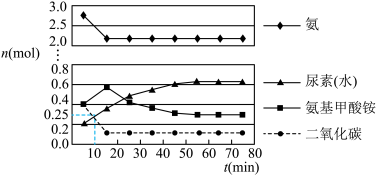
①若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则10 min内第一步反应中生成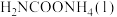 (氨基甲酸铵)的平均反应速率为
(氨基甲酸铵)的平均反应速率为_______ 。
②反应进行15分钟后,随着时间的变化,尿素和氨基甲酸铵的物质的量变化比较明显,但氨气和二氧化碳的物质的量基本不变,其主要原因是_______ ,第一步反应的平衡常数
_______ (列出算式即可)。
 是重要的化工原料,在生产和生活中都发挥着重要作用。
是重要的化工原料,在生产和生活中都发挥着重要作用。(1)配合物广泛存在于自然界,其中
 能与
能与 形成深蓝色
形成深蓝色 溶液。
溶液。①基态
 的3d电子轨道表示式为
的3d电子轨道表示式为②
 的配位原子是
的配位原子是(2)氨是制取硝酸的重要原料。氨的催化氧化过程主要有以下两个反应:
Ⅰ.


Ⅱ.


①反应


②不同温度下氨催化氧化的平衡常数如下(
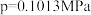 );
);| 温度(℃) | 300 | 500 | 700 | 900 | 1100 |
反应Ⅰ( ) ) | 6.3×1041 | 1.1×1026 | 2.1×1019 | 3.8×1015 | 3.4×1011 |
反应Ⅱ( ) ) | 7.3×1056 | 7.1×1034 | 2.6×1025 | 1.5×1020 | 6.7×1016 |
A.如果对反应不加控制,氨和氧气反应的最终产物主要是

B.为使反应有利于向生成更多的NO方向进行,不必关注热力学问题(平衡移动问题),需要关注动力学问题(反应速率问题)
C.在实际生产中,需采用高压氧化,以利于提高NO的产率
D.反应中需控制氨氧比、选择性催化剂的形状、气固相接触时间等
(3)已知可通过下列方法合成尿素:
第一步:

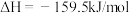
第二步:在体积为5 L的密闭容器中加入1 mol
 和4 mol
和4 mol  ,在一定条件下反应进行到10 min时,测得
,在一定条件下反应进行到10 min时,测得 和尿素的物质的量均为0.25 mol,15 min后,测得
和尿素的物质的量均为0.25 mol,15 min后,测得 的物质的量为0.1 mol,如图所示。
的物质的量为0.1 mol,如图所示。
①若用单位时间内物质的量的变化来表示固体或纯液体的反应速率,则10 min内第一步反应中生成
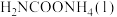 (氨基甲酸铵)的平均反应速率为
(氨基甲酸铵)的平均反应速率为②反应进行15分钟后,随着时间的变化,尿素和氨基甲酸铵的物质的量变化比较明显,但氨气和二氧化碳的物质的量基本不变,其主要原因是

您最近一年使用:0次
名校
解题方法
5 . 汞及其化合物广泛应用于医药、冶金及其他精密高新科技领域。
(1)干燥的 固体上通入
固体上通入 可反应制得
可反应制得 和
和 ,反应的化学方程式为
,反应的化学方程式为___________ 。该反应中氧化产物是___________ 。
(2)富氧燃烧烟气中 的脱除主要是通过与
的脱除主要是通过与 反应实现,反应的化学方程式为
反应实现,反应的化学方程式为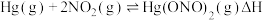
根据实验结果,有研究组提出了 与
与 的可能反应机理:
的可能反应机理:

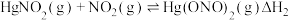

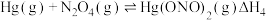
①根据盖斯定律,
___________ (写出一个代数式即可)。
②上述反应体系在一定条件下建立平衡后,下列说法正确的是___________ 。
A.增大 的浓度,可提高
的浓度,可提高 的平衡脱除率
的平衡脱除率
B.升高温度,正反应速率增大,逆反应速率减小
C.恒温恒压下充入 ,可提高原料的平衡转化率
,可提高原料的平衡转化率
D.加入催化剂,可降低反应活化能,提高脱除速率
③在常压、温度范围为15~60℃条件下,将浓度为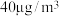 汞蒸气和
汞蒸气和 的
的 气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。
气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。 的平均脱除反应速率为
的平均脱除反应速率为___________ 
ⅱ)
___________ 0(填“>”或“<”)
④富氧燃烧烟气中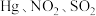 等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于
等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于 转化为
转化为 而脱除,但随着循环水量的增大,
而脱除,但随着循环水量的增大, 的去除率下降,其原因可能是
的去除率下降,其原因可能是___________ 。 溶液可用于手术刀消毒。
溶液可用于手术刀消毒。 与
与 的混合溶液中主要存在平衡:
的混合溶液中主要存在平衡:

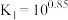
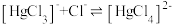
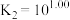
 的
的 溶液中加入
溶液中加入 固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数
固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数 随
随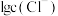 的变化如图所示
的变化如图所示 ]。
]。
①熔融状态的 不能导电,
不能导电, 是
是___________ (填“共价”或“离子”)化合物。
②A点溶液中
___________  。
。
③A点溶液中 的转化率为
的转化率为___________ (列出计算式)。
(1)干燥的
 固体上通入
固体上通入 可反应制得
可反应制得 和
和 ,反应的化学方程式为
,反应的化学方程式为(2)富氧燃烧烟气中
 的脱除主要是通过与
的脱除主要是通过与 反应实现,反应的化学方程式为
反应实现,反应的化学方程式为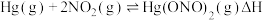
根据实验结果,有研究组提出了
 与
与 的可能反应机理:
的可能反应机理:
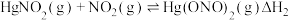

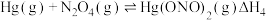
①根据盖斯定律,

②上述反应体系在一定条件下建立平衡后,下列说法正确的是
A.增大
 的浓度,可提高
的浓度,可提高 的平衡脱除率
的平衡脱除率B.升高温度,正反应速率增大,逆反应速率减小
C.恒温恒压下充入
 ,可提高原料的平衡转化率
,可提高原料的平衡转化率D.加入催化剂,可降低反应活化能,提高脱除速率
③在常压、温度范围为15~60℃条件下,将浓度为
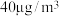 汞蒸气和
汞蒸气和 的
的 气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。
气体通入反应容器中,测得出口气流中的汞浓度随反应时间的变化如图1所示。
 的平均脱除反应速率为
的平均脱除反应速率为
ⅱ)

④富氧燃烧烟气中
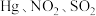 等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于
等污染物可通过配有循环水系统的分压精馏塔进行一体化脱除,污染物脱除率随循环水量的变化如图2所示。循环水的加入有利于 转化为
转化为 而脱除,但随着循环水量的增大,
而脱除,但随着循环水量的增大, 的去除率下降,其原因可能是
的去除率下降,其原因可能是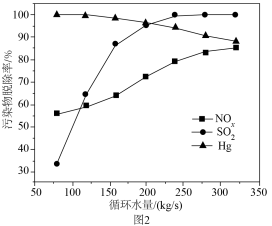
 溶液可用于手术刀消毒。
溶液可用于手术刀消毒。 与
与 的混合溶液中主要存在平衡:
的混合溶液中主要存在平衡:
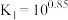
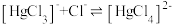
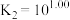
 的
的 溶液中加入
溶液中加入 固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数
固体(设溶液体积保持不变),溶液中含氯微粒的物质的量分数 随
随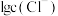 的变化如图所示
的变化如图所示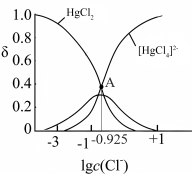
 ]。
]。①熔融状态的
 不能导电,
不能导电, 是
是②A点溶液中

 。
。③A点溶液中
 的转化率为
的转化率为
您最近一年使用:0次
2024-03-01更新
|
508次组卷
|
3卷引用:广东省广州市第二中学2023-2024学年高三上学期期末化学试卷
广东省广州市第二中学2023-2024学年高三上学期期末化学试卷广东省东莞市东华高级中学 东华松山湖高级中学 2024届高三下学期第三次模拟考试 化学试题 (已下线)大题04 化学反应原理综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
名校
解题方法
6 . 某化学兴趣小组探究 和
和 的化学性质。
的化学性质。
Ⅰ.实验准备:饱和氯水的制备
(1)图中仪器A的名称为___________ 。___________ 。
(3)实验室最适合用于处理多余氯气的是___________ (填字母)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液
Ⅱ.实验探究
①取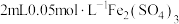 溶液于试管中,滴加3滴
溶液于试管中,滴加3滴 溶液,溶液变红色;
溶液,溶液变红色;
②取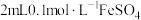 溶液于试管中,先滴加3滴
溶液于试管中,先滴加3滴 溶液,振荡,溶液无现象,再滴加3滴饱和氯水,溶液变黄色。
溶液,振荡,溶液无现象,再滴加3滴饱和氯水,溶液变黄色。
【发现问题】小组成员针对实验②中溶液未变红色,而呈现黄色的现象展开了探究。
【查阅文献】
i. 能将
能将 氧化成
氧化成 ,硫氰
,硫氰 常温下为黄色液体,易挥发,可与水发生反应:
常温下为黄色液体,易挥发,可与水发生反应: ;
;
ii.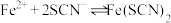 ,
,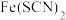 为无色配合物。
为无色配合物。
【提出猜想】猜想一 被氯水氧化成
被氯水氧化成 ,使溶液呈黄色;
,使溶液呈黄色;
猜想二 加入氯水后部分 被氧化为
被氧化为 ,
, (红色),但由于存在反应:
(红色),但由于存在反应: ,实验②生成的
,实验②生成的 浓度比实验①的小,
浓度比实验①的小, 溶液在浓度较低时呈黄色。
溶液在浓度较低时呈黄色。
【验证猜想】
(4)为验证猜想,小组成员设计了以下实验,请补充表格中的操作及现象
【提出质疑】
(5)甲同学提出,实验④并不能证明猜想一正确,理由是___________ 。
【再次探究】
(6)小组成员进行进一步探究,请完成表格中的实验操作及现象
【得出结论】
(7)由实验结论可以判断:本实验条件下还原性强弱:
___________  (填“强于”“弱于”或“等于”)。
(填“强于”“弱于”或“等于”)。
 和
和 的化学性质。
的化学性质。Ⅰ.实验准备:饱和氯水的制备
(1)图中仪器A的名称为
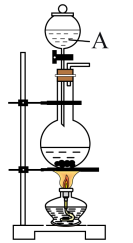
(3)实验室最适合用于处理多余氯气的是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. 溶液
溶液Ⅱ.实验探究
①取
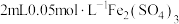 溶液于试管中,滴加3滴
溶液于试管中,滴加3滴 溶液,溶液变红色;
溶液,溶液变红色;②取
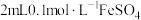 溶液于试管中,先滴加3滴
溶液于试管中,先滴加3滴 溶液,振荡,溶液无现象,再滴加3滴饱和氯水,溶液变黄色。
溶液,振荡,溶液无现象,再滴加3滴饱和氯水,溶液变黄色。【发现问题】小组成员针对实验②中溶液未变红色,而呈现黄色的现象展开了探究。
【查阅文献】
i.
 能将
能将 氧化成
氧化成 ,硫氰
,硫氰 常温下为黄色液体,易挥发,可与水发生反应:
常温下为黄色液体,易挥发,可与水发生反应: ;
;ii.
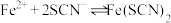 ,
,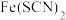 为无色配合物。
为无色配合物。【提出猜想】猜想一
 被氯水氧化成
被氯水氧化成 ,使溶液呈黄色;
,使溶液呈黄色;猜想二 加入氯水后部分
 被氧化为
被氧化为 ,
, (红色),但由于存在反应:
(红色),但由于存在反应: ,实验②生成的
,实验②生成的 浓度比实验①的小,
浓度比实验①的小, 溶液在浓度较低时呈黄色。
溶液在浓度较低时呈黄色。【验证猜想】
(4)为验证猜想,小组成员设计了以下实验,请补充表格中的操作及现象
| 实验序号 | 实验操作 | 现象 | 实验结论 |
| ③ | 取少量实验①的溶液于试管中, | 猜想二正确 | |
| ④ | 取少量实验②的溶液于试管中,滴加3滴饱和 溶液 溶液 | 溶液变浑浊 | 猜想一也正确 |
【提出质疑】
(5)甲同学提出,实验④并不能证明猜想一正确,理由是
【再次探究】
(6)小组成员进行进一步探究,请完成表格中的实验操作及现象
| 实验序号 | 实验操作 | 现象 |
| ⑤ | 滴加3滴蒸馏水 | 无明显现象 | |
| ⑥ | 无明显现象 | ||
| ⑦ | 滴加3滴饱和氯水 | 溶液变橙红色 | |
| ⑧ | 滴加3滴 溶液 溶液 | ||
| 得出结论 | i.由实验⑥的现象可以判断:猜想一不正确, ii.结合实验⑤⑦⑧的现象可以判断:猜想二正确。 | ||
【得出结论】
(7)由实验结论可以判断:本实验条件下还原性强弱:

 (填“强于”“弱于”或“等于”)。
(填“强于”“弱于”或“等于”)。
您最近一年使用:0次
2024-01-22更新
|
490次组卷
|
3卷引用:广东省深圳市龙岗区2023-2024学年高三上学期1月期末考试化学试题
广东省深圳市龙岗区2023-2024学年高三上学期1月期末考试化学试题广东省东莞市东华高级中学 东华松山湖高级中学 2024届高三下学期第三次模拟考试 化学试题 (已下线)大题02 化学实验综合题(分类过关)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
7 . 下列事实中,不能用化学平衡移动原理解释的是
A.棕色的 体系加压后,颜色先变深后逐渐变浅 体系加压后,颜色先变深后逐渐变浅 |
| B.在配制硫酸亚铁溶液时往往要加入少量铁粉 |
| C.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小 |
| D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 |
您最近一年使用:0次
名校
解题方法
8 . 工业上利用黄铁矿(FeS2)制取硫酸,其反应流程如下:

| A.反应①矿石粉碎的目的是提高反应速率 |
| B.反应②中即使通入过量的氧气,也不能将SO2全部转化成SO3 |
| C.接触室选择500℃左右的温度是因为比常温更有利于合成SO3 |
| D.过量的氨水吸收SO2的化学方程式:2NH3·H2O+SO2=(NH4)2SO3+H2O |
您最近一年使用:0次
2024-03-20更新
|
83次组卷
|
2卷引用:广东省惠州一中实验学校2023-2024学年高二上学期期中考试化学试题
9 . 下列对化学平衡移动的分析中,不正确 的是
①已达平衡的反应 ,当仅增加反应物物质的量时,平衡一定向正反应方向移动
,当仅增加反应物物质的量时,平衡一定向正反应方向移动
②已达平衡的反应 ,当仅增大
,当仅增大 的浓度时,平衡向正反应方向移动,
的浓度时,平衡向正反应方向移动, 的转化率升高
的转化率升高
③有气体参加的反应达平衡时,仅缩小容器容积,平衡一定向气体总系数增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
①已达平衡的反应
 ,当仅增加反应物物质的量时,平衡一定向正反应方向移动
,当仅增加反应物物质的量时,平衡一定向正反应方向移动②已达平衡的反应
 ,当仅增大
,当仅增大 的浓度时,平衡向正反应方向移动,
的浓度时,平衡向正反应方向移动, 的转化率升高
的转化率升高③有气体参加的反应达平衡时,仅缩小容器容积,平衡一定向气体总系数增大的方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡一定不移动
| A.①④ | B.①②③ | C.②③④ | D.①②③④ |
您最近一年使用:0次
2023-12-09更新
|
196次组卷
|
6卷引用:广东省广州市培英中学2023-2024学年高二上学期期中考试化学试题
广东省广州市培英中学2023-2024学年高二上学期期中考试化学试题北京市昌平区第二中学2023-2024高二上学期期中考试化学试题(已下线)寒假作业03 化学平衡-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)江西省上饶市广丰中学2023-2024学年高二上学期12月考试化学试卷(已下线)专题03 化学平衡-【寒假自学课】2024年高二化学寒假提升学与练(人教版2019)安徽省淮北市第一中学2023-2024学年高二下学期寒假自主学习质量评估化学试题
名校
10 . 已知:可逆反应2SO2(g) + O2(g)⇌2SO3(g) △H<0,在一密闭容器中,该反应已达到平衡状态,按要求完成下列内容:
(1)2mol SO2(g) 和 1mol O2(g)的总能量_______ 2mol SO3(g)的总能量(填写“>”、“<”或“=”)
(2)保持容器体积不变,升高温度,平衡_______ 移动(填写“正向”、“逆向”或“不”)
(3)保持温度不变,压缩体积,平衡_______ 移动(填写“正向”、“逆向”或“不”),平衡常数_______ (填写“增大”、“减小”或“不变”)
(4)常温下, 溶液中,
溶液中,
_______ (填“>”“<”或“=”) ;
; 溶液的
溶液的
_______ 。
(5) 溶液呈
溶液呈_______ (填“酸”“碱”或“中”)性,其原因是_______ (用离子方程式表示)。
(1)2mol SO2(g) 和 1mol O2(g)的总能量
(2)保持容器体积不变,升高温度,平衡
(3)保持温度不变,压缩体积,平衡
(4)常温下,
 溶液中,
溶液中,
 ;
; 溶液的
溶液的
(5)
 溶液呈
溶液呈
您最近一年使用:0次