1 .  的资源化不仅能减少
的资源化不仅能减少 排放,还能有效利用碳资源。
排放,还能有效利用碳资源。
(1) 制取低碳醇的反应如下:
制取低碳醇的反应如下:
反应Ⅰ:
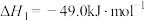
反应Ⅱ:

则 与
与 合成
合成 的热化学方程式为
的热化学方程式为___________ ;在密闭容器中,按 充入
充入 和
和 ,平衡时
,平衡时 、含碳物质的物质的量分数随温度变化的曲线如图所示,图中表示
、含碳物质的物质的量分数随温度变化的曲线如图所示,图中表示 组分的是曲线
组分的是曲线___________ (填序号)。

(2)250℃时,向 恒容密闭容器中通入
恒容密闭容器中通入 、
、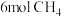 ,发生如下反应:
,发生如下反应: 。平衡时,各组分体积分数如下表所示。
。平衡时,各组分体积分数如下表所示。
该条件下, 的平衡转化率为
的平衡转化率为___________ ;向平衡体系中再通入 、
、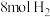 ,平衡
,平衡___________ (填“正向移动”、“逆向移动”或“不移动”)。
(3)用 溶液吸收
溶液吸收 可得
可得 溶液。室温下,
溶液。室温下,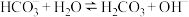 的平衡常数K=
的平衡常数K=___________ [已知: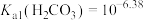 ]。在密闭容器中,向含有催化剂的
]。在密闭容器中,向含有催化剂的 溶液中通入
溶液中通入 制备
制备 ,测得
,测得 的转化率随温度的变化如图所示。在40℃至80℃过程中,转化率迅速上升的原因是
的转化率随温度的变化如图所示。在40℃至80℃过程中,转化率迅速上升的原因是___________ 。

 的资源化不仅能减少
的资源化不仅能减少 排放,还能有效利用碳资源。
排放,还能有效利用碳资源。(1)
 制取低碳醇的反应如下:
制取低碳醇的反应如下:反应Ⅰ:

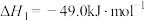
反应Ⅱ:


则
 与
与 合成
合成 的热化学方程式为
的热化学方程式为 充入
充入 和
和 ,平衡时
,平衡时 、含碳物质的物质的量分数随温度变化的曲线如图所示,图中表示
、含碳物质的物质的量分数随温度变化的曲线如图所示,图中表示 组分的是曲线
组分的是曲线
(2)250℃时,向
 恒容密闭容器中通入
恒容密闭容器中通入 、
、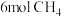 ,发生如下反应:
,发生如下反应: 。平衡时,各组分体积分数如下表所示。
。平衡时,各组分体积分数如下表所示。| 物质 |  |  | CO |  |
| 体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
 的平衡转化率为
的平衡转化率为 、
、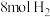 ,平衡
,平衡(3)用
 溶液吸收
溶液吸收 可得
可得 溶液。室温下,
溶液。室温下,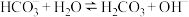 的平衡常数K=
的平衡常数K=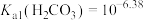 ]。在密闭容器中,向含有催化剂的
]。在密闭容器中,向含有催化剂的 溶液中通入
溶液中通入 制备
制备 ,测得
,测得 的转化率随温度的变化如图所示。在40℃至80℃过程中,转化率迅速上升的原因是
的转化率随温度的变化如图所示。在40℃至80℃过程中,转化率迅速上升的原因是
您最近一年使用:0次
名校
解题方法
2 . 甲醇是一种可再生能源。工业上可用CO和 合成甲醇:
合成甲醇: 。一定条件下向2L的密闭容器中充入1molCO和
。一定条件下向2L的密闭容器中充入1molCO和 发生反应,CO的平衡转化率与温度、压强的关系如图所示:
发生反应,CO的平衡转化率与温度、压强的关系如图所示:
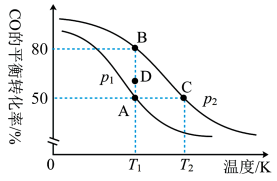
(1)该反应的
_______ 0、
_______ 0(填“>”“<”或“=”),_______ (填“低温”或“高温”)有利于该反应自发进行。
(2)生产中有利于增大CO平衡转化率的措施有_______ 。(至少写出3条)
(3)①A、B、C三点平衡常数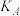 、
、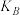 、
、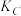 的大小关系是
的大小关系是_______ 。
②压强
_______  (填“>”“<”或“=”);若
(填“>”“<”或“=”);若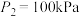 ,计算B点的
,计算B点的
_______ 。(要求写出计算过程,结果保留2位有效数字; 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。
③在 和
和 条件下,由D点到A点过程中,正、逆反应速率之间的关系:
条件下,由D点到A点过程中,正、逆反应速率之间的关系:
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
 合成甲醇:
合成甲醇: 。一定条件下向2L的密闭容器中充入1molCO和
。一定条件下向2L的密闭容器中充入1molCO和 发生反应,CO的平衡转化率与温度、压强的关系如图所示:
发生反应,CO的平衡转化率与温度、压强的关系如图所示:
(1)该反应的


(2)生产中有利于增大CO平衡转化率的措施有
(3)①A、B、C三点平衡常数
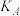 、
、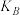 、
、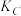 的大小关系是
的大小关系是②压强

 (填“>”“<”或“=”);若
(填“>”“<”或“=”);若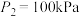 ,计算B点的
,计算B点的
 为以分压表示的平衡常数,分压=总压×物质的量分数)。
为以分压表示的平衡常数,分压=总压×物质的量分数)。③在
 和
和 条件下,由D点到A点过程中,正、逆反应速率之间的关系:
条件下,由D点到A点过程中,正、逆反应速率之间的关系:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
名校
解题方法
3 . 从低品位铜镍矿(含有Fe2O3、FeO、MgO、CuO等杂质)资源中提取镍和铜的一种工艺流程如下:
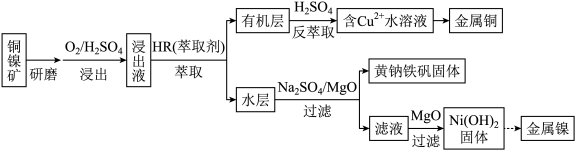
(1)上述流程中,加快反应速率的措施是_______ 。
(2)萃取时发生反应:Cu2+ + 2HR CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:
CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:_______ 。
(3)黄钠铁矾[NaFe3(OH)6(SO4)2]比Fe(OH)3更易形成沉淀。反应终点pH与Fe3+、Ni2+沉淀率的关系如下表。
① 生成黄钠铁矾的离子方程式是_______ 。
② 沉淀Fe3+时最适宜选用的反应终点pH是_______ 。
(4)第二次使用MgO调节pH使Ni2+沉淀完全,宜将pH调节至_______ (填序号)(已知Ksp[Ni(OH)2 ] = 2.1×10-15)。
a.6~7 b.9~10 c.11~12

(1)上述流程中,加快反应速率的措施是
(2)萃取时发生反应:Cu2+ + 2HR
 CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:
CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:(3)黄钠铁矾[NaFe3(OH)6(SO4)2]比Fe(OH)3更易形成沉淀。反应终点pH与Fe3+、Ni2+沉淀率的关系如下表。
| 反应终点pH | 沉淀率/% | |
| Fe3+ | Ni2+ | |
| 1.5 | 94.04 | 0.19 |
| 2.5 | 99.21 | 0.56 |
| 3.8 | 99.91 | 3.31 |
② 沉淀Fe3+时最适宜选用的反应终点pH是
(4)第二次使用MgO调节pH使Ni2+沉淀完全,宜将pH调节至
a.6~7 b.9~10 c.11~12
您最近一年使用:0次
名校
解题方法
4 . 设反应①Fe(s) + CO2(g) FeO(s) + CO(g) 的平衡常数为K1,反应②Fe(s) + H2O(g)
FeO(s) + CO(g) 的平衡常数为K1,反应②Fe(s) + H2O(g) FeO(s) + H2(g) 的平衡常数为K2。在不同温度下,K1和K2的值如下:
FeO(s) + H2(g) 的平衡常数为K2。在不同温度下,K1和K2的值如下:
(1)现有反应③ H2(g) + CO2(g) H2O(g) + CO(g),写出该反应的平衡常数K3的数学表达式K3=
H2O(g) + CO(g),写出该反应的平衡常数K3的数学表达式K3=______________ ,根据反应①与②,可推导出K1、K2和K3之间的关系式为______________ 。
(2)从上表和K1、K2和K3之间的关系可以推断:反应①是___________ (填“吸”、“ 放”,下同)热反应,反应③是___________ 热反应。
(3)图表示该反应③在时刻t1达到平衡,在时刻t2因改变某个条件而发生变化的情况:
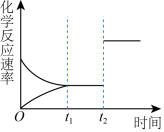
①图中时刻t2时改变的条件是_________ (写出一种即可),
②973K时测得反应①中CO2和CO 的浓度分别为0.025mol/L和0.1mol/L,此时反应①是否处于化学平衡状态_______ (选填“是”或“否”), 化学反应速度v(正)_________ v(逆)(选填“>”、“<”或“=”)。
 FeO(s) + CO(g) 的平衡常数为K1,反应②Fe(s) + H2O(g)
FeO(s) + CO(g) 的平衡常数为K1,反应②Fe(s) + H2O(g) FeO(s) + H2(g) 的平衡常数为K2。在不同温度下,K1和K2的值如下:
FeO(s) + H2(g) 的平衡常数为K2。在不同温度下,K1和K2的值如下:| 温度 | K1 | K2 |
| 973K | 1.47 | 2.38 |
| 1173K | 2.15 | 1.67 |
(1)现有反应③ H2(g) + CO2(g)
 H2O(g) + CO(g),写出该反应的平衡常数K3的数学表达式K3=
H2O(g) + CO(g),写出该反应的平衡常数K3的数学表达式K3=(2)从上表和K1、K2和K3之间的关系可以推断:反应①是
(3)图表示该反应③在时刻t1达到平衡,在时刻t2因改变某个条件而发生变化的情况:

①图中时刻t2时改变的条件是
②973K时测得反应①中CO2和CO 的浓度分别为0.025mol/L和0.1mol/L,此时反应①是否处于化学平衡状态
您最近一年使用:0次



