名校
解题方法
1 . “绿水青山就是金山银山”,现在人们越来越注重对环境的保护,污水的处理和废旧电池的回收成为环境保护的重要课题。
Ⅰ.工业上常用还原沉淀法处理含铬废水(Cr2O 和CrO
和CrO ),其流程为
),其流程为
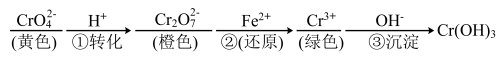
已知步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s) Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)·c3(OH-)=10-32。
Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)·c3(OH-)=10-32。
(1)步骤①中存在反应2CrO +2H+
+2H+ Cr2O
Cr2O +H2O,若向K2Cr2O7溶液中加NaOH浓溶液,能出现的现象是
+H2O,若向K2Cr2O7溶液中加NaOH浓溶液,能出现的现象是_______ ,原因是 _______ 。
(2)步骤③中,当将溶液的pH调节至_______ 时,可认为废水中的铬元素已基本除尽。(当溶液中c(Cr3+)≤10-5mol·L-1时,可视作该离子沉淀完全)
Ⅱ.镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:
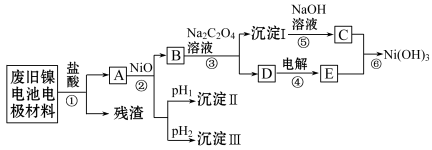
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+;
②某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如表所示:
回答下列问题:
(3)根据上表数据判断步骤②依次析出沉淀Ⅱ_______ 和沉淀Ⅲ_______ (填化学式),则pH1_______ pH2(填“>”“=”或“<”)。
(4)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则③的化学方程式是_______ 。第③步反应后的操作名称是 _______ 。
(5)试写出⑥的离子方程式_______ 。
Ⅰ.工业上常用还原沉淀法处理含铬废水(Cr2O
 和CrO
和CrO ),其流程为
),其流程为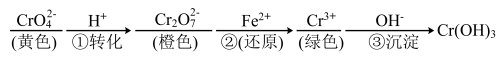
已知步骤③生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)
 Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)·c3(OH-)=10-32。
Cr3+(aq)+3OH-(aq) Ksp=c(Cr3+)·c3(OH-)=10-32。(1)步骤①中存在反应2CrO
 +2H+
+2H+ Cr2O
Cr2O +H2O,若向K2Cr2O7溶液中加NaOH浓溶液,能出现的现象是
+H2O,若向K2Cr2O7溶液中加NaOH浓溶液,能出现的现象是(2)步骤③中,当将溶液的pH调节至
Ⅱ.镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:

已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+;
②某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如表所示:
| M(OH)n | Ksp | pH | |
| 开始沉淀 | 沉淀完全 | ||
| Al(OH)3 | 1.9×10-23 | 3.43 | 4.19 |
| Fe(OH)3 | 3.8×10-38 | 2.53 | 2.94 |
| Ni(OH)2 | 1.6×10-14 | 7.60 | 9.75 |
(3)根据上表数据判断步骤②依次析出沉淀Ⅱ
(4)已知溶解度:NiC2O4>NiC2O4·H2O>NiC2O4·2H2O,则③的化学方程式是
(5)试写出⑥的离子方程式
您最近一年使用:0次
2 . 变化观念与平衡思想是化学学科核心素养之一。下列实验事实不能用平衡移动原理解释的是
| A.由H2、I2(g)、HI组成的平衡体系,加压后颜色加深 |
| B.工业合成氨过程中及时分离出氨气,有利于提高原料转化率 |
| C.通常在硫酸铁或硫酸亚铁溶液中加入少许稀硫酸,抑制其水解 |
| D.久置的氯水黄绿色会褪去 |
您最近一年使用:0次
名校
解题方法
3 . 根据下列实验设计,回答问题:
(1)利用实验(Ⅰ)探究锌与0.1mol/L硫酸和2mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项):_______ 。

(2)实验(Ⅱ)探究浓度对化学化学平衡影响。已知: (橙色)
(橙色) (黄色)
(黄色) 推测D试管中实验现象为
推测D试管中实验现象为_______ ,用平衡移动原理解释原因:______________ 。

(3)实验(Ⅲ)目的是探究浓度对反应速率的影响,实验中发生反应:
 ,某小组也用酸性
,某小组也用酸性 溶液和草酸(
溶液和草酸( )溶液进行实验,实验操作及现象如下表:
)溶液进行实验,实验操作及现象如下表:

①由实验ⅰ、实验ⅱ可得出的结论是_______ 。
②关于实验ⅱ中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的 对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
提供的试剂:0.01mol/L酸性 溶液,0.1mol/L草酸溶液,3mol/L硫酸,
溶液,0.1mol/L草酸溶液,3mol/L硫酸, 溶液,
溶液, 固体,蒸馏水。
固体,蒸馏水。
补全实验ⅲ的操作:向试管中先加入5mL 0.01mol/L酸性 溶液,
溶液,_______ ,最后加入5mL 0.1mol/L草酸溶液。
③基于以上实验与分析,推测实验(Ⅲ)设计_______ (填“能”或“不能”)达到实验目的。
(1)利用实验(Ⅰ)探究锌与0.1mol/L硫酸和2mol/L硫酸反应的速率,可以测定收集一定体积氢气所用的时间。此方法需要控制的变量有(写出1项):

(2)实验(Ⅱ)探究浓度对化学化学平衡影响。已知:
 (橙色)
(橙色) (黄色)
(黄色) 推测D试管中实验现象为
推测D试管中实验现象为
(3)实验(Ⅲ)目的是探究浓度对反应速率的影响,实验中发生反应:

 ,某小组也用酸性
,某小组也用酸性 溶液和草酸(
溶液和草酸( )溶液进行实验,实验操作及现象如下表:
)溶液进行实验,实验操作及现象如下表:
| 编号 | 实验操作 | 实验现象 |
| ⅰ | 向一支试管中先加入5mL 0.01mol/L酸性 溶液,再加入1滴3mol/L硫酸和9滴蒸馏水,最后加入5mL 0.1mol/L草酸溶液 溶液,再加入1滴3mol/L硫酸和9滴蒸馏水,最后加入5mL 0.1mol/L草酸溶液 | 前10min内溶液紫色无明显变化,后颜色逐渐变浅,30min后几乎变为无色 |
| ⅱ | 向另一支试管中先加入5mL 0.01mol/L酸性 溶液,再加入10滴3mol/L硫酸,最后加入5mL 0.1mol/L草酸溶液 溶液,再加入10滴3mol/L硫酸,最后加入5mL 0.1mol/L草酸溶液 | 80s内溶液紫色无明显变化,后颜色迅速变浅,约150s后几乎变为无色 |
②关于实验ⅱ中80s后溶液颜色迅速变浅的原因,该小组提出了猜想:该反应中生成的
 对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。
对反应有催化作用。利用提供的试剂设计实验ⅲ,验证猜想。提供的试剂:0.01mol/L酸性
 溶液,0.1mol/L草酸溶液,3mol/L硫酸,
溶液,0.1mol/L草酸溶液,3mol/L硫酸, 溶液,
溶液, 固体,蒸馏水。
固体,蒸馏水。补全实验ⅲ的操作:向试管中先加入5mL 0.01mol/L酸性
 溶液,
溶液,③基于以上实验与分析,推测实验(Ⅲ)设计
您最近一年使用:0次
解题方法
4 . K2Cr2O7溶液中存在平衡: (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+ ΔH<0。取2 mL 0.1 mol/L K2Cr2O7,溶液进行以下实验,溶液颜色变浅且平衡正向移动的是
(黄色)+2H+ ΔH<0。取2 mL 0.1 mol/L K2Cr2O7,溶液进行以下实验,溶液颜色变浅且平衡正向移动的是
 (橙色)+H2O
(橙色)+H2O 2
2 (黄色)+2H+ ΔH<0。取2 mL 0.1 mol/L K2Cr2O7,溶液进行以下实验,溶液颜色变浅且平衡正向移动的是
(黄色)+2H+ ΔH<0。取2 mL 0.1 mol/L K2Cr2O7,溶液进行以下实验,溶液颜色变浅且平衡正向移动的是| A.加入KCl(s) | B.滴加少量6mol/LKOH溶液 |
| C.加热溶液 | D.滴加少量6mol/LH2SO4溶液 |
您最近一年使用:0次
5 . 某温度下,反应 CH2=CH2(g)+H2O(g)⇌CH3CH2OH(g)在密闭容器中达到平衡。下列说法正确的是
| A.加压,υ正增大,υ逆减小,平衡正向移动 |
| B.加入催化剂,CH2=CH2的平衡转化率增大 |
| C.再充入一定量CH2=CH2,CH2=CH2的平衡转化率增大 |
| D.分离出CH3CH2OH(g),υ逆减小,平衡正向移动 |
您最近一年使用:0次
名校
6 . 下列事实不能用勒夏特列原理解释的是
| A.用排饱和食盐水的方法收集氯气 |
B.向含有 的红色溶液中加铁粉,振荡,溶液颜色变浅或褪去 的红色溶液中加铁粉,振荡,溶液颜色变浅或褪去 |
C.增大压强(减小容器的容积), 与 与 混合气体的平衡体系颜色先变深后变浅 混合气体的平衡体系颜色先变深后变浅 |
D.增大压强(减小容器的容积), 、 、 、HI混合气体的平衡体系颜色变深 、HI混合气体的平衡体系颜色变深 |
您最近一年使用:0次
名校
7 . 关于合成氨工业的说法中不正确的是
A.由于 易液化, 易液化, 、 、 可循环使用,则总的说来,氨的产率很高 可循环使用,则总的说来,氨的产率很高 |
| B.工业上采用高温条件的目的是为了提高平衡转化率 |
| C.对原料气进行压缩可增大原料气的转化率 |
| D.使用催化剂能加快该反应速率的原因是降低了活化能 |
您最近一年使用:0次
8 . 根据实验目的,下列实验及现象、结论都正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 比较S、C的非金属性 | 分别测定等物质的量浓度的H2SO3和H2CO3溶液的pH,后者较大 | 证明非金属性:S>C |
| B | 检验某溶液中是否含二价铁离子 | 取少量溶液于试管中,滴入酸性高锰酸钾溶液,紫色褪去 | 证明溶液含有二价铁 |
| C | 探究氢离子浓度对 、 、 相互转化的影响 相互转化的影响 | 向K2Cr2O7溶液中缓慢滴加硫酸,黄色变为橙红色 | 增大氢离子浓度,转化平衡向生成 的方向移动 的方向移动 |
| D | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,产生无色气体 | 乙醇中含有水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-11-21更新
|
101次组卷
|
3卷引用:广东省茂名市电白区2022-2023学年高二上学期期中选择性考试化学试题
名校
9 . 已知: 溶液中存在如下平衡:
溶液中存在如下平衡: (蓝色)
(蓝色)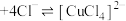 (黄色)
(黄色)
 。某同学通过实验研究氯化铜溶液颜色的变化。下列说法不正确的是。
。某同学通过实验研究氯化铜溶液颜色的变化。下列说法不正确的是。

 溶液中存在如下平衡:
溶液中存在如下平衡: (蓝色)
(蓝色)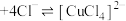 (黄色)
(黄色)
 。某同学通过实验研究氯化铜溶液颜色的变化。下列说法不正确的是。
。某同学通过实验研究氯化铜溶液颜色的变化。下列说法不正确的是。
| A.①溶液呈蓝色 | B.②中黄色物质是 |
| C.若对①加热,溶液可能会变为绿色 | D.若取②中溶液稀释,溶液不可能变为蓝色 |
您最近一年使用:0次
2022-11-16更新
|
123次组卷
|
3卷引用:广东省深圳市校联盟2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
10 . “哈伯法”合成氨的反应: △H,相关键能数据如下表:
△H,相关键能数据如下表:
(1)ΔH=_______ kJ·mol-1。
(2)在恒温恒容密闭容器中进行工业合成氨反应,下列能表示达到平衡状态的是_______(填序号)。
(3)结合平衡移动原理解释“哈伯法”中“分离液氨”的目的:_______ 。
(4)向恒温恒容的密闭容器中按1:3体积比通入 和
和 ,反应达平衡时
,反应达平衡时 的体积分数为25.0%,则
的体积分数为25.0%,则 的平衡转化率
的平衡转化率
_______ 。第一次平衡后充入适量 ,再次平衡时
,再次平衡时 的体积分数
的体积分数_______ 25.0%。(填“大于”“小于”或“等于”)
 △H,相关键能数据如下表:
△H,相关键能数据如下表:| 化学键 | N≡N | H-H | N-H |
键能( ) ) | 946.0 | 436.0 | 390.8 |
(2)在恒温恒容密闭容器中进行工业合成氨反应,下列能表示达到平衡状态的是_______(填序号)。
| A.单位时间内断开3a个H-H键的同时形成6a个N-H键 |
| B.混合气体的平均相对分子质量不再发生变化 |
| C.混合气体的密度不再发生变化 |
D.反应容器中 , , 的物质的量的比值不再发生变化 的物质的量的比值不再发生变化 |
(4)向恒温恒容的密闭容器中按1:3体积比通入
 和
和 ,反应达平衡时
,反应达平衡时 的体积分数为25.0%,则
的体积分数为25.0%,则 的平衡转化率
的平衡转化率
 ,再次平衡时
,再次平衡时 的体积分数
的体积分数
您最近一年使用:0次



