名校
解题方法
1 . 氟碳铈矿(主要成分为 )是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图:
)是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图:

(1) 中
中 的化合价为
的化合价为___________ ;氧化焙烧时不能使用陶瓷容器的原因是产物 会腐蚀
会腐蚀 生成
生成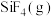 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(2)氧化焙烧后的产物之一为 ,则酸浸时发生反应的离子方程式为
,则酸浸时发生反应的离子方程式为___________ 。
(3)操作I的名称为___________ ;有机物 能将
能将 从水溶液中提取出来,该过程可表示为
从水溶液中提取出来,该过程可表示为 。向
。向 中加入稀硫酸能获得较纯的含
中加入稀硫酸能获得较纯的含 水溶液,从平衡移动角度解释其原因
水溶液,从平衡移动角度解释其原因___________ 。
(4)写出向 悬浊液中通入氧气得到产品
悬浊液中通入氧气得到产品 的化学方程式
的化学方程式___________ 。
 )是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图:
)是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图:
(1)
 中
中 的化合价为
的化合价为 会腐蚀
会腐蚀 生成
生成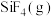 ,该反应的化学方程式为
,该反应的化学方程式为(2)氧化焙烧后的产物之一为
 ,则酸浸时发生反应的离子方程式为
,则酸浸时发生反应的离子方程式为(3)操作I的名称为
 能将
能将 从水溶液中提取出来,该过程可表示为
从水溶液中提取出来,该过程可表示为 。向
。向 中加入稀硫酸能获得较纯的含
中加入稀硫酸能获得较纯的含 水溶液,从平衡移动角度解释其原因
水溶液,从平衡移动角度解释其原因(4)写出向
 悬浊液中通入氧气得到产品
悬浊液中通入氧气得到产品 的化学方程式
的化学方程式
您最近一年使用:0次
名校
解题方法
2 . 探究甲醇对丙烷制丙烯的影响。丙烷制烯烃过程主要发生的反应有
ⅰ.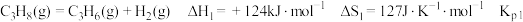
ⅱ.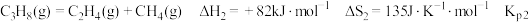
ⅲ.
已知: 为用气体分压表示的平衡常数,分压=物质的量分数×总压。在
为用气体分压表示的平衡常数,分压=物质的量分数×总压。在 下,丙烷单独进料时,平衡体系中各组分的体积分数
下,丙烷单独进料时,平衡体系中各组分的体积分数 见下表。
见下表。
(1)比较反应自发进行(∆G=∆H-T∆S<0)的最低温度,反应ⅰ_____ 反应 ⅱ(填“>”或“<”)。
(2)①从初始投料到达到平衡,反应 ⅰ、ⅱ、ⅲ 的丙烷消耗的平均速率从大到小的顺序为:_____ 。
②平衡体系中检测不到 ,可认为存在反应:
,可认为存在反应: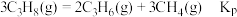 ,下列相关说法正确的是
,下列相关说法正确的是_____ (填标号)。
a.
b.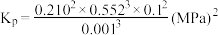
c.使用催化剂,可提高丙烯的平衡产率
d.平衡后再通入少量丙烷,可提高丙烯的体积分数
③由表中数据推算:丙烯选择性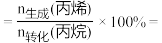
_____ (列出计算式)。
(3)丙烷甲醇共进料时,还发生反应:ⅳ.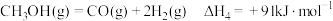 ,在
,在 下,平衡体系中各组分体积分数与进料比的关系如图所示。
下,平衡体系中各组分体积分数与进料比的关系如图所示。
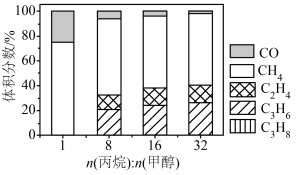
①进料比n(丙烷):n(甲醇) 时,体系总反应:
时,体系总反应: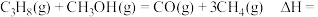
______  。
。
②随着甲醇投料增加,平衡体系中丙烯的体积分数降低的原因是______ 。
ⅰ.
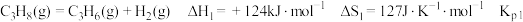
ⅱ.
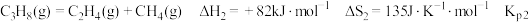
ⅲ.

已知:
 为用气体分压表示的平衡常数,分压=物质的量分数×总压。在
为用气体分压表示的平衡常数,分压=物质的量分数×总压。在 下,丙烷单独进料时,平衡体系中各组分的体积分数
下,丙烷单独进料时,平衡体系中各组分的体积分数 见下表。
见下表。| 物质 | 丙烯 | 乙烯 | 甲烷 | 丙烷 | 氢气 |
| 体积分数(%) | 21 | 23.7 | 55.2 | 0.1 | 0 |
(1)比较反应自发进行(∆G=∆H-T∆S<0)的最低温度,反应ⅰ
(2)①从初始投料到达到平衡,反应 ⅰ、ⅱ、ⅲ 的丙烷消耗的平均速率从大到小的顺序为:
②平衡体系中检测不到
 ,可认为存在反应:
,可认为存在反应: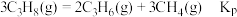 ,下列相关说法正确的是
,下列相关说法正确的是a.

b.
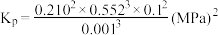
c.使用催化剂,可提高丙烯的平衡产率
d.平衡后再通入少量丙烷,可提高丙烯的体积分数
③由表中数据推算:丙烯选择性
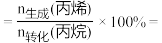
(3)丙烷甲醇共进料时,还发生反应:ⅳ.
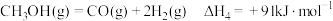 ,在
,在 下,平衡体系中各组分体积分数与进料比的关系如图所示。
下,平衡体系中各组分体积分数与进料比的关系如图所示。
①进料比n(丙烷):n(甲醇)
 时,体系总反应:
时,体系总反应: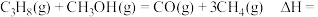
 。
。②随着甲醇投料增加,平衡体系中丙烯的体积分数降低的原因是
您最近一年使用:0次
名校
3 . 下列事实中,不能用勒夏特列原理解释的是
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
③实验室常用排饱和食盐水的方法收集氯气
④棕红色NO2加压后颜色先变深后变浅
⑤加入催化剂有利于合成氨的反应
⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深
⑦500℃时比室温更有利于合成氨的反应
⑧将混合气体中的氨液化有利于合成氨反应
①Fe(SCN)3溶液中加入固体KSCN后颜色变深
②向稀盐酸中加入少量蒸馏水,盐酸中氢离子浓度降低
③实验室常用排饱和食盐水的方法收集氯气
④棕红色NO2加压后颜色先变深后变浅
⑤加入催化剂有利于合成氨的反应
⑥由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深
⑦500℃时比室温更有利于合成氨的反应
⑧将混合气体中的氨液化有利于合成氨反应
| A.①②⑥⑧ | B.①③⑥⑧ | C.②⑤⑥⑦ | D.②③⑦⑧ |
您最近一年使用:0次
名校
解题方法
4 . I:室温下,通过下列实验探究 溶液的性质。
溶液的性质。
依据实验操作和现象,回答下列问题:
(1)向0.1mol/L 溶液滴入酚酞溶液,观察到的现象是
溶液滴入酚酞溶液,观察到的现象是___________ ,原因___________ (用离子方程式表示)。
(2)实验3中随 的不断通入,溶液中
的不断通入,溶液中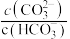
___________ (填减小、不变或增大)。
(3)常温下, 均为12的
均为12的 溶液与NaOH溶液中水电离出的
溶液与NaOH溶液中水电离出的 之比为
之比为___________ 。
Ⅱ:① 溶液②
溶液② 溶液③
溶液③ 溶液④
溶液④ 气体⑤碘水⑥氨水⑦
气体⑤碘水⑥氨水⑦ 溶液
溶液
(4)向②中通入足量④,发生反应的离子方程式为___________ 。
(5)为得到浓度较大的⑤,实验室在配制时,常加入 ,溶液中存在如下平衡:
,溶液中存在如下平衡: ,向⑤中加入一定量的①,该平衡将
,向⑤中加入一定量的①,该平衡将___________ (填“正向”或“逆向”)移动。
Ⅲ:
(6)泡沫灭火器原理(用离子方程式表示):___________
(7)配置 溶液为什么要将
溶液为什么要将 固体溶解在浓盐酸中(用离子方程式表示):
固体溶解在浓盐酸中(用离子方程式表示):___________
(8)加热蒸干 为什么得不到
为什么得不到 原理(用化学方程式表示):
原理(用化学方程式表示):___________
 溶液的性质。
溶液的性质。| 实验 | 实验操作和现象 |
| 1 | 用 试纸测定0.1mol/L 试纸测定0.1mol/L 溶液的 溶液的 ,测得 ,测得 约为12 约为12 |
| 2 | 向0.1mol/L 溶液中加入过量0.2mol/L 溶液中加入过量0.2mol/L 溶液,产生白色沉淀 溶液,产生白色沉淀 |
| 3 | 向0.1mol/L 溶液中通入过量 溶液中通入过量 ,测得溶液 ,测得溶液 约为8 约为8 |
| 4 | 向0.1mol/L 溶液中滴加几滴0.05mol/L 溶液中滴加几滴0.05mol/L ,观察不到实验现象 ,观察不到实验现象 |
(1)向0.1mol/L
 溶液滴入酚酞溶液,观察到的现象是
溶液滴入酚酞溶液,观察到的现象是(2)实验3中随
 的不断通入,溶液中
的不断通入,溶液中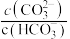
(3)常温下,
 均为12的
均为12的 溶液与NaOH溶液中水电离出的
溶液与NaOH溶液中水电离出的 之比为
之比为Ⅱ:①
 溶液②
溶液② 溶液③
溶液③ 溶液④
溶液④ 气体⑤碘水⑥氨水⑦
气体⑤碘水⑥氨水⑦ 溶液
溶液(4)向②中通入足量④,发生反应的离子方程式为
(5)为得到浓度较大的⑤,实验室在配制时,常加入
 ,溶液中存在如下平衡:
,溶液中存在如下平衡: ,向⑤中加入一定量的①,该平衡将
,向⑤中加入一定量的①,该平衡将Ⅲ:
(6)泡沫灭火器原理(用离子方程式表示):
(7)配置
 溶液为什么要将
溶液为什么要将 固体溶解在浓盐酸中(用离子方程式表示):
固体溶解在浓盐酸中(用离子方程式表示):(8)加热蒸干
 为什么得不到
为什么得不到 原理(用化学方程式表示):
原理(用化学方程式表示):
您最近一年使用:0次
名校
解题方法
5 . I、II、III三个容积均为2L的恒容密闭容器中均投入1mol CO2 和3mol H2 ,在不同温度下发生反应:CO2(g) + 3H2⇌CH3OH(g) + H2O(g) 。反应10min,测得各容器内CO2的物质的量分别如图所示。下列说法正确的是
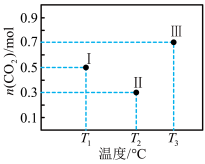

| A.升高温度、增大压强均有利于提高 H2的平衡转化率 |
| B.10min后,向容器Ⅲ中再加入1mol CO2 (g)和1mol H2O (g),此时反应逆向进行 |
| C.容器Ⅱ中的平均速率:v(CO2) =0.07 mol·L-1·min-1 |
| D.10min时,容器Ⅰ中 v(正) = v(逆) |
您最近一年使用:0次
名校
解题方法
6 . 某废矿渣的主要成分有 、
、 、
、 、
、 ,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
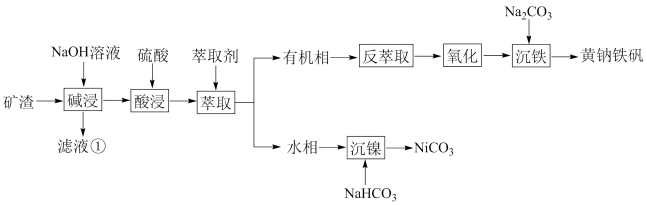
已知:i.黄钠铁矾 有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
ii.常温下,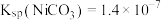 ;
;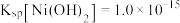 。
。
回答下列问题:
(1)滤液①中,主要存在的钠盐有_____________________ 。
(2)“萃取”可将金属离子进行富集与分离,原理如下:
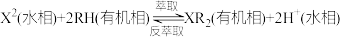 。
。
则“反萃取”应控制在____________________ (填“碱性”、“酸性”或“中性”)环境进行。
(3)“氧化”中加入 ,反应的氧化剂和还原剂的物质的量比为
,反应的氧化剂和还原剂的物质的量比为____________________ 。
(4)“沉镍”过程同时产生一种气体,该反应的离子方程式为_________________________ ,“沉镍”时若溶液 过大会导致
过大会导致 的产率下降,原因是
的产率下降,原因是__________________________ 。
(5)“沉铁”过程反应的离子方程式为_________________________ 。
(6)定量分析:
测定“酸漫”后的溶液中 的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液
的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液 ,然后用
,然后用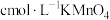 溶液滴定至终点,平行测定三次,平均消耗
溶液滴定至终点,平行测定三次,平均消耗 溶液
溶液 。则溶液中
。则溶液中 的物质的量浓度为
的物质的量浓度为___________  。
。
 、
、 、
、 、
、 ,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
,为节约和充分利用资源,通过如下工艺流程回收铁、镍。
已知:i.黄钠铁矾
 有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;
有稳定、颗粒大、易沉降、易过滤、几乎不溶于水等特点;ii.常温下,
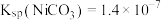 ;
;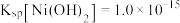 。
。回答下列问题:
(1)滤液①中,主要存在的钠盐有
(2)“萃取”可将金属离子进行富集与分离,原理如下:
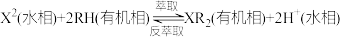 。
。则“反萃取”应控制在
(3)“氧化”中加入
 ,反应的氧化剂和还原剂的物质的量比为
,反应的氧化剂和还原剂的物质的量比为(4)“沉镍”过程同时产生一种气体,该反应的离子方程式为
 过大会导致
过大会导致 的产率下降,原因是
的产率下降,原因是(5)“沉铁”过程反应的离子方程式为
(6)定量分析:
测定“酸漫”后的溶液中
 的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液
的浓度,可确定萃取剂添加的量。取“酸浸”后的溶液 ,然后用
,然后用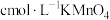 溶液滴定至终点,平行测定三次,平均消耗
溶液滴定至终点,平行测定三次,平均消耗 溶液
溶液 。则溶液中
。则溶液中 的物质的量浓度为
的物质的量浓度为 。
。
您最近一年使用:0次
名校
7 . 某兴趣小组以重铬酸钾( )溶液为研究对象,通过改变条件使其发生“色彩变幻”。
)溶液为研究对象,通过改变条件使其发生“色彩变幻”。
已知:在水溶液中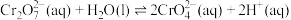
查阅资料:①含铬元素的离子在溶液中的颜色: (橙色)、
(橙色)、 (黄色)、
(黄色)、 (绿色);
(绿色);
② 易溶于水,
易溶于水, 为难溶于水的黄色沉淀。
为难溶于水的黄色沉淀。
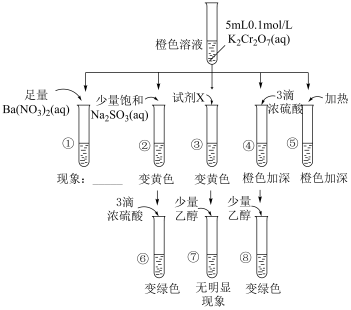
回答下列问题:
(1)设计实验①、③来验证减小生成物浓度对平衡的影响,则实验①的现象为___________ ,试剂X是___________ (填化学式)。
(2)根据实验②、⑥的现象,分析实验②溶液变黄的原因是___________ ,实验⑥中发生反应的离子方程式为___________ 。
(3)结合③、④、⑦、⑧可得出结论为___________ 。
(4)设计实验④的目的是验证增大生成物浓度平衡逆向移动,能否达到预期?___________ (填“能”或“否”)。
(5)设计实验⑤的目的是研究温度对平衡的影响,由现象可知:
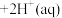 正反应的焓变
正反应的焓变
_______ 0(填“>”、“<”或“=”)。
 )溶液为研究对象,通过改变条件使其发生“色彩变幻”。
)溶液为研究对象,通过改变条件使其发生“色彩变幻”。已知:在水溶液中
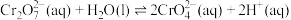
查阅资料:①含铬元素的离子在溶液中的颜色:
 (橙色)、
(橙色)、 (黄色)、
(黄色)、 (绿色);
(绿色);②
 易溶于水,
易溶于水, 为难溶于水的黄色沉淀。
为难溶于水的黄色沉淀。
回答下列问题:
(1)设计实验①、③来验证减小生成物浓度对平衡的影响,则实验①的现象为
(2)根据实验②、⑥的现象,分析实验②溶液变黄的原因是
(3)结合③、④、⑦、⑧可得出结论为
(4)设计实验④的目的是验证增大生成物浓度平衡逆向移动,能否达到预期?
(5)设计实验⑤的目的是研究温度对平衡的影响,由现象可知:

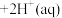 正反应的焓变
正反应的焓变
您最近一年使用:0次
2024-01-09更新
|
55次组卷
|
2卷引用:安徽省安庆市田家炳中学(安庆市第十中学)2023-2024学年高二上学期期中考试化学试题
解题方法
8 . “碳达峰、碳中和”是我国社会发展重大战略之一, 的综合利用是实现“碳达峰、碳中和”的有效途径,以下为常见的两种利用
的综合利用是实现“碳达峰、碳中和”的有效途径,以下为常见的两种利用 的方法。
的方法。
方法I: 加氢制备合成气
加氢制备合成气
在一定温度、压强为 条件下,
条件下, 和
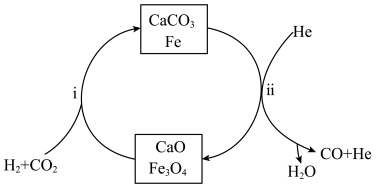
和 按照1:1投料,反应经图所示过程,可实现二氧化碳的高效转化。
按照1:1投料,反应经图所示过程,可实现二氧化碳的高效转化。
相关化学键的键能数据如下表:
(1)该反应的热化学方程式为
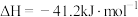 ,则
,则
______ 。
(2)有关该反应的说法错误的是_______(填标号)。
(3)反应i达到平衡后通入 ,有利于反应ii的进行,结合平衡移动原理,解释原因
,有利于反应ii的进行,结合平衡移动原理,解释原因_____________________________________________ 。
方法II: 重整制备合成气
重整制备合成气
 重整制备合成气时发生的反应主要有:
重整制备合成气时发生的反应主要有:
主反应:

副反应: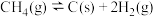
(4)在一定条件下,向 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,只发生主反应,测得平衡时压强变为原来的1.5倍,则该反应的平衡常数
,只发生主反应,测得平衡时压强变为原来的1.5倍,则该反应的平衡常数
__________ 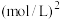 。
。
(5)主反应的反应速率 ,
, ,
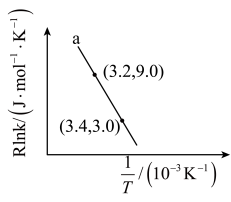
, 符合阿伦尼乌斯公式
符合阿伦尼乌斯公式 (Ea为活化能、T为温度,R、C为常数),实验测得
(Ea为活化能、T为温度,R、C为常数),实验测得 的实验数据如图所示,则该反应正反应的活化能为
的实验数据如图所示,则该反应正反应的活化能为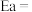
________  ,升高温度时,
,升高温度时,
_____ (填“增大”、“减小”或“不变”)。
(6)一定条件下重整反应中会因发生副反应产生积碳而导致催化剂活性降低,若向容器中通入过量水蒸气可以清除积碳,反应的化学方程式为__________ , 的值
的值__________ (填“增大”、“减小”或“不变”)。
 的综合利用是实现“碳达峰、碳中和”的有效途径,以下为常见的两种利用
的综合利用是实现“碳达峰、碳中和”的有效途径,以下为常见的两种利用 的方法。
的方法。方法I:
 加氢制备合成气
加氢制备合成气在一定温度、压强为
 条件下,
条件下, 和
和 按照1:1投料,反应经图所示过程,可实现二氧化碳的高效转化。
按照1:1投料,反应经图所示过程,可实现二氧化碳的高效转化。相关化学键的键能数据如下表:

化学键 |
|
|
|
|
键能E/( | 745 | a | 1046 | 436 |
(1)该反应的热化学方程式为

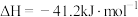 ,则
,则
(2)有关该反应的说法错误的是_______(填标号)。
| A.当装置内的气体压强不变时,反应达到平衡状态 |
B.若在反应中能及时分离出 ,可以提高 ,可以提高 的转化率 的转化率 |
C.反应ii的总反应为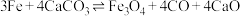 |
D.选择合适的催化剂会提高平衡时 的产率 的产率 |
(3)反应i达到平衡后通入
 ,有利于反应ii的进行,结合平衡移动原理,解释原因
,有利于反应ii的进行,结合平衡移动原理,解释原因方法II:
 重整制备合成气
重整制备合成气 重整制备合成气时发生的反应主要有:
重整制备合成气时发生的反应主要有:主反应:


副反应:
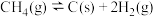
(4)在一定条件下,向
 的恒容密闭容器中通入
的恒容密闭容器中通入 和
和 ,只发生主反应,测得平衡时压强变为原来的1.5倍,则该反应的平衡常数
,只发生主反应,测得平衡时压强变为原来的1.5倍,则该反应的平衡常数
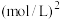 。
。(5)主反应的反应速率
 ,
, ,
, 符合阿伦尼乌斯公式
符合阿伦尼乌斯公式 (Ea为活化能、T为温度,R、C为常数),实验测得
(Ea为活化能、T为温度,R、C为常数),实验测得 的实验数据如图所示,则该反应正反应的活化能为
的实验数据如图所示,则该反应正反应的活化能为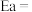
 ,升高温度时,
,升高温度时,

(6)一定条件下重整反应中会因发生副反应产生积碳而导致催化剂活性降低,若向容器中通入过量水蒸气可以清除积碳,反应的化学方程式为
 的值
的值
您最近一年使用:0次
名校
9 . 根据实验目的,下列实验及现象、结论正确的是
| 选项 | 实验目的 | 实验及现象 | 结论 |
| A | 探究温度对平衡移动的影响 | 向试管中加入2mL CuCl2溶液,CuCl2溶液存在 CuCl2溶液,CuCl2溶液存在   ,加热试管,溶液由蓝绿色变为黄绿色 ,加热试管,溶液由蓝绿色变为黄绿色 | 其他条件不变时,升高温度,平衡向吸热反应方向移动 |
| B | 探究氢离子浓度对 、 、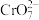 相互转化的影响 相互转化的影响 | 向2mL K2Cr2O7溶液中滴加5~10滴 K2Cr2O7溶液中滴加5~10滴 NaOH溶液,溶液变为黄色 NaOH溶液,溶液变为黄色 | 其他条件不变时,减小氢离子浓度,平衡向生成 的方向移动 的方向移动 |
| C | 探究压强对平衡移动的影响 | 用注射器吸入20mLNO2和N2O4混合气体,向内推动注射器,混合气体颜色加深 | 其他条件不变时,加压,平衡向生成NO2的方向移动 |
| D | 验证CH3COOH和H2CO3的酸性 | 向盛有2mL1mol/L的Na2CO3溶液中,逐滴加入同体积同浓度的CH3COOH溶液,无气泡产生 | 酸性强弱: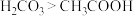 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 在实验室中进行下列实验,下列操作能实现实验目的的是
| 选项 | 实验目的 | 操作 |
| A | 检验甲酸中是否含有羧基 | 取其水溶液于试管中,向其中加入少量金属钠,观察溶液中有无气泡产生 |
| B | 检验某溶液中是否含有 | 取少量待测液于试管中,向其中滴加浓氨水,生成白色沉淀,继续滴加浓氨水,观察沉淀是否溶解 |
| C | 检验牺牲阳极法对钢铁防腐的效果 | 将镀层有破损的镀锌铁片放入酸化的3%NaCl溶液中,一段时间后,取少量溶液向其中加入 溶液,观察有无蓝色沉淀生成 溶液,观察有无蓝色沉淀生成 |
| D | 探究氢离子浓度对 、 、 互相转化影响 互相转化影响 | 向 溶液中缓慢滴加浓盐酸,观察溶液颜色的变化 溶液中缓慢滴加浓盐酸,观察溶液颜色的变化 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-01-02更新
|
385次组卷
|
2卷引用:山西省三重教育2023-2024学年高三上学期联考理科综合试题







