名校
解题方法
1 .  常用作有机合成催化剂,现有如下两种方法制备
常用作有机合成催化剂,现有如下两种方法制备 。已知:
。已知: 晶体呈白色,微溶于水,不溶于稀盐酸,露置于潮湿空气中易转化为绿色的
晶体呈白色,微溶于水,不溶于稀盐酸,露置于潮湿空气中易转化为绿色的 ,且易见光分解。
,且易见光分解。
方法一:利用热分解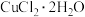 (绿色)制备
(绿色)制备 ,并进行相关探究。
,并进行相关探究。
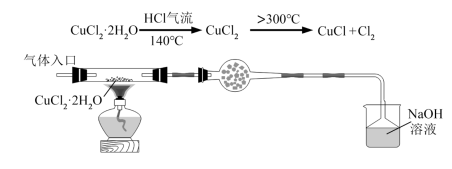
(1)将下列实验操作按先后顺序排列为:a→→→→→→d______
a.检查装置的气密性后加入药品 b.点燃酒精灯加热至 ,反应一段时间
,反应一段时间
c.调整酒精灯温度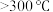 ,反应一段时间 d.停止通入
,反应一段时间 d.停止通入
e.停止通入 ,然后通入干燥
,然后通入干燥 f.在“气体入口”处通入干燥
f.在“气体入口”处通入干燥
g.熄灭酒精灯
(2)当观察到___________ 时,反应达到终点,停止加热。
方法二:以 (含少量
(含少量 )粗品为原料制取
)粗品为原料制取 ,设计的合成路线如下:
,设计的合成路线如下:
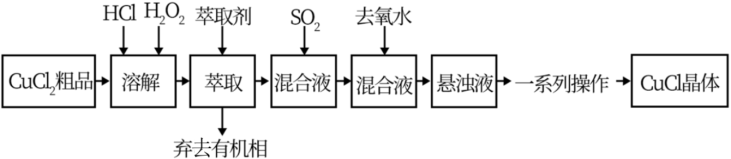
查阅资料可知:①在较高的盐酸浓度下, 能溶解于甲基异丁基甲酮:
能溶解于甲基异丁基甲酮:
② 在溶液中存在:
在溶液中存在: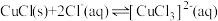 。
。
(3)写出 通入混合液中发生的反应的离子方程式
通入混合液中发生的反应的离子方程式___________ 。
(4)下列叙述正确的是___________(填字母)。

(5)向混合液中加入去氧水的目的是___________ 。
(6)现称取 产品,用硫酸酸化的硫酸铁完全溶解,并稀释成
产品,用硫酸酸化的硫酸铁完全溶解,并稀释成 。每次用移液管移取
。每次用移液管移取 溶液于锥形瓶中,再用
溶液于锥形瓶中,再用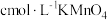 溶液滴定,平均消耗
溶液滴定,平均消耗 。
。
①按该实验方案计算产品的纯度为___________ %。
②有同学认为该实验方案明显不合理,会导致计算的 纯度
纯度___________ (填“偏高”或“偏低”)
 常用作有机合成催化剂,现有如下两种方法制备
常用作有机合成催化剂,现有如下两种方法制备 。已知:
。已知: 晶体呈白色,微溶于水,不溶于稀盐酸,露置于潮湿空气中易转化为绿色的
晶体呈白色,微溶于水,不溶于稀盐酸,露置于潮湿空气中易转化为绿色的 ,且易见光分解。
,且易见光分解。方法一:利用热分解
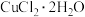 (绿色)制备
(绿色)制备 ,并进行相关探究。
,并进行相关探究。
(1)将下列实验操作按先后顺序排列为:a→→→→→→d
a.检查装置的气密性后加入药品 b.点燃酒精灯加热至
 ,反应一段时间
,反应一段时间c.调整酒精灯温度
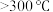 ,反应一段时间 d.停止通入
,反应一段时间 d.停止通入
e.停止通入
 ,然后通入干燥
,然后通入干燥 f.在“气体入口”处通入干燥
f.在“气体入口”处通入干燥
g.熄灭酒精灯
(2)当观察到
方法二:以
 (含少量
(含少量 )粗品为原料制取
)粗品为原料制取 ,设计的合成路线如下:
,设计的合成路线如下:
查阅资料可知:①在较高的盐酸浓度下,
 能溶解于甲基异丁基甲酮:
能溶解于甲基异丁基甲酮:②
 在溶液中存在:
在溶液中存在: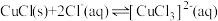 。
。(3)写出
 通入混合液中发生的反应的离子方程式
通入混合液中发生的反应的离子方程式(4)下列叙述正确的是___________(填字母)。

A. 原料中含有的 原料中含有的 经氧化、萃取几乎都在有机相中被除去 经氧化、萃取几乎都在有机相中被除去 |
| B.加入萃取剂后,混合物转移至分液漏斗中,塞上玻璃塞,如图用力振摇 |
| C.上述合成路线中,一系列操作包括:抽滤、洗涤、干燥,且干燥时应注意密封、避光 |
D.该流程中温度越高越有利于将 转化为 转化为 |
(6)现称取
 产品,用硫酸酸化的硫酸铁完全溶解,并稀释成
产品,用硫酸酸化的硫酸铁完全溶解,并稀释成 。每次用移液管移取
。每次用移液管移取 溶液于锥形瓶中,再用
溶液于锥形瓶中,再用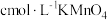 溶液滴定,平均消耗
溶液滴定,平均消耗 。
。①按该实验方案计算产品的纯度为
②有同学认为该实验方案明显不合理,会导致计算的
 纯度
纯度
您最近半年使用:0次
名校
解题方法
2 . 由 键构建
键构建 键是有机化学的热点研究领域。我国科学家利用
键是有机化学的热点研究领域。我国科学家利用 苯基甘氨酸中的
苯基甘氨酸中的 键在
键在 作用下构建
作用下构建 键,实现了喹啉并内酯的高选择性制备。合成路线如图。
键,实现了喹啉并内酯的高选择性制备。合成路线如图。
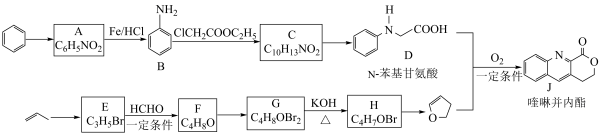
已知:i.
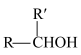
ii.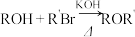
(1) 的反应类型是
的反应类型是___________ 。
(2)B具有碱性, 转化为
转化为 的反应中,使
的反应中,使 过量可以提高
过量可以提高 的平衡转化率,
的平衡转化率, 的作用是
的作用是___________ (写出一条即可)。
(3)C转化为 的化学方程式为
的化学方程式为___________ 。
(4) 转化为
转化为 的化学方程式为
的化学方程式为___________ ; 生成
生成 的过程中会得到少量的聚合物,写出其中一种的结构简式:
的过程中会得到少量的聚合物,写出其中一种的结构简式:___________ 。
(5)已知:
i.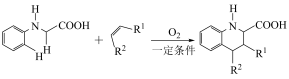
ii.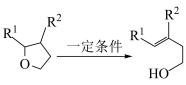
①D和 在
在 作用下得到
作用下得到 的4步反应如图(无机试剂及条件已略去),中间产物1中有两个六元环和一个五元环,中间产物3中有三个六元环。结合已知反应信息,写出结构简式:中间产物1
的4步反应如图(无机试剂及条件已略去),中间产物1中有两个六元环和一个五元环,中间产物3中有三个六元环。结合已知反应信息,写出结构简式:中间产物1___________ ,中间产物3___________ 。
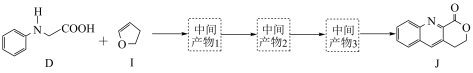
②D和 转化成
转化成 的过程中还生成水,理论上该过程中消耗的
的过程中还生成水,理论上该过程中消耗的 与生成的
与生成的 的物质的量之比为
的物质的量之比为___________ 。
 键构建
键构建 键是有机化学的热点研究领域。我国科学家利用
键是有机化学的热点研究领域。我国科学家利用 苯基甘氨酸中的
苯基甘氨酸中的 键在
键在 作用下构建
作用下构建 键,实现了喹啉并内酯的高选择性制备。合成路线如图。
键,实现了喹啉并内酯的高选择性制备。合成路线如图。
已知:i.

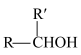
ii.
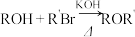
(1)
 的反应类型是
的反应类型是(2)B具有碱性,
 转化为
转化为 的反应中,使
的反应中,使 过量可以提高
过量可以提高 的平衡转化率,
的平衡转化率, 的作用是
的作用是(3)C转化为
 的化学方程式为
的化学方程式为(4)
 转化为
转化为 的化学方程式为
的化学方程式为 生成
生成 的过程中会得到少量的聚合物,写出其中一种的结构简式:
的过程中会得到少量的聚合物,写出其中一种的结构简式:(5)已知:
i.

ii.

①D和
 在
在 作用下得到
作用下得到 的4步反应如图(无机试剂及条件已略去),中间产物1中有两个六元环和一个五元环,中间产物3中有三个六元环。结合已知反应信息,写出结构简式:中间产物1
的4步反应如图(无机试剂及条件已略去),中间产物1中有两个六元环和一个五元环,中间产物3中有三个六元环。结合已知反应信息,写出结构简式:中间产物1
②D和
 转化成
转化成 的过程中还生成水,理论上该过程中消耗的
的过程中还生成水,理论上该过程中消耗的 与生成的
与生成的 的物质的量之比为
的物质的量之比为
您最近半年使用:0次
解题方法
3 . 雾霾含有大量的污染物SO2、NO。工业上变废为宝利用工业尾气获得NH4NO3产品的流程图如下:(Ce为铈元素)

(1)上述流程中循环使用的物质有_____________________ 。
(2)上述合成路线中用到15%~20%的乙醇胺(HOCH2CH2NH2),其水溶液具有弱碱性,显碱性的原因:HOCH2CH2NH2 + H2O
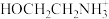 +OH-,写出乙醇胺吸收CO2的化学方程式
+OH-,写出乙醇胺吸收CO2的化学方程式___________ 。
(3)写出吸收池Ⅲ中酸性条件下NO转化为 (或NO转化为
(或NO转化为 )的离子方程式:
)的离子方程式:_____ (任选其一)。
(4)向吸收池Ⅳ得到的 溶液中滴加少量CaCl2溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因:
溶液中滴加少量CaCl2溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因:________________________________________ 。
(5)从氧化池Ⅵ中得到粗产品NH4NO3的实验操作是______________ 、____________ 、过滤、洗涤等。上述流程中每一步均恰好完全反应,若制得NH4NO3质量为0.8kg,电解池V制得2mol/L的 溶液2L,则氧化池Ⅵ中消耗的O2在标准状况下的体积为
溶液2L,则氧化池Ⅵ中消耗的O2在标准状况下的体积为________ L。

(1)上述流程中循环使用的物质有
(2)上述合成路线中用到15%~20%的乙醇胺(HOCH2CH2NH2),其水溶液具有弱碱性,显碱性的原因:HOCH2CH2NH2 + H2O

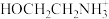 +OH-,写出乙醇胺吸收CO2的化学方程式
+OH-,写出乙醇胺吸收CO2的化学方程式(3)写出吸收池Ⅲ中酸性条件下NO转化为
 (或NO转化为
(或NO转化为 )的离子方程式:
)的离子方程式:(4)向吸收池Ⅳ得到的
 溶液中滴加少量CaCl2溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因:
溶液中滴加少量CaCl2溶液,出现浑浊,pH降低,用平衡移动原理解释溶液pH降低的原因:(5)从氧化池Ⅵ中得到粗产品NH4NO3的实验操作是
 溶液2L,则氧化池Ⅵ中消耗的O2在标准状况下的体积为
溶液2L,则氧化池Ⅵ中消耗的O2在标准状况下的体积为
您最近半年使用:0次
名校
4 . 以含镓废料[主要成分为 ]为原料制备半导体材料
]为原料制备半导体材料 的工艺如图所示。已知:
的工艺如图所示。已知: 和
和 的性质相似。下列叙述错误的是
的性质相似。下列叙述错误的是
 ]为原料制备半导体材料
]为原料制备半导体材料 的工艺如图所示。已知:
的工艺如图所示。已知: 和
和 的性质相似。下列叙述错误的是
的性质相似。下列叙述错误的是 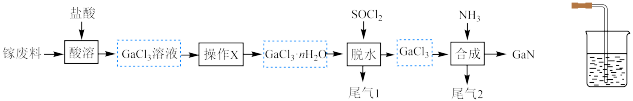
A.操作 不宜温度过高 不宜温度过高 |
B.用 固体可替代“脱水”中的 固体可替代“脱水”中的 |
C.用酸性 溶液可检验“脱水”产生的气体含 溶液可检验“脱水”产生的气体含 |
| D.不能用如图装置吸收“合成”中尾气 |
您最近半年使用:0次
2024-04-01更新
|
177次组卷
|
2卷引用:吉林省白山市2023-2024学年高三第二次模拟考试化学试题
23-24高三下·福建·阶段练习
5 . 二氧化铈 是一种用途广泛的稀土化合物。以氟碳铈矿(主要含
是一种用途广泛的稀土化合物。以氟碳铈矿(主要含 )为原料制备
)为原料制备 的一种工艺流程如图所示:
的一种工艺流程如图所示: 能与
能与 结合成
结合成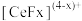 ,也能与
,也能与 结合成
结合成 ;
;
②在硫酸体系中 能被萃取剂
能被萃取剂 萃取,而
萃取,而 不能。
不能。
回答下列问题:
(1)氧化焙烧中氧化的目的是_______ 。
(2)“萃取”时存在反应: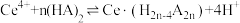 ,如图中D是分配比,表示
,如图中D是分配比,表示 分别在有机层中与水层中存在形式的物质的量浓度之比
分别在有机层中与水层中存在形式的物质的量浓度之比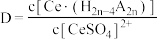 保持其它条件不变,若在起始料液中加入不同量的
保持其它条件不变,若在起始料液中加入不同量的 以改变水层中的
以改变水层中的 ,请解释D随起始料液中
,请解释D随起始料液中 变化的原因:
变化的原因:_______ 。 的作用下
的作用下 转化为
转化为 ,反应的离子方程式为:
,反应的离子方程式为:_______ 。
(4)向水层中加入 溶液来调节溶液的
溶液来调节溶液的 ,
, 应大于
应大于_______ 时, 完全生成
完全生成 沉淀。(已知
沉淀。(已知 )
)
(5)“氧化”步骤中氧化剂与还原剂物质的量之比为_______ 。
(6) 是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧,在尾气消除过程中发生着
是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧,在尾气消除过程中发生着 的循环,请写出
的循环,请写出 消除
消除 尾气(气体产物是空气的某一成分)的化学方程式
尾气(气体产物是空气的某一成分)的化学方程式_______ 。
(7)氧化铈 ,常用作玻璃工业添加剂,在其立方晶胞中掺杂
,常用作玻璃工业添加剂,在其立方晶胞中掺杂 ,
, 占据原来
占据原来 的位置,可以得到更稳定的结构,如图所示,
的位置,可以得到更稳定的结构,如图所示, 晶胞中
晶胞中 与最近
与最近 的核间距为
的核间距为 。(已知:
。(已知: 的空缺率
的空缺率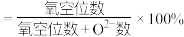 )
) 点原子的分数坐标为
点原子的分数坐标为 ,则
,则 点原子的分数坐标为
点原子的分数坐标为_______ 。
② 晶胞中与
晶胞中与 最近的
最近的 的个数为
的个数为_______ 。
③ 晶体的密度为
晶体的密度为_______ (只需列出表达式)。
④若掺杂 后得到
后得到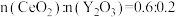 的晶体,则此晶体中
的晶体,则此晶体中 的空缺率为
的空缺率为_______ 。
 是一种用途广泛的稀土化合物。以氟碳铈矿(主要含
是一种用途广泛的稀土化合物。以氟碳铈矿(主要含 )为原料制备
)为原料制备 的一种工艺流程如图所示:
的一种工艺流程如图所示: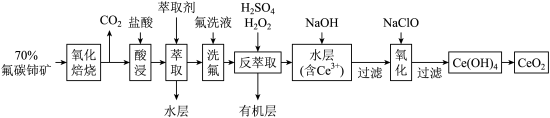
 能与
能与 结合成
结合成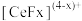 ,也能与
,也能与 结合成
结合成 ;
;②在硫酸体系中
 能被萃取剂
能被萃取剂 萃取,而
萃取,而 不能。
不能。回答下列问题:
(1)氧化焙烧中氧化的目的是
(2)“萃取”时存在反应:
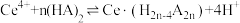 ,如图中D是分配比,表示
,如图中D是分配比,表示 分别在有机层中与水层中存在形式的物质的量浓度之比
分别在有机层中与水层中存在形式的物质的量浓度之比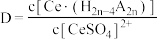 保持其它条件不变,若在起始料液中加入不同量的
保持其它条件不变,若在起始料液中加入不同量的 以改变水层中的
以改变水层中的 ,请解释D随起始料液中
,请解释D随起始料液中 变化的原因:
变化的原因: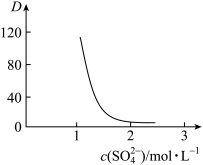
 的作用下
的作用下 转化为
转化为 ,反应的离子方程式为:
,反应的离子方程式为:(4)向水层中加入
 溶液来调节溶液的
溶液来调节溶液的 ,
, 应大于
应大于 完全生成
完全生成 沉淀。(已知
沉淀。(已知 )
)(5)“氧化”步骤中氧化剂与还原剂物质的量之比为
(6)
 是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧,在尾气消除过程中发生着
是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧,在尾气消除过程中发生着 的循环,请写出
的循环,请写出 消除
消除 尾气(气体产物是空气的某一成分)的化学方程式
尾气(气体产物是空气的某一成分)的化学方程式(7)氧化铈
 ,常用作玻璃工业添加剂,在其立方晶胞中掺杂
,常用作玻璃工业添加剂,在其立方晶胞中掺杂 ,
, 占据原来
占据原来 的位置,可以得到更稳定的结构,如图所示,
的位置,可以得到更稳定的结构,如图所示, 晶胞中
晶胞中 与最近
与最近 的核间距为
的核间距为 。(已知:
。(已知: 的空缺率
的空缺率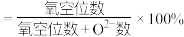 )
)
 点原子的分数坐标为
点原子的分数坐标为 ,则
,则 点原子的分数坐标为
点原子的分数坐标为②
 晶胞中与
晶胞中与 最近的
最近的 的个数为
的个数为③
 晶体的密度为
晶体的密度为④若掺杂
 后得到
后得到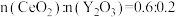 的晶体,则此晶体中
的晶体,则此晶体中 的空缺率为
的空缺率为
您最近半年使用:0次
6 . 尿素是一种适用于各种土壤和植物的有机态氮肥,是首个由无机物人工合成的有机物。以 等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。
等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。
(1)1828年,德国化学家维勒使用无机物质氰酸银(AgCNO)与 在一定条件下反应制得
在一定条件下反应制得 。
。
①该反应的化学方程式是___________ 。
② 晶体中含有的化学键有
晶体中含有的化学键有___________ (填序号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(2) 和
和 合成尿素
合成尿素 的能量变化如图所示,写出该反应的热化学方程式:
的能量变化如图所示,写出该反应的热化学方程式:___________ 。
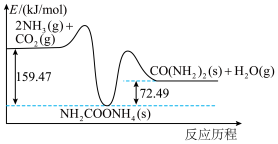
(3)在恒容密闭容器中发生反应: ,下列能说明该反应达到平衡状态的是___________(填序号)。
,下列能说明该反应达到平衡状态的是___________(填序号)。
(4)在恒容密闭容器中发生反应: ,测得
,测得 的平衡转化率与起始投料比[
的平衡转化率与起始投料比[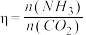 ,
, 分别为1∶1、2∶1、3∶1]和温度关系如图所示。
分别为1∶1、2∶1、3∶1]和温度关系如图所示。
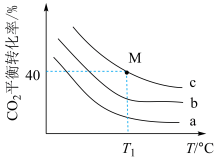
①曲线a代表的投料比为___________ ;
②若 ℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内,
℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内, 分压的平均变化率为
分压的平均变化率为___________  ,M点对应条件下的分压平衡常数为
,M点对应条件下的分压平衡常数为___________  (列出计算式即可)。
(列出计算式即可)。
 等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。
等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。(1)1828年,德国化学家维勒使用无机物质氰酸银(AgCNO)与
 在一定条件下反应制得
在一定条件下反应制得 。
。①该反应的化学方程式是
②
 晶体中含有的化学键有
晶体中含有的化学键有A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(2)
 和
和 合成尿素
合成尿素 的能量变化如图所示,写出该反应的热化学方程式:
的能量变化如图所示,写出该反应的热化学方程式:
(3)在恒容密闭容器中发生反应:
 ,下列能说明该反应达到平衡状态的是___________(填序号)。
,下列能说明该反应达到平衡状态的是___________(填序号)。A.单位时间内每消耗44g ,同时生成18g ,同时生成18g |
| B.容器中混合气体平均摩尔质量不变 |
C.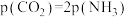 |
D. 的分压保持不变 的分压保持不变 |
(4)在恒容密闭容器中发生反应:
 ,测得
,测得 的平衡转化率与起始投料比[
的平衡转化率与起始投料比[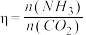 ,
, 分别为1∶1、2∶1、3∶1]和温度关系如图所示。
分别为1∶1、2∶1、3∶1]和温度关系如图所示。
①曲线a代表的投料比为
②若
 ℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内,
℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内, 分压的平均变化率为
分压的平均变化率为 ,M点对应条件下的分压平衡常数为
,M点对应条件下的分压平衡常数为 (列出计算式即可)。
(列出计算式即可)。
您最近半年使用:0次
解题方法
7 . 尿素[CO(NH2)2]是一种重要的氮肥。工业上以CO2和NH3为原料合成尿素,在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g) H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272
H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272
反应Ⅱ:H2NCOONH4(s) CO(NH2)2(s)+H2O(g) ΔH2=
CO(NH2)2(s)+H2O(g) ΔH2=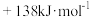
总反应Ⅲ:2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(g) ∆H3
CO(NH2)2(s)+H2O(g) ∆H3
(1)CO2的电子式为___________ ;1mol CO(NH2)2中含有___________ molπ键。
(2)反应Ⅰ的熵变ΔS___________  填“
填“ ”“
”“ ”或“
”或“ ”
” ,反应Ⅲ的
,反应Ⅲ的 H3=
H3=___________ 。
(3)下列关于尿素合成的说法正确的是___________。
反应Ⅰ:2NH3(g)+CO2(g)
 H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272
H2NCOONH4(s)(氨基甲酸铵) ΔH1=-272
反应Ⅱ:H2NCOONH4(s)
 CO(NH2)2(s)+H2O(g) ΔH2=
CO(NH2)2(s)+H2O(g) ΔH2=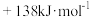
总反应Ⅲ:2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(g) ∆H3
CO(NH2)2(s)+H2O(g) ∆H3(1)CO2的电子式为
(2)反应Ⅰ的熵变ΔS
 填“
填“ ”“
”“ ”或“
”或“ ”
” ,反应Ⅲ的
,反应Ⅲ的 H3=
H3=(3)下列关于尿素合成的说法正确的是___________。
| A.及时分离出尿素可促使反应Ⅱ向正反应方向移动 |
| B.从合成塔出来的混合气体分离出水蒸气后可以循环使用 |
| C.保持容积不变,充入惰性气体增大压强,可提高总反应Ⅲ的反应速率 |
| D.保持压强不变,降低氨碳比[n(NH3)/n(CO2)]可提高反应Ⅰ中NH3的平衡转化率 |
您最近半年使用:0次
解题方法
8 . 苯甲酸甲酯是一种无色透明油状液体,具有浓郁的冬青油香气,用于配制香水、香精,也可用作有机合成中间体、溶剂等。某实验小组以苯甲酸和甲醇为原料模拟工业合成苯甲酸甲酯,步骤如下:
Ⅰ.制备:向100mL如图所示的装置A中加入磁力搅拌子,然 后依次加入6.1 g苯甲酸、10 mL 95%甲醇、20 mL苯,微热将苯甲酸全部融化后,加入2.5克固体氯化铝催化剂。按如图所示组装好仪器,并预先在分水器内加入水至略低于支管口,加热回流4 h,直至反应基本完成。
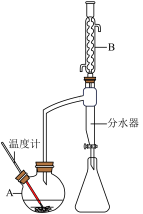
实验过程中分水器得到的液体会分层,需多次开启分水器活塞将下层液体放出。
Ⅱ.分离提纯:待反应液冷却至室温后过滤掉氯化铝,将液体倒入盛有冷水的烧杯中,再经过一系列分离提纯操作,最后蒸馏收集196~199°C馏分,得到5.0 g产品。
可能用到的数据如下:
请回答下列问题:
(1)苯甲酸的沸点高于苯甲酸甲酯的原因为___________ 。
(2)加料时,n(甲醇):n(苯甲酸)约为5:1,甲醇过量的原因是____________ ;但醇酸比超过5:1时,醇酸比的增加对产率影响不大,原因是___________ 。
(3)该实验的温度控制在85°C,应采取的加热方式为___________ 。
(4)实验中需多次将分水器中下层液体放出,其目的是___________ ,判断反应已经完成的标志是___________ 。
(5)步骤Ⅱ中,“一系列分离提纯操作”过程中用到的试剂包括a.无水氯化钙,b.饱和食盐水,c.5% Na2CO3溶液。按操作先后顺序应依次加入___________ (填字母),加入饱和食盐水的作用是___________ 。
(6)传统制法用浓硫酸催化,浓硫酸催化具有活性高,价格低廉的优点,但现代工艺多以固体氯化铝作催化剂。这样改进最主要的原因是___________ 。
Ⅰ.制备:向100mL如图所示的装置A中加入磁力搅拌子,然 后依次加入6.1 g苯甲酸、10 mL 95%甲醇、20 mL苯,微热将苯甲酸全部融化后,加入2.5克固体氯化铝催化剂。按如图所示组装好仪器,并预先在分水器内加入水至略低于支管口,加热回流4 h,直至反应基本完成。

实验过程中分水器得到的液体会分层,需多次开启分水器活塞将下层液体放出。
Ⅱ.分离提纯:待反应液冷却至室温后过滤掉氯化铝,将液体倒入盛有冷水的烧杯中,再经过一系列分离提纯操作,最后蒸馏收集196~199°C馏分,得到5.0 g产品。
可能用到的数据如下:
| 有机物名称 | 相对分子质量 | 密度/(g· cm-3) | 沸点/°C | 溶解性 |
| 苯甲酸 | 122 | 1.26 | 249 | 微溶于水,易溶于乙醇 |
| 甲醇 | 32 | 0.79 | 64.8 | 易溶于水 |
| 苯甲酸甲酯 | 136 | 1.08 | 198 | 难溶于水、易溶于乙醇 |
| 苯 | 78 | 0.88 | 80.1 | 难溶于水 |
(1)苯甲酸的沸点高于苯甲酸甲酯的原因为
(2)加料时,n(甲醇):n(苯甲酸)约为5:1,甲醇过量的原因是
(3)该实验的温度控制在85°C,应采取的加热方式为
(4)实验中需多次将分水器中下层液体放出,其目的是
(5)步骤Ⅱ中,“一系列分离提纯操作”过程中用到的试剂包括a.无水氯化钙,b.饱和食盐水,c.5% Na2CO3溶液。按操作先后顺序应依次加入
(6)传统制法用浓硫酸催化,浓硫酸催化具有活性高,价格低廉的优点,但现代工艺多以固体氯化铝作催化剂。这样改进最主要的原因是
您最近半年使用:0次
9 . 抗击“疫情”期间,过氧乙酸是常用的消毒剂之一,实验室拟合成过氧乙酸并测定其含量。
(1)浓缩H2O2
在图示装置(加热装置已省略)中,由分液漏斗向冷凝管1中滴加30%H2O2溶液,最终得到质量分数约68%的H2O2溶液。
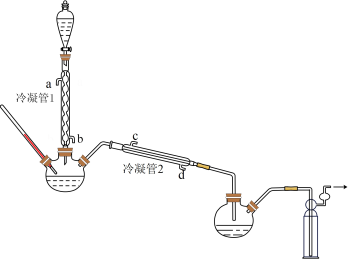
①冷凝管1、冷凝管2中进水接口依次为、___________ (填字母)。
②加热温度不宜超过60℃的原因是___________ 。
(2)合成过氧乙酸
向带有搅拌装置及温度计的500mL三口烧瓶中先加入16g冰醋酸,在搅拌下滴加90g68%H2O2溶液,最后加入4.1mL浓硫酸,搅拌5h,静置20h。(已知CH3COOH+H2O2= +H2O)
+H2O)
①用浓缩的68%H2O2溶液代替常见的30%H2O2溶液的目的是___________ 。
②充分搅拌的目的是___________ 。
(3)过氧乙酸含量的测定
步骤a:称取5.0g过氧乙酸试样(液体),配制成100mL溶液A。
步骤b:在碘量瓶中加入5.0mL 溶液、3滴
溶液、3滴 溶液、5.0mL溶液A,摇匀,用0.01mol/L的
溶液、5.0mL溶液A,摇匀,用0.01mol/L的 溶液滴定至溶液呈微红色。
溶液滴定至溶液呈微红色。
步骤c:向滴定后的溶液中再加1.0gKI(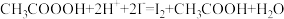 ),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的
),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的 标准溶液滴定至蓝色刚好褪去(
标准溶液滴定至蓝色刚好褪去( )。重复步骤b,步骤c三次,测得平均消耗
)。重复步骤b,步骤c三次,测得平均消耗 标准溶液的体积为20.00mL。
标准溶液的体积为20.00mL。
①步骤a中配制溶液A时,需要用到的玻璃仪器除烧杯、胶头滴管、玻璃棒和量筒外,还需要______ 。
②设计步骤b的目的是___________ 。
③过氧乙酸的质量分数为___________ %。
(1)浓缩H2O2
在图示装置(加热装置已省略)中,由分液漏斗向冷凝管1中滴加30%H2O2溶液,最终得到质量分数约68%的H2O2溶液。

①冷凝管1、冷凝管2中进水接口依次为、
②加热温度不宜超过60℃的原因是
(2)合成过氧乙酸
向带有搅拌装置及温度计的500mL三口烧瓶中先加入16g冰醋酸,在搅拌下滴加90g68%H2O2溶液,最后加入4.1mL浓硫酸,搅拌5h,静置20h。(已知CH3COOH+H2O2=
 +H2O)
+H2O)①用浓缩的68%H2O2溶液代替常见的30%H2O2溶液的目的是
②充分搅拌的目的是
(3)过氧乙酸含量的测定
步骤a:称取5.0g过氧乙酸试样(液体),配制成100mL溶液A。
步骤b:在碘量瓶中加入5.0mL
 溶液、3滴
溶液、3滴 溶液、5.0mL溶液A,摇匀,用0.01mol/L的
溶液、5.0mL溶液A,摇匀,用0.01mol/L的 溶液滴定至溶液呈微红色。
溶液滴定至溶液呈微红色。步骤c:向滴定后的溶液中再加1.0gKI(
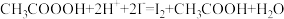 ),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的
),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂20mL,摇匀,用淀粉溶液作指示剂,用0.05mol/L的 标准溶液滴定至蓝色刚好褪去(
标准溶液滴定至蓝色刚好褪去( )。重复步骤b,步骤c三次,测得平均消耗
)。重复步骤b,步骤c三次,测得平均消耗 标准溶液的体积为20.00mL。
标准溶液的体积为20.00mL。①步骤a中配制溶液A时,需要用到的玻璃仪器除烧杯、胶头滴管、玻璃棒和量筒外,还需要
②设计步骤b的目的是
③过氧乙酸的质量分数为
您最近半年使用:0次
10 . 过氧乙酸是具有重要用途的有机合成氧化剂和化工原料,实验室拟合成过氧乙酸并测定其含量。
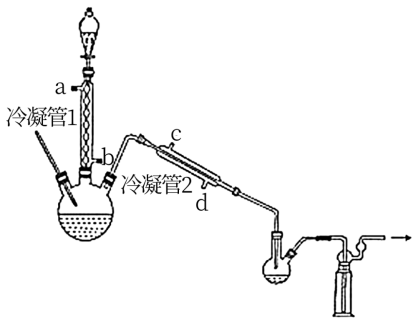
(1)浓缩H2O2
在图示装置(加热装置已省略)中,由分液漏斗向冷凝管1中滴加30% H2O2溶液,最终得到质量分数约68%的H2O2溶液。
①冷凝管1、冷凝管2中进水接口依次为___ 、___ 。(填字母)
②加热温度不宜超过60℃的原因是___ 。
(2)合成过氧乙酸
向带有搅拌装置及温度计的500mL三口烧瓶中先加入16g冰醋酸,在搅拌下滴加90g68%H2O2溶液,最后加入4.1mL浓硫酸,搅拌5h,静置20h。
(已知:CH3COOH+H2O2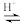
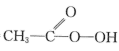 +H2O)
+H2O)
①用浓缩的68%H2O2溶液代替常见的30%H2O2溶液的目的是___ ;浓硫酸的作用是___ 。
②充分搅拌的目的是___ 。
(3)过氧乙酸含量的测定
步骤a:称取5.0g过氧乙酸试样(液体),配制成100mL溶液A。
步骤b:在碘量瓶中加入5.0mLH2SO4溶液、3滴MnSO4溶液、5.0mL溶液A,摇匀,用0.01mol•L-1的KMnO4溶液滴定至溶液呈微红色。
步骤c:向滴定后的溶液中再加1.0gKI(CH3COOOH+2H++2I-=I2+CH3COOH+H2O),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂2.0mL,摇匀,用淀粉溶液作指示剂,用0.05mol•L-1的Na2S2O3标准溶液滴定至蓝色刚好褪去(I2+2S2O =2I-+S4O
=2I-+S4O )。重复步骤b、步骤c三次,测得平均消耗Na2S2O3标准溶液的体积为20.00mL。
)。重复步骤b、步骤c三次,测得平均消耗Na2S2O3标准溶液的体积为20.00mL。
①步骤a中配制溶液A时,需要用到的玻璃仪器除烧杯、100mL容量瓶、玻璃棒和量筒外,还需要____ 。
②设计步骤b的目的是___ 。
③过氧乙酸的质量分数为___ %。

(1)浓缩H2O2
在图示装置(加热装置已省略)中,由分液漏斗向冷凝管1中滴加30% H2O2溶液,最终得到质量分数约68%的H2O2溶液。
①冷凝管1、冷凝管2中进水接口依次为
②加热温度不宜超过60℃的原因是
(2)合成过氧乙酸
向带有搅拌装置及温度计的500mL三口烧瓶中先加入16g冰醋酸,在搅拌下滴加90g68%H2O2溶液,最后加入4.1mL浓硫酸,搅拌5h,静置20h。
(已知:CH3COOH+H2O2
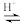
 +H2O)
+H2O)①用浓缩的68%H2O2溶液代替常见的30%H2O2溶液的目的是
②充分搅拌的目的是
(3)过氧乙酸含量的测定
步骤a:称取5.0g过氧乙酸试样(液体),配制成100mL溶液A。
步骤b:在碘量瓶中加入5.0mLH2SO4溶液、3滴MnSO4溶液、5.0mL溶液A,摇匀,用0.01mol•L-1的KMnO4溶液滴定至溶液呈微红色。
步骤c:向滴定后的溶液中再加1.0gKI(CH3COOOH+2H++2I-=I2+CH3COOH+H2O),摇匀,置于暗处5min,用蒸馏水冲洗瓶盖及四周,加钼酸铵催化剂2.0mL,摇匀,用淀粉溶液作指示剂,用0.05mol•L-1的Na2S2O3标准溶液滴定至蓝色刚好褪去(I2+2S2O
 =2I-+S4O
=2I-+S4O )。重复步骤b、步骤c三次,测得平均消耗Na2S2O3标准溶液的体积为20.00mL。
)。重复步骤b、步骤c三次,测得平均消耗Na2S2O3标准溶液的体积为20.00mL。①步骤a中配制溶液A时,需要用到的玻璃仪器除烧杯、100mL容量瓶、玻璃棒和量筒外,还需要
②设计步骤b的目的是
③过氧乙酸的质量分数为
您最近半年使用:0次



