1 . 下列说法正确的是
A.在恒容恒温条件下,当 达到平衡后,再充入一定量的 达到平衡后,再充入一定量的 后达平衡, 后达平衡, 转化率将增大 转化率将增大 |
B.对于反应 达平衡后,缩小容器体积, 达平衡后,缩小容器体积, 的浓度增大 的浓度增大 |
| C.可逆反应达到平衡后,增大任何一种反应物的量,都可使平衡正向移动 |
D.在恒温条件下,当 反应平衡后,缩小体积,活化分子百分数增加 反应平衡后,缩小体积,活化分子百分数增加 |
您最近一年使用:0次
2 .  和
和 合成乙醇反应为
合成乙醇反应为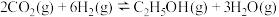 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图甲;已知
充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图甲;已知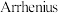 经验公式为
经验公式为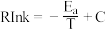 (
( 为活化能,k为速率常数,R和C为常数),为探究
为活化能,k为速率常数,R和C为常数),为探究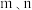 两种催化剂的催化效能,进行了实验探究,依据实验数据获得图乙曲线,下列有关说法正确的是
两种催化剂的催化效能,进行了实验探究,依据实验数据获得图乙曲线,下列有关说法正确的是
 和
和 合成乙醇反应为
合成乙醇反应为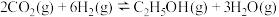 。将等物质的量的
。将等物质的量的 和
和 充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图甲;已知
充入一刚性容器中,测得平衡时乙醇的体积分数随温度和压强的关系如图甲;已知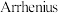 经验公式为
经验公式为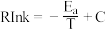 (
( 为活化能,k为速率常数,R和C为常数),为探究
为活化能,k为速率常数,R和C为常数),为探究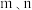 两种催化剂的催化效能,进行了实验探究,依据实验数据获得图乙曲线,下列有关说法正确的是
两种催化剂的催化效能,进行了实验探究,依据实验数据获得图乙曲线,下列有关说法正确的是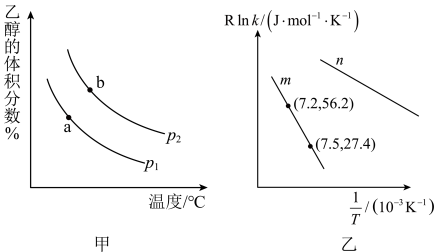
A.图甲压强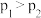 |
B.图甲 两点的平衡常数 两点的平衡常数 |
C.在m催化剂作用下,该反应的活化能 |
| D.由图乙中信息获知催化效能较高的催化剂是n |
您最近一年使用:0次
3 . 下列有关合成氨工业的说法,正确的是
A.根据勒夏特列原理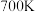 左右比室温更有利于合成氨的反应 左右比室温更有利于合成氨的反应 |
B.由于氨易液化, 在实际生产中可循环使用,所以总体来说合成氨的产率很高 在实际生产中可循环使用,所以总体来说合成氨的产率很高 |
| C.升高温度可以加快反应速率,且有利于化学平衡向合成氨的方向移动 |
D.合成氨采用的压强是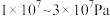 ,因为该压强下铁触媒的活性最高 ,因为该压强下铁触媒的活性最高 |
您最近一年使用:0次
4 . 下列反应达到平衡后,升高温度和增大压强,平衡移动方向一致的是
A.C(s) + CO2(g) 2CO(g)△H>0 2CO(g)△H>0 |
B.Cl2(g) +H2O(l) HCl(aq)+HClO(aq)△H>0 HCl(aq)+HClO(aq)△H>0 |
C.H2(g) +I2(g) 2HI(g)△H<0 2HI(g)△H<0 |
D.O2(g) +2SO2(g) 2SO3(g)△H<0 2SO3(g)△H<0 |
您最近一年使用:0次
名校
5 . 某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如图所示图像(图中p表示压强,T表示温度,n表示物质的量),下列结论正确的是
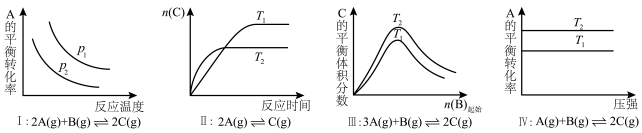

A.反应I: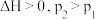 |
B.反应II: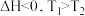 |
C.反应III: 或 或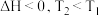 |
D.反应IV: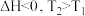 |
您最近一年使用:0次
名校
6 . 下列事实,不能用勒夏特列原理来解释的是
| A.往稀硫酸中加入铁粉,溶液颜色加深 |
B.升高温度, 的醋酸溶液的导电能力增强 的醋酸溶液的导电能力增强 |
| C.拧开可乐瓶盖,有大量气泡冒出 |
| D.实验室制备乙酸乙酯时,使用过量的乙醇作原料 |
您最近一年使用:0次
名校
7 . 氨对发展农业有着重要意义,也是重要的化工原料。合成氨的生产流程示意如下。

下列说法不正确 的是

下列说法
| A.为防止原料气中混有的杂质使催化剂“中毒”而丧失催化活性,原料气必须经过净化 |
| B.压缩机加压过程,既要考虑平衡移动的问题,又要考虑加压对设备材料的强度设备的制造要求的问题 |
| C.合成氨反应的温度控制在500℃左右,此温度下反应物的平衡转化率最大 |
| D.冷却过程,及时将NH3从平衡混合物中分离除去,促使合成氨反应向生成氨气的方向移动 |
您最近一年使用:0次
名校
解题方法
8 . 在一容积可变的密闭容器中加入一定量的X、Y,发生反应mX(g)⇌nY(g) ∆H=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
下列说法正确 的是
| 温度(℃) | c(Y)/(mol/L) | ||
| 1L | 2L | 4L | |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
| A.m>n |
| B.Q<0 |
| C.体积不变,温度升高,平衡向逆反应方向移动 |
| D.温度不变,压强增大,Y的质量分数减少 |
您最近一年使用:0次
2024-01-18更新
|
32次组卷
|
22卷引用:2015-2016学年云南省昆明三中高二下期中化学试卷
2015-2016学年云南省昆明三中高二下期中化学试卷(已下线)2011-2012学年江西省上高二中高二上学期第三次月考化学试卷(已下线)2011-2012学年湖南省望城县第一中学高二上学期期末质量检测化学试卷(已下线)2012-2013学年河北省邢台一中高一下学期第三次月考化学试卷(已下线)2013-2014学年黑龙江省哈师大附中高二上学期期中化学试卷(已下线)2013-2014学年安徽省屯溪一中高二上学期期中考试化学试卷(已下线)2014年高二化学人教版选修四 8化学平衡移动练习卷(已下线)2015届黑龙江省双鸭山市第一中学高三9月月考化学试卷(已下线)2014-2015湖南省新化一中高二上学期期中化学试卷2014-2015学年内蒙古包头市第一中学高一下学期期末考试化学试卷2015-2016浙江宁波效实中学高二上期中考试化学试题卷2016-2017学年四川省成都开发区实验中学高二10月月考化学卷辽宁省大连市第二十四中学2017-2018学年高二上学期期中考试化学试题黑龙江省孙吴县第一中学2017-2018学年高二上学期期中考试化学试题步步为赢 高二化学暑假作业:作业九 化学反应速率和化学平衡吉林省白城市第一中学2018-2019学年高一下学期期末考试化学试题福建省三明市三地三校2020-2021学年高二上学期期中联考化学试题吉林省延边朝鲜族自治州汪清县第四中学2020-2021学年高二上学期期末考试化学试题黑龙江省鹤岗市第一中学2021-2022学年高二上学期期中考试化学试题湖南师范大学附属中学2021-2022学年高一下学期期末考试化学试题湖南省常德市第一中学2023-2024学年高二上学期12月月考化学试题海南省琼海市嘉积中学2023-2024学年高二上学期期末考试化学试题A卷
名校
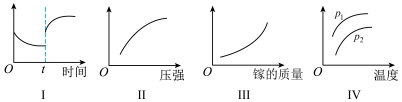
9 . 工业上利用固体Ga与 高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol
高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol 时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
 高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol
高温条件下合成半导体材料氮化镓(GaN)固体,同时有氢气生成。反应中,每生成3mol 时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
时放出30.8kJ的热量。恒温恒容密闭体系内进行上述反应,下列有关下图的表达正确的是
| A.I图像中如果纵坐标为正反应速率,则t时刻改变的条件可以为升温或加压 |
B.Ⅱ图像中纵坐标可以为 的百分含量 的百分含量 |
| C.Ⅲ图像中纵坐标可以为化学反应速率 |
D.Ⅳ图像中纵坐标可以为体系内混合气体平均相对分子质量,且 |
您最近一年使用:0次
名校
解题方法
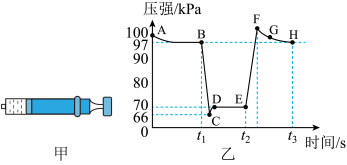
10 . 利用传感技术可探究压强对 化学平衡移动的影响。往注射器中充入适量
化学平衡移动的影响。往注射器中充入适量 气体如图甲所示;恒定温度下,再分别在
气体如图甲所示;恒定温度下,再分别在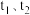 时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图乙所示。下列说法中错误的是
时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图乙所示。下列说法中错误的是
 化学平衡移动的影响。往注射器中充入适量
化学平衡移动的影响。往注射器中充入适量 气体如图甲所示;恒定温度下,再分别在
气体如图甲所示;恒定温度下,再分别在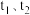 时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图乙所示。下列说法中错误的是
时快速移动注射器活塞后保持活塞位置不变,测得注射器内气体总压强随时间变化的曲线如图乙所示。下列说法中错误的是
A.在B、E两点,对应的正反应速率: |
| B.C到D点平衡逆向移动,针筒内气体颜色D比B点深 |
C.B、H两点,对应的 浓度相等 浓度相等 |
D.B点处 的转化率为6% 的转化率为6% |
您最近一年使用:0次



